第六章
肠道疾病
第一节
功能性胃肠病

王吉耀 朱畴文
功能性胃肠病(functional gastrointestinal disorders,FGIDs)是由生物、心理、社会因素共同作用而引起的肠道与脑相互作用异常、没有生理结构异常为基础的一组表现为慢性或反复发作的胃肠道症状的综合征。是多种因素(包括肠道微生态、黏膜免疫功能的改变、肠道信号变化内脏高敏、中枢神经系统对肠道信号和运动功能调节异常)相互作用的结果。
【分类】
2006年5月,FGIDs国际专家工作组推出了《功能性胃肠病罗马Ⅲ新分类和诊断标准》,2011年工作组成立了17个委员会修订罗马Ⅲ,2014年召开会议,2016年发表了罗马Ⅳ标准(表15-6-1)。
表15-6-1 罗马Ⅳ标准功能性胃肠病的分类(成人)

续表

注:上述标准要求在诊断前症状至少存在6个月,且最近3个月有活动症状
一、癔 球 症
癔球症(globus hystericus)是主观上有某种说不清楚的东西或团块,在咽底部环状软骨水平处引起胀满、受压或阻塞等不适感,中医学称为“梅核气”。中年患者多见,男女无差别。没有证据证明该病与咽喉部任何解剖结构异常有关。起病时多有精神心理因素,提示发病很可能与内脏敏感性增加、焦虑和郁抑有关。病理生理研究提示与发生食管动力障碍者的喉和下咽部炎症、咽部环状肌痉挛、反流性喉炎、上食管括约肌压力升高、松弛不协调相关。临床表现主要为特殊形式的咽下困难,经常做吞咽动作以求解除症状,有咽部异物感等,但是吞咽食物无困难。胃镜和直接喉镜检查不能发现咽食管部有任何器质性病变或异物。食管测压无明确压力改变。有报警症状如吞咽痛、声音嘶哑、体重减轻应该做进一步检查。
罗马Ⅳ标准把癔球症列为功能性食管疾病的一种,其诊断标准为:诊断前症状出现至少6个月,1周至少发作1次,近3个月满足以下所有标准:
1.喉部持续或间断的无痛性团块或异物感,体检、内镜未见异常①感觉出现在两餐之间;②没有吞咽困难或吞咽痛;③近端食管无胃黏膜异位。
2.没有胃食管酸反流病和嗜酸性粒细胞食管炎引起症状的证据。
3.无食管运动障碍病 如贲门失弛缓、食管胃流出道梗阻、弥漫性食管痉挛、食管无蠕动和胡桃夹食管。
本病缺少有效的药物治疗,对本病的解释和对患者心理疏导对缓解症状有效。
二、嗳气疾病
可以听到气从食管或胃到达咽喉部,称为嗳气。罗马Ⅳ将罗马Ⅲ中嗳气疾病的吞气症删除,而根据气体来源分为胃前(来源于食管)和胃(来源于胃)的过度嗳气。
诊断标准:症状出现至少6个月,近3个月每天至少3次以上,胃前过度嗳气患者有频繁、重复地嗳气,可以多达20次/分。高分辨测压和腔内阻抗测定可用于区分胃前和胃嗳气。其发生常与应激性事件相关。在焦虑性疾病中有较高发生率。过度嗳气也可发生在脑炎、暴食症和强迫症患者,应予以鉴别。
治疗上可通过解释症状、演示正确动作、饮食调整(如避免嚼硬物、口香糖和饮产气饮料,鼓励慢咽、小口吞咽,进食时不说话等),一般不提倡药物治疗,症状严重时,可试用镇静类药物和行为治疗嗳气疾病,通过生物反馈减少膈肌收缩。
三、功能性消化不良
消化不良(dyspepsia)是指源于胃十二指肠区域的一种症状或一组症状,其特异性的症状包括餐后饱胀、早饱感、上腹痛或上腹烧灼感。经检查排除了可引起这些症状的器质性、全身性或代谢性疾病时,这一临床症候群便称为功能性消化不良(functional dyspepsia,FD)。有消化不良症状的患者大约70%是功能性的,曾被称为非溃疡性消化不良。FD是临床上最常见的一种功能性胃肠病,我国人群患病率为18%~45%,占消化门诊的20%~50%,已成为影响现代人生活质量的重要疾病之一。
【发病机制】
FD是多因素引起的,病理生理机制复杂,至今尚未完全清楚,与胃肠动力、感觉异常、黏膜完整性破坏、低度炎症、免疫激活、脑-肠轴调节异常相关。
(一)胃肠运动功能障碍
1/3患者有胃排空延缓,也有1/3患者有胃容受性障碍(适应性舒张不足),并与早饱症状有关,更易出现上腹疼痛和嗳气;患者胃排空延迟、餐后胃窦动力降低,引起餐后腹胀、恶心、呕吐等症状。
(二)内脏感觉异常
胃十二指肠对扩张或酸、脂质等化学物质腔内刺激的敏感性增高。抑酸治疗对少数患者可起到缓解消化不良症状的作用。
(三)Hp感染
是产生FD症状的可能原因。根除Hp后确实有部分FD患者消化不良症状得到改善。也有可能抗Hp时抗生素的应用对肠道菌群产生影响而改善FD症状。
(四)心理社会因素
FD是一种公认的心身疾病,精神、心理因素可能是FD的重要病因。中枢神经系统对内脏高敏感性的发生起重要作用。躯体化、人际敏感、不良生活事件与功能性胃肠道疾病显著相关,焦虑和抑郁等精神障碍和个性异常参与了FD的发生。
(五)胃肠激素紊乱和脑-肠轴功能障碍
胃肠激素如胃动素、胃泌素、胆囊收缩素以及血管活性肠肽、降钙素基因相关肽及P物质等,可能涉足了FD的病理生理机制,且与胃电变化相关。自主神经系统功能异常,尤其是迷走传出神经功能障碍,被认为是胃容受功能受损和胃窦动力低下的可能机制之一。
(六)十二指肠低度炎症、黏膜通透性和食物抗原
感染、应激、十二指肠酸暴露、抽烟食物过敏可引起十二指肠黏膜炎症和通透性改变,黏膜屏障受损,引起FD。
(七)环境因素
急性感染后在部分患者诱发FD。
【临床表现】
1.餐后饱胀
食物长时间存留于胃内引起的不适感。
2.早饱感
指进食少许食物即感胃部饱满,食欲消失,不能进常规量的饮食。
3.上腹痛
位于胸骨剑突下与脐水平以上、两侧锁骨中线之间区域的疼痛,疼痛多无规律性,部分患者与进食有关,有时患者无疼痛感,而主诉为特别的不适。
4.上腹烧灼感
位于胸骨剑突下与脐水平以上、两侧锁骨中线之间区域的难受的灼热感,与烧心不同,后者指胸骨后的烧灼样疼痛或不适,是GERD的特征性症状。
恶心、呕吐并不常见,往往发生在胃排空明显延迟的患者。不少患者同时伴有失眠、焦虑、抑郁、头痛、注意力不集中等精神症状。
FD患者常以上述某一个或某一组症状为主,在病程中症状也可发生变化。起病多缓慢,病程常经年累月,呈持续性或反复发作,不少患者有饮食、精神等诱发因素。
【诊断与鉴别诊断】
(一)诊断标准
根据功能性胃肠病的罗马Ⅳ标准,功能性消化不良的诊断需满足:诊断前症状出现至少6个月,近3个月满足以下标准:
1.主要标准
必须包括以下1条或多条:①餐后饱胀不适;②早饱感;③上腹痛;④上腹烧灼感。通过常规检查(包括内镜)找不到可以解释上述症状的器质性或代谢性疾病的证据。
2.亚型标准
FD根据临床特点,还可以分为以下两个亚型,各自的诊断标准分别为:
(1)餐后不适综合征(postprandial distress syndrome,PDS):
病程6个月,近3个月至少具备以下1个症状,每周至少发作3天:①发生在进平常餐量后的餐后饱胀,严重到影响日常生活;②早饱感使其不能完成平常餐量的进食。支持诊断的条件包括上腹胀或餐后恶心或过度嗳气,可同时存在EPS。
(2)上腹疼痛综合征(epigastric pain syndrome,EPS):
病程6个月,近3个月每周至少1次,必须具备以下所有症状:①上腹部疼痛,严重到影响日常生活;②上腹部烧灼感,严重到影响日常生活。支持诊断的条件包括疼痛常因进餐诱发或缓解,或发生在空腹状态,可同时存在PDS。
(二)诊断程序
FD为一排除性诊断,需全面病史采集和体格检查。确定有无“报警”症状和体征:体重减轻、贫血、上腹包块、频繁呕吐、呕血或黑便、消化不良症状进行性加重、有肿瘤家族史等。对有“报警”症状和体征者,必须彻底检查直至找到病因。没有者可以先行 13 C呼气试验,如果Hp阳性,可以抗Hp治疗。根除Hp后,如果症状继续存在,可以用PPI抗酸治疗。治疗无反应者选择腹部超声检查以及胃镜检查。
对诊断不能肯定者,进行定期随访,可能发现隐蔽的器质性疾病。对有精神心理障碍者,也建议及时进行检查,明确排除器质性疾病对解释病情更为有利。
(三)鉴别诊断
首先需要与引起消化不良的器质性疾病包括食管、胃十二指肠、肝胆胰等病变,特别是消化性溃疡、胃食管反流病(GERD)及恶性病变,也需与以产生上消化道症状为突出表现的其他系统疾病相鉴别,如糖尿病、慢性肾功能不全、充血性心力衰竭、甲状腺功能亢进症及硬皮病等,以及某些药物,包括NSAID类和某些抗生素等。
【治疗】
明确为FD者,应分出亚型,以给予针对性治疗。治疗以缓解症状,提高患者的生活质量为主要目的。
(一)一般治疗
帮助患者认识、理解病情,改善生活习惯,避免烟、咖啡、酒及非甾体类抗炎药。应避免个人生活经历中会诱发症状的食物。建议少食多餐,避免一次大量进食。
(二)药物治疗
1.根除幽门螺杆菌治疗
对Hp阳性患者根除治疗是治疗感染性FD最有成本效益的治疗方法。
2.抑酸药
质子泵抑制剂和选择H 2 受体拮抗剂适用于非进餐相关消化不良中以上腹痛、烧灼感为主要症状者。对减轻PDS症状无效。
3.促胃肠动力药
可改善与进餐相关的上腹部症状,以上腹饱胀、早饱、嗳气为主要症状患者常作为优先选用,常用药有多潘立酮(10mg,3次/日)、莫沙必利(5mg,3次/日)或伊托必利,均在餐前15~30分钟服用,疗程2~8周。少部分患者有腹鸣、稀便或腹泻、腹痛不良反应,减量或使用一段时间后这些不良反应可减轻。
4.精神心理治疗
抗抑郁药作为二线治疗药物,常用的有三环类如阿米替林、5-HT再摄取抑制药如氟西汀等。此外,行为治疗、认知疗法和心理干预等也可试用。
四、肠易激综合征
肠易激综合征(irritable bowel syndrome,IBS)是临床上最常见的一种功能性肠病,以与排便相关的反复发作的腹痛和排便习惯改变为主要特征。是最常见的消化性疾病之一,我国患病率约7%~12%。对年轻人影响大于50岁以上者。女性较男性多见,有家族聚集倾向。IBS对患者的生活质量和社会交往有明显的负面影响,并直接或间接地消耗大量的医疗保健资源。
【病因与发病机制】
IBS是多因素影响的疾患。有复杂的病理生理机制,包括遗传、环境和心理因素。触发和加重IBS的因素包括胃肠炎病史、食物不耐受、慢性应激、憩室病和外科手术。发病机制因人而异,差异很大。包括胃肠动力的异常、内脏高敏感性、小肠通透性增加、免疫激活、肠道菌群改变和脑-肠轴调节功能紊乱。
(一)胃肠动力异常
长期以来胃肠道动力学异常是症状发生的主要病理学基础,腹泻型IBS患者结肠运动指数增多,各段结肠推进性蠕动明显增加,以降乙结肠明显,并可伴腹痛。而便秘型IBS患者则多表现为痉挛性收缩和腹胀,结肠节段性收缩增加,高幅推进性收缩减少。腹泻型IBS患者胃结肠反射呈持续的增高反应,便秘型则反应减少。
(二)内脏高敏感
大量研究普遍观察到IBS患者对各种生理性和非生理性刺激(如进食、肠腔扩张、肠肌收缩、肠内化学物质、某些胃肠激素等)极为敏感,较易感到腹痛,即痛阈降低,甚至对正常状态下的肠蠕动亦较常人更易感觉到。这种感觉异常的神经生理基础可能是黏膜及黏膜下的内脏传入神经末梢兴奋阈值降低,和(或)中枢神经系统对传入神经冲动的感知异常,以及传出神经对传入信息的负反馈抑制的调控能力的减弱,从而相对增强了痛觉信号。
(三)肠道免疫激活、小肠通透性及肠道微生态的改变
大量研究提示IBS与肠道感染有关,2/3IBS患者的黏膜活检有低度炎症和肥大细胞浸润。急性感染是诱发IBS的危险因素之一,在近期有细菌性胃肠炎患者中约7%~30%发生IBS,为“感染后的肠易激综合征”。在小肠炎症和通透性增加的情况下,食物抗原通过肠上皮屏障间隙,导致肥大细胞浸润激活,释放介质,激活免疫系统。近期报道麦麸、可发酵寡聚糖、二糖、单糖及多元醇(fermentable oligo-,di-,and monosaccuarides and polyols,FODMAPs)等快速发酵、有渗透活性的短链碳水化合物被识别为IBS症状的重要诱发因素,吸收性差的碳水化合物发挥渗透效应,增加肠内发酵,加重症状。研究还发现IBS患者粪微生物群与健康对照差异明显。
(四)中枢感觉异常和神经内分泌
研究表明IBS患者存在CNS的感觉异常和调节异常,IBS可以被认为是对脑-肠系统的超敏反应,包括对肠神经系统和CNS。由于脑-肠轴还通过胃肠激素等神经内分泌系统达到胃肠功能调节的目的,5-HT已被认为是参与胃肠道动力和感觉非常重要的神经递质,其3型和4型受体对5-HT激动药或拮抗药的不同反应是近年来药物治疗开发的热点。研究还发现,IBS患者血浆中胆囊收缩素(CCK)、生长抑素(SS)和胃动素的浓度也有明显改变。
(五)社会心理因素
IBS症状的发生、严重程度与精神紧张应激强度相关。IBS患者往往同时有心理和精神障碍,社会心理因素对IBS患者的影响可能通过CNS介导。包括情感、性、生理虐待史、睡眠剥夺、应激生活事件、长期社会应激以及不良的心理应付等。近期研究发现焦虑、紧张、抑郁可直接作用损伤肠黏膜屏障,有利于大分子物质通过,激活免疫系统。
此外,IBS有明显家族聚集的倾向,因此基因易感性遗传因素也需认真考虑。
【临床表现】
IBS起病通常缓慢、隐匿,间歇性发作,有缓解期;病程可长达数年至数十年,但全身健康状况却不受影响。胃肠道症状有:
1.腹痛
与排便相关,为一项主要症状且为IBS必备症状,大多伴有排便异常并于排便后缓解或改善,部分患者易在进食后出现;发生于腹部任何部位,局限性或弥漫性,性质、程度各异,但不会进行性加重,极少有睡眠中痛醒者。不少患者有排便习惯的改变,如腹泻、便秘或两者交替。
2.腹泻
一般每日3~5次,少数可达十数次。粪量正常(<200g/d),禁食72小时后应消失,夜间不出现(这点极罕见于器质性疾患),通常仅在晨起时发生,约1/3患者可因进食诱发。大便多呈稀糊状,也可为成形软便或稀水样。可带有黏液,但无脓血。排便不干扰睡眠。
3.便秘
为排便困难,粪便干结、量少,呈羊粪状或细杆状,表面可附黏液;亦可间或与短期腹泻交替,排便不尽感明显,粪便可带较多黏液;早期多为间断性,后期可为持续性,甚至长期依赖泻药。
4.其他
腹胀在白天加重,夜间睡眠后减轻。近半数患者有胃灼热、早饱、恶心、呕吐等上消化道症状,常伴非结肠源性症状和胃肠外症状,如慢性盆腔痛、性功能障碍和风湿样症状等。
部分患者尚有不同程度的心理精神异常表现,如抑郁、焦虑、紧张、多疑或敌意等,精神、饮食等因素常可诱使症状复发或加重。
【诊断与鉴别诊断】
(一)诊断
1.罗马Ⅳ诊断标准
在诊断前至少6个月最近3个月内每周至少1天反复发作腹痛,且伴有以下两条或两条以上:①与排便相关;②发作时伴排便次数的改变;③发作时伴排便性状的改变。
2.罗马Ⅳ标准根据Bristol大便性状分型(BSFS)(资源 57)
作为IBS亚型的分型标准(基于患者14天的日记):
(1)IBS便秘型(IBS-C):
块状/硬便(BSFS:1~2型)>25%,且稀/水样便(BSFS:6~7型)<25%。
(2)IBS腹泻型(IBS-D):
稀/水样便>25%,且块状/硬便<25%。
(3)IBS混合型(IBS-M):
稀便和硬便均>25%。
(4)IBS未定型(IBS-U):
排便性状改变未达到上述三型要求。根据症状分为IBS伴腹泻和IBS伴便秘。

(资源57) Bristol大便性状分型(图)
IBS的诊断属排除性诊断。按上述标准,谨慎地排除可引起腹痛、腹泻、便秘的各种器质性疾病基础上可作出诊断。因此,一般通过详细询问病史、临床特征、用药史以及心理精神史和常规的体检即可诊断大部分IBS,诊断作出后还要注意随访,以确保诊断的正确性。一般而言,在仔细体格检查(包括直肠指检)的基础上,应常规检测全血细胞计数、大便潜血和镜检、肝功能检查、红细胞沉降率(ESR)和C反应蛋白。对有报警症状(包括发热、体重下降、便血或黑便、贫血、夜间或顽固性腹泻、严重便秘、腹部包块以及年龄因素)者,应做肠镜和其他进一步检查。
3.推荐诊断程序
①首先根据病史和临床特征等症状为基础作出初步诊断,诊断较明确者可试行诊断性治疗并进一步观察;②对新近出现持续的大便习惯(频率、性状)改变或与以往发作形式不同或症状逐步加重者、有上述报警症状、有大肠癌/结肠息肉/IBD/乳糜泻家族史者、年龄≥40岁者,应将结肠镜检查列为常规。对无上述情况,年龄在40岁以下,具有典型IBS症状者,粪常规为必要检查。IBS患者有一部分症状与器质性疾病是重叠的。例如:甲状腺疾病、乳糜泻、炎症性肠病、显微镜下结肠炎、乳糖不耐受、小肠细菌过度生长,甚至结肠癌,如果缺乏报警症状,临床表现都可类似IBS。因此对怀疑IBS的患者进行一些针对性的检查,是有一定临床意义的。对于诊断可疑和症状顽固、治疗无效者,应有选择性地作进一步检查以排除器质性疾病:血钙,甲状腺功能检查,乳糖氢呼气试验,粪便培养和镜检,72小时粪便脂肪定量,胃肠道内镜检查和抽取胃十二指肠液镜检、培养(以排除小肠细菌污染综合征和某些寄生虫感染,如贾第鞭毛虫),小肠CT,胃肠通过时间测定,肛门直肠压力测定,钡灌肠,排粪造影,胃十二指肠压力测定,腹部B超和CT, 75 Se类胆酸牛磺酸试验( 75 Se HCAT,用于观察有无胆汁酸吸收不良),抗肌内膜抗体,肠腔放置气囊和直肠测压等运动功能检查。
(二)鉴别诊断
1.以腹泻为主的IBS
应与肠道炎症性疾病相鉴别,如肠道感染(细菌、病毒、寄生虫、HIV-相关性、肠结核)、IBD(溃疡性结肠炎和克罗恩病)、结肠癌、神经内分泌肿瘤、饮食(麦麸、酒精、FODMAPs)、药物(化疗药、NSAIDs、SSRIs、抗生素)、吸收不良(胰功能障碍、小肠疾患)等加以鉴别。有时与功能性腹泻(持续性或反复排糊状便或水样便,不伴有腹痛)在临床上鉴别较为困难。
2.以便秘为主的IBS
除了与由于妊娠、饮食习惯改变或外出旅游等有关的偶发便秘鉴别外,需与结肠癌、内分泌病(如甲减、甲状旁腺功能亢进)、神经病(如帕金森病、多发性硬化症),以及药物(化疗、钙通道阻滞剂等)引起的相鉴别。
3.以腹痛为主的IBS
应与妇科疾病(卵巢癌、子宫内膜异位症)和精神疾病(如抑郁、焦虑、躯体化)引起腹痛相鉴别。功能性消化不良亦引起腹痛,文献报道两种疾病的重叠率在30%以上,若患者还存在上述预警症状,需立即行内镜检查以资鉴别。
4.鉴别诊断
还应包括甲状腺功能亢进症、胃泌素瘤、乳糖酶缺乏症、肠道吸收不良综合征等。一般而言,以下临床症状不支持IBS的诊断,而多提示存在肠道器质性疾病:老年起病,进行性加重,惊扰睡眠,发热,明显消瘦,脱水,吸收不良,夜间腹泻,大便带脓血或脂肪泻,直肠出血,腹痛与排便关系不肯定,心身疾病多继发于症状等。
总之,IBS是指一组以腹痛、腹胀、排便习惯和大便性状异常,缺乏特异性的形态学、生化和感染性病因的症候群。临床上以症状为诊断基础,结合肠镜和钡剂灌肠检查排除肠道器质性病变后可成立诊断。
【治疗】
目的是消除患者顾虑,改善症状,提高生活质量。治疗原则是在建立良好医患关系基础上,根据症状严重程度进行分级治疗和根据症状类型进行对症治疗。注意治疗措施的个体化和综合运用。建议采用综合治疗,应包括精神心理行为干预治疗、饮食调整及药物治疗。
(一)建立良好的医患关系
是最有效、经济的IBS治疗方法,也是所有治疗方法得以有效实施的基础。在这种关系中,医生须注意倾听、分析解释、明确问题和期望、给予答复,并使患者参与到治疗过程中,使患者树立信心,增加信任,从而减少患者的就医次数,提高患者的满意度。
(二)饮食
包括调整饮食(减少FODMAPs的摄入),避免以下因素:过度饮食、大量饮酒、咖啡因、高脂饮食、某些具有“产气”作用的蔬菜、豆类等、精加工面粉和人工食品、山梨糖醇及果糖。便秘为主要症状的IBS患者,注意调整膳食纤维及纤维制剂:如谷物、水果、蔬菜、种子、坚果和豆类等主要膳食纤维,包括水溶性纤维如欧车前(psyllium)、卵叶车前(ispaghula)、以及非水溶性纤维(如纤维素、半纤维素和木质素等)。一般从低剂量开始逐步增加剂量并应个体化。发现由饮食引起的不良反应(食物不耐受、食物过敏)采用食物过敏原皮肤试验和食物激发试验发现致敏食物,包括亚裔人群常见的乳糖不耐受,行剔除饮食治疗。
(三)药物治疗
对药物的选择应因人而异,对症处理。以腹泻症状为主要表现的IBS患者的药物治疗可选择解痉、止泻类药物;以便秘症状为主要表现的IBS患者的药物治疗可选择促动力、通便类药物,但应避免应用刺激性缓泻剂;以腹痛、腹胀为主要表现的IBS患者的药物治疗可选择具有调节内脏感觉作用的药物,纠正内脏感觉异常,缓解症状;具有明显抑郁和(或)焦虑等精神障碍表现者,应考虑给予心理行为干预的认知疗法及低剂量抗抑郁、抗焦虑药物治疗。
1.解痉药
抗胆碱能药物除阿托品和莨菪碱类外,常使用相对特异性肠道平滑肌钙离子通道拮抗药,调节肠道运动,如匹维溴胺50mg,3次/日;奥替溴胺40mg,3次/日。另外,曲美布汀为外周性脑啡肽类似物,作用于外周阿片类受体以刺激小肠动力和阿络酮通路以抑制结肠动力,是一种胃肠运动双向调节剂,100mg,3次/日。薄荷油有钙通道阻滞特性200mg,3次/日,不良反应非常罕见。
2.止泻药
IBS-D可选用洛哌丁胺,为人工合成的外周阿片肽μ受体激动剂,2~4mg,4次/日,或复方地芬诺酯(苯乙哌啶),每次1~2片,2~4次/日;但需注意便秘、腹胀等不良反应。轻症者可选用吸附剂,如双八面体蒙脱石等。
3.导泻药
IBS-C可使用导泻药,一般主张使用作用温和的缓泻药以减少不良反应和药物依赖性。如乳果糖15~30ml睡前服,或乳果糖10~15ml,3次/日、山梨醇5~10g,3次/日;也常用渗透性轻泻剂如聚乙二醇(PEG4000)、容积性泻剂如欧车前制剂或甲基纤维素等。
4.促泌剂
卢比前列酮是氯离子通道激活剂,可刺激肠道分泌液体,改善IBS-C症状。
5.肠道感觉和(或)动力调节药
非多托嗪(fedotozine):是阿片类κ受体激动剂,特异性抑制外周内脏传入神经而降低内脏敏感性,30~70mg,3次/日,能有效地缓解IBS患者的腹痛症状。促动力药如多潘立酮10mg,3次/日;莫沙必利,5~10mg,3次/日或伊托必利均可用于IBS-C的治疗。普卡必利(prucalopride)是5HT4激动剂用于IBS-C,1~2mg/d。
6.益生菌
某些益生菌可以减低肠道细胞钙离子通道和类阿片受体的表达,减少循环中细胞因子的水平。从而减少内脏的高敏感性和炎症反应,在IBS中起作用。证据显示益生菌比安慰剂更加有效。可作为患者(特别是有腹痛和胀气患者)的二线用药。
7.抗生素
利福昔明-α是非吸收抗生素,用于IBS-D,200mg,每日4次,10~14天。对于非便秘型IBS和胀气也有效。
8.抗抑郁药
对腹痛症状重而上述治疗无效,特别是伴有较明显精神症状者可试用。腹泻型患者可用三环类抗抑郁药,如阿米替林10~50mg,2~4次/日。便秘型患者中,选择性5-羟色胺重再摄取抑制药,如帕罗西汀或西酞普兰,可加快小肠传递,并避免三环类抗抑郁药最常见的便秘不良反应。
小剂量的抗抑郁药还可显著地降低内脏敏感性,减少胃肠道症状。患者常常反感医生对其使用抗抑郁药,导致依从性差。因此,应用抗抑郁药的关键在于用药前对患者进行充分解释,使患者理解用药意图并愿意试用。
(四)改进生活方式和心理和行为治疗
睡眠差会加重IBS症状,每周3~5次,每次20~60分钟的有氧运动可以减轻症状。许多研究认为认知行为治疗、标准心理以及催眠疗法对部分IBS患者具有一定疗效。
(五)中医药治疗
中药、针灸等治疗IBS的疗效,有待进一步验证。
【预后】
IBS呈良性过程,症状可反复或间歇发作,影响生活质量,但一般不会严重影响全身情况。在医师的持续关注下,经进一步咨询、健康教育和合理用药,可在数周至数年内达到症状的缓解。无疗效者可增加精神社会学的支持治疗和应用一些有特殊作用的药物;对重症、顽固的病例,不必追求治愈,更应着力于患者功能的改善,提高生活质量。
五、功能性便秘
便秘一般即指慢性便秘,主要是指粪便干结、次数减少、排便困难或不尽感以及在不用通便药时完全排空粪便的次数明显减少等。上述症状若同时存在2种以上时,可诊断为症状性便秘。便秘的病因包括功能性和器质性两种。如能排除便秘的器质性病因,如由胃肠道疾病、累及消化道的系统性疾病如糖尿病、神经系统疾病等引起,即可诊断为功能性便秘(functional constipation,FC)。
【病因与发病机制】
正常的排便生理过程包括产生便意和排便动作两个过程:①肠内容物以正常速度通过各段,粪便及时抵达直肠,直肠扩张引起排便反射即发生便意;②经直肠排出,排便动作受到大脑皮质和腰骶部脊髓内低级中枢的调节,通过直肠收缩、肛门括约肌松弛、两旁侧肛提肌收缩、盆底下降、腹肌和膈肌也协调收缩,腹压增高,促使粪便排出肛门。正常排便生理过程中出现某一环节的障碍都可能引起便秘。
功能性便秘的危险因素包括生活方式、心理压力等。根据病理生理学机制可将患者分为排空迟缓型、功能性出口梗阻型和合并或混合型。
(一)排空迟缓型
又称慢传输型便秘(slow transit constipation,STC)或结肠无力,在特发性便秘中占13%,是指肠内容物从近端结肠向远端结肠和直肠运动的速度低于正常人,这种异常被证明与异常的肠道动力有关,其机制包括结肠高幅推进性收缩数量减少和远端不协调的运动增多,可能存在肠肌间神经丛的异常(如Cajal间质细胞数量减少)和肠神经递质(如 VIP、NO、5-TH)水平下降。
(二)功能性
出口梗阻型便秘(outlet obstructive constipation,OOC)又称为盆底功能障碍或盆底肌协调运动障碍,是指粪便堆积于直肠内而不能顺利地从肛门排出,占28%,可伴有轻度的结肠传输减慢或正常。导致盆底功能障碍的机制很复杂且不明确,可分为盆底肌群张力过高(不能松弛或松弛不良或矛盾运动)以及肌肉张力过低(巨直肠和严重的盆底下垂)。这些异常包括横纹肌、平滑肌功能不良和动力障碍、直肠感觉损害、中枢或盆腔阴部神经功能异常等。
(三)混合型便秘
兼备以上两型的原因特点。
【临床表现】
有时患者唯一的主诉是粪便干结、排便费力。结肠痉挛引起便秘时,排出的粪便呈羊粪状。由于用力排出坚硬的粪块,可引起肛门疼痛、肛裂,甚至诱发痔疮和乳头炎。有时,在排便时由于粪块嵌塞于直肠腔内难于排出,但有少量水样粪质绕过粪块自肛门排出,而形成假性腹泻。部分患者排便时可有左腹痉挛性痛和下坠感。另外还可有腹痛、腹胀、恶心、口臭、食欲缺乏、疲乏无力及头痛、头昏等症状。体检时,常可在降结肠和乙状结肠部位触及粪块及痉挛的肠段。
【实验室与辅助检查】
(一)实验室检查
血常规、甲状腺素、血清钙等。
(二)结肠镜检查
可直接观察黏膜是否存在病变,并可做活组织检查以明确病变的性质,以排除器质性病变。
(三)特殊检查
胃肠通过试验(gastrointestinal transit test,GIT),肛门直肠测压(anorectal manometry,ARM),排粪造影(barium defecography,BD),气囊排出试验(balloon expulsion test,BET),结肠压力监测等。其他还包括放射性核素直肠造影、盆底肌电图和肛门超声内镜检查等。
【诊断与鉴别诊断】
(一)诊断标准
采用罗马Ⅳ标准,在排除器质性疾病导致的便秘后,符合以下情况者可判定为功能性便秘:诊断前症状出现至少6个月,近3个月症状有下列特点:
1.必须符合以下两点或两点以上:①至少25%的排便感到费力;②至少25%的排便为块状便或硬便;③至少25%的排便有不尽感;④至少25%的排便有肛门直肠梗阻感/阻塞感;⑤至少25%的排便需以手法帮助(如以手指帮助排便、盆底支持);⑥每周排便<3次。
2.不使用轻泻药时几乎无松软便。
3.没有足够的证据诊断IBS。
(二)诊断程序
1.详细的病史询问
(包括症状的时间长度、排便频率、是否伴腹痛腹胀、大便的性状数量、排便的困难程度、有无可导致便秘药物的服用史)、体格检查(腹部检查和直肠指检为必要项目)、有关的实验室检查、结肠镜、影像学检查和特殊检查等方法,排除引起便秘的器质性或医源性疾病,如代谢性、神经性、(如中枢神经系统和脊髓损伤)肌肉性、机械性、药物性以及其他可能的因素。对于近期出现便秘、特别有报警症状(年龄>40岁,便血、粪隐血阳性、贫血、消瘦、腹块、有结直肠息肉史和结直肠肿瘤家族史者)者,应做结肠镜排除结直肠肿瘤。
2.区分便秘类型
①慢传输型便秘:常有排便次数减少,少便意,粪质坚硬,因而排便困难;直肠指检时无粪便或触及坚硬的粪便,而肛门外括约肌的缩肛和用力排便功能正常;全胃肠或结肠通过时间延长,肛门直肠测压显示正常。②出口梗阻型便秘:排便费力、不尽感或下坠感、排便量少,有便意或缺乏便意;肛直肠指检时直肠内存有不少泥样粪便,用力排便时肛门外括约肌呈矛盾性收缩;全胃肠或结肠通过时间显示正常,多数标志物可潴留在直肠内;肛门直肠测压显示用力排便时肛门外括约肌呈矛盾性收缩或直肠壁的感觉阈值异常。③混合型便秘,具备①和②的特点。有严重便秘而传输时间正常者,常有更多的心理压力和异常的疾病行为。
3.判别程度
根据便秘有关症状轻重及对生活影响的程度分为轻、中、重3度:轻度,症状较轻,不影响生活,整体调整治疗即可,无须用药;重度或难治性便秘,便秘症状持续,严重影响生活甚至工作,需用药通便排便,不能停药或药物治疗无效者;中度,介于轻、重之间。
(三)鉴别诊断
主要与器质性或医源性疾病引起的便秘鉴别,例如肛门直肠结构异常疾病(瘘管,栓塞性痔,狭窄,肿瘤占位)、内分泌/代谢疾病(糖尿病,高钙血症,低钾血症,甲状腺功能减退,甲状旁腺功能亢进)、神经源性疾病(脑血管意外、帕金森病、脊髓肿瘤)、平滑肌或结缔组织疾病(淀粉样变性、硬皮病)、药物(止痛药:麻醉药、非甾体类抗炎药物;抗酸药:氢氧化铝、碳酸钙;抗胆碱能药物;抗抑郁药物、抗高血压及抗心律失常药物:钙通道阻滞剂,特别是维拉帕米;金属:铋剂、铁剂、重金属;拟交感神经作用药物:伪麻黄素)。
还应与以便秘为主要表现的肠易激综合征(IBS)鉴别,FC也可以有腹痛和胀气,但并非主要症状,不符合IBS的诊断标准。
【治疗】
治疗原则是根据便秘轻重、病因和类型,采用综合治疗,包括一般治疗、药物治疗、生物反馈训练和手术治疗。治疗目的是使患者缓解症状、恢复排便生理。
(一)一般治疗
包括对患者进行健康教育,了解便秘的慢性过程,为了治疗的成功而改变生活方式,包括适当的体育活动,增加液体和食物纤维的摄入,养成定时排便的习惯,如早餐后10~15分钟排便(利用胃结肠反射)等。并可适当予以心理治疗,在仔细排除引起便秘的病理性因素后,对患者做充分解释,让其消除疑虑、确立信心,并告诫患者某些非处方药物和长期精神紧张的危害,增进患者对治疗的依从性。对在应激或情绪障碍情况下加重便秘的患者,可行心理治疗。
(二)泻药
经上述处理仍未奏效者,可适当地使用轻泻剂,其基本作用为刺激肠道分泌和减少吸收,增加肠腔内渗透压和流体静力压。也应告诫患者避免过度使用轻泻剂。
1.容积性泻药
能加速结肠和全胃肠道运转,吸附水分,使大便松软易排,缓解便秘及排便紧迫感,由于它的安全性常为治疗的首选,主要包括可溶性纤维素(果胶、车前草、燕麦麸等)和不可溶纤维(植物纤维、木质素等),可供使用的有欧车前、聚卡波非钙、麦麸、甲基纤维素。促肠分泌药卢比前列酮(24μg,2次/日,与食物同服)可以增加排便次数、改善性状,减少排便困难。
2.润滑性泻剂
能润滑肠壁,软化大便,使粪便易于排出,使用方便,如开塞露、矿物油或液状石蜡,每次10~30ml。
3.渗透性泻剂
常用的药物有乳果糖(10~15g,3次/日)、山梨醇(5~10g,3次/日),聚乙二醇4000等。后者适用于粪块嵌塞或作为慢性便秘者的临时治疗措施。每日可摄入聚乙二醇较小剂量(20g),即可产生有效的导泻作用,是对容积性轻泻剂疗效差的便秘患者的较好选择。
4.刺激性泻剂
药物或其代谢物能够刺激肠壁,增强肠蠕动,促进排便。长期使用可出现依赖,造成结肠黑变病,产生不可逆的肠神经系统损害。包括含蒽醌类的植物性泻药(大黄、弗朗鼠李皮、番泻叶、芦荟)、酚酞、双醋酚丁、蓖麻油等。刺激性泻剂应在容积性和盐类泻剂无效时短期使用。
5.软化性泻药
如二辛基硫酸琥珀酸钠50~250mg/d。
(三)促动力药
用于慢传输型便秘,有莫沙必利、伊托必利。选择性作用于结肠5-HT受体的普卡必利(1~4mg/d)可改善大便性状、频次和排便困难等症状。
(四)微生态制剂
能防止有害菌的定植和入侵,补充有效菌群发酵糖产生大量的有机酸,使肠腔内pH值下降,调节肠道正常蠕动,改变肠道微生态环境,改变粪便性状有利粪便排出,对缓解便秘和腹胀均有一定的作用。
(五)中医中药
中医主张辨证施治,有些验方如中药敷脐辅助治疗显示疗效,但大多数的中药方剂等,尚没得到有效验证。
(六)清洁灌肠
对有粪便嵌塞或严重排出道阻滞性便秘需采用清洁灌肠,或采用栓剂(甘油栓)。
(七)生物反馈治疗
借助声音和图像反馈刺激大脑,通过测量内脏功能使患者了解自己的生理异常,从而学会纠正这种异常。常用于出口梗阻型便秘。
(八)手术治疗
经过正规保守治疗仍无效者,才考虑外科手术治疗,用于功能性便秘的治疗不多。应注意有无严重的心理障碍,术前需要进行疗效预测。经生理学和心理学两方面的严格评价后慎重选择。近年来,腹腔镜手术治疗慢性便秘愈来愈受到关注。
主要参考文献
1.中华医学会消化病学分会胃肠动力学组.外科学分会结直肠肛门外科学组.中国慢性便秘的诊治指南(2013,武汉).中华消化杂志,2013,33(5):291-297.
2.Drossman DA.Functional gastrointestinal disorders:history,pathophysiology,clinical features,and RomeⅣ.Gastroenterology,2016,150(6):1262-1279.
3.Lacy BE,Mearin F,Chang L,et al.Bowel disorders.Gastroenterology,2016,150(6):1393-1407.
第二节
胃肠道间质瘤

刘天舒
胃肠道间质瘤(gastrointestinal stromal tumors,GIST)是起源于胃肠道间叶组织的肿瘤,是消化道最常见的软组织肿瘤,估计年发病率约为10~20/100万。GIST可起源于胃肠道的任何部位,但是大部分发生于胃(60%)和小肠(30%),十二指肠和直肠原发较少见,极少起源于食管和阑尾。GIST好发年龄为40~69岁,男女发病率无明显差异。
【病因与发病机制】
目前认为GIST的发生与患者特征性的基因改变密切相关。根据目前已知的基因改变,GIST分为3类: c-kit 基因突变型(80%~85%), PDGFR 基因突变型(5%~10%)和野生型(约10%)。
原癌基因 c-kit 位于人染色体4q12,其产物是Ⅲ型酪氨酸激酶受体,即CD117。GIST中至少存在 c-kit 4个位点的突变:11号外显子(60%~70%),9号外显子(5%~15%),13号外显子(1%),17号外显子(1%)。
血小板衍生生长因子受体-α(platelet-derived growth factor receptor alpha, PDGFR-α )由定位于人染色体4q12的 PDGFR-α 基因编码,位于细胞膜表面,属于酪氨酸激酶受体的一种。 PDGFR-α 基因突变型GIST患者的突变大多数(80%)发生在 PDGFR-α 基因第18号外显子。
还有约10%的GIST患者不存在 c-kit 基因或 PDGFR-α 基因突变,被称为野生型GIST。
【病理】
(一)大体病理学特征
GIST好发部位依次为胃、小肠、结直肠和食管。肿瘤呈局限性生长,常表现为孤立、界限清楚的结节,大体形态呈结节状或分叶状,切面呈灰白色、红色,均匀一致,质韧,可见出血、坏死、黏液变及囊性变。
(二)组织病理学特征
根据组织学表现,GIST主要分为3型:梭形细胞为主型,上皮样细胞为主型和混合细胞型。其中梭形细胞为主型最常见。
(三)免疫组织化学特征
CD117是胃肠道间质瘤的特异性指标,90%以上的胃肠道间质瘤表达CD117。在CD117表达阴性的GIST患者中,约35% PDGFR-α 表达阳性。此外,琥珀酸脱氢酶亚基蛋白(succinate dehydrogenase subunits B,SDHB)表达缺失可协助鉴别野生型GIST。
功能未知蛋白1(discovered on GIST 1,DOG1)是一个钙离子依赖的受体激活氯离子通道蛋白,其在GIST中高表达,阳性率约80%~97%,且与基因突变类型不相关,可协助诊断GIST。
GIST患者中其他一些高表达指标有:细胞间黏附糖蛋白CD34(70%),平滑肌肌动蛋白SMA(25%)、desmin(少于5%)。
(四)分期
2010年国际抗癌联盟(UICC)根据肿瘤大小、核分裂象指数和肿瘤部位对GIST进行了TNM分期(表15-6-2),存在淋巴结转移和(或)远处转移的病例均归为Ⅳ期。
表15-6-2 UICC GIST TNM分期
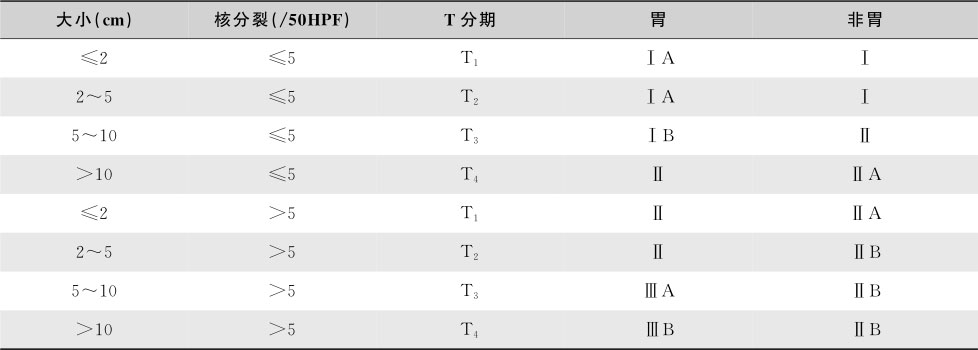
(五)病理分级
GIST的生物学行为从良性到显著恶性不等,2015年美国国家癌症网络(NCCN)根据肿瘤大小和核分裂相,对手术后的GIST进行了恶性潜能评估(表15-6-3,表15-6-4)。若肿瘤发生腹腔内破裂,则认为有高度侵袭危险性。
表15-6-3 胃GIST恶性潜能评估指南
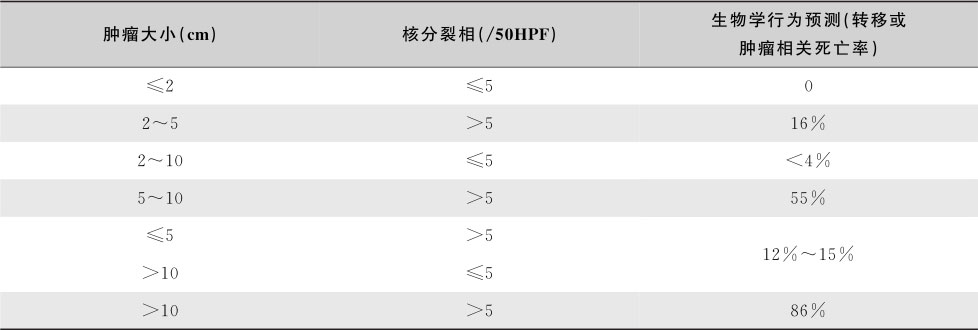
表15-6-4 小肠GIST恶性潜能评估指南
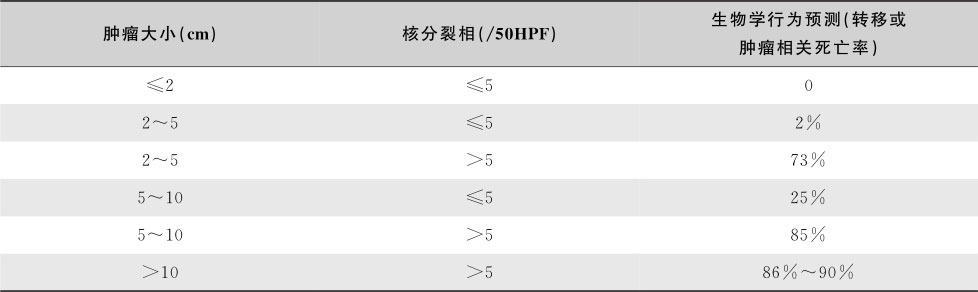
【临床表现】
随肿瘤的大小和位置不同,GIST患者可有不同的症状。出血是最常见症状。腹腔内出血可表现为严重贫血或急腹症,消化道出血则表现为呕血和黑便等。部分患者表现为肿瘤破裂、消化道梗阻或阑尾炎样疼痛等急腹症。10%~25%的患者表现为肿瘤转移的症状,有20%的患者无临床症状而由内镜、影像学或外科手术发现。
【诊断】
诊断主要依据影像学检查和病理结果,尤其是后者。
(一)影像学检查
CT可以帮助鉴别肿瘤良恶性,明确肿瘤的部位、大小及侵犯范围,但CT表现无特异性。MRI在显示肿瘤内坏死、出血、囊性变及周围脏器受累方面有一定价值。血管造影在合并出血的GIST患者中可协助明确出血部位及栓塞化疗定位。超声引导下细针穿刺对诊断GIST、获得病理有重要价值。
(二)病理诊断
GIST的病理诊断根据大体表现、组织病理学特征及免疫组化和基因检测结果综合诊断。其中,组织学符合典型GIST,CD117阳性可直接诊断;组织形态学可疑,CD117阴性的病例,需检测 DOG 1、 PDGFR-α 。对明确诊断的GIST,推荐检测 c-kit 及 PDGFR-α 突变,野生型GIST推荐进一步行 SDH 基因突变检测。
【鉴别诊断】
恶性程度低的GIST需与腺瘤、平滑肌瘤及神经鞘瘤鉴别。恶性程度高的GIST需与腺癌、淋巴瘤及神经内分泌癌、肉瘤等鉴别。除GIST特异性的病理表现外,SMA、desmin等免疫组化可协助鉴别。
【治疗】
(一)手术治疗
对于可切除的GIST,手术是最主要的治疗手段。手术目标是将包含完整假包膜的肿瘤全部切除,操作过程中尽量动作轻柔,避免肿瘤破裂。由于淋巴结转移发生率低,淋巴结清扫并不要求。
(二)药物治疗
传统的化疗对GIST无效。手术和靶向治疗是GIST的主要治疗模式。
1.甲磺酸伊马替尼
是一种酪氨酸激酶抑制剂,可选择性抑制 c-kit 、 PDGFR 、 Bcr-Abl 等酪氨酸激酶受体,从而抑制其介导的细胞行为。
对不能切除和(或)转移的恶性GIST患者,甲磺酸伊马替尼的推荐剂量为400mg/d。在治疗后未能获得满意的反应,如果没有严重的药物不良反应,剂量可考虑从400mg/d增加到600mg/d或800mg/d。甲磺酸伊马替尼应持续使用直至病情进展。
对GIST完全切除术后患者,应根据复发风险决定是否进行辅助治疗。中高危患者是辅助治疗的适应人群。中危组推荐治疗时间为1年,高危组治疗时间大于24个月。目前也有研究提示大于24个月的辅助治疗,可明显降低患者远期复发风险。
对于潜在可切除的患者,术前接受伊马替尼治疗可提高手术切除率。推荐伊马替尼应使用至最大疗效,即连续两次CT或MRI提示病灶不再缩小,可考虑手术。若疾病进展,则需考虑立即停止药物治疗,考虑手术。
2.舒尼替尼
是一个多靶点酪氨酸激酶抑制剂,可作为伊马替尼耐药GIST的二线用药。推荐剂量为37.5mg/d,持续使用,或者50mg/d,服用4周停2周。
对于伊马替尼和舒尼替尼耐药的GIST患者,可尝试使用瑞戈非尼或推荐参加临床研究。
【预后】
GIST完全切除术后3年生存率为75%,5年生存率为32%~63%。不完全切除患者5年生存率仅9%。转移性GIST患者的中位生存时间为20个月。分子靶向药物的应用,延长了患者的生存时间,复发转移的GIST患者接受伊马替尼治疗后,中位总生存时间可达到57个月。
除肿瘤大小、位置、核分裂相、肿瘤是否破裂外,GIST的预后还与基因突变类型等因素相关。其中, c-kit 基因突变伴随杂合性缺失是预后不良因素之一。 Ki- 67、 p 53、 Bcl- 2等指标也对GIST的预后有参考价值。由于GIST具有动态非定向性分化的特征,因此,即使是良性的GIST,手术切除后仍有复发可能,故所有GIST患者均应定期随访。
主要参考文献
1.中华医学会外科学分会胃肠外科学组.胃肠间质瘤规范化外科治疗专家共识.中国实用外科杂志,2015,35(06):593-598.
2.Bischof DA,Dodson R,Jimenez MC,et al.Adherence to Guidelines for Adjuvant Imatinib Therapy for GIST:A Multi-institutional Analysis.J Gastrointest Surg,2015,19(6):1022-1028.
3.Dailey DD,Ehrhart EJ,Duval DL,et al.DOG1 is a sensitive and specific immunohistochemical marker for diagnosis of canine gastrointestinal stromal tumors.J Vet Diagn Invest,2015,27(3):268-277.
第三节
胃肠胰神经内分泌肿瘤

刘 懿
神经内分泌肿瘤(neuroendocrine neoplasms,NENs)是一类起源于胚胎的神经内分泌细胞、具有神经内分泌标记物和可以产生多肽激素的肿瘤。其中,胃肠胰神经内分泌肿 瘤 (gastroenteropancreatic neuroendocrine neoplasms,GEP-NENs)原发于胃黏膜、小肠和大肠、直肠或胰腺等,常分为胰腺神经内分泌肿瘤(pancreatic neuroendocrine neoplasms,p NENs)和胃肠道神经内分泌肿瘤(gastrointestinal neuroendocrine neoplasms,GI-NENs)两部分,GEP-NENs能够产生5-羟色胺代谢产物或多肽激素,如胰高血糖素、胰岛素、胃秘素或促肾上腺皮质激素等,引起血管运动障碍、胃肠症状、心脏和肺部病变等症状,既往称为类癌综合征(carcinoid syndrome),临床上出现典型症状者少见。近年来对GEP-NENs的研究取得了一定的进展,尤其是分子标志物和辅助检查的应用,显著提高了GEP-NENs诊断的准确率。
【流行病学】
NENs近年来发病率和患病率显著上升。其中,GEPNENs约占全身NENs的55%。美国监测、流行病学与最终结果数据库(SEER)数据显示,NENs发病率的上升幅度高达500%,日本的资料表明,p NENs的年发病率为2.23/10万,中国台湾最新研究显示NENs发病率在12年间上升了5倍。GEP-NENs可发生于任何年龄,阑尾神经内分泌肿瘤的发病年龄较轻,平均30岁,其他部位的神经内分泌肿瘤发病年龄平均50岁左右。除阑尾神经内分泌肿瘤外,大部分神经内分泌肿瘤发多见于男性。90%以上的神经内分泌肿瘤发生于胃肠道,最常见发病部位为直肠和胃。
【病因与发病机制】
病因尚未阐明。GEP-NENs是一种能产生小分子多肽类或肽类激素的肿瘤,故又称小分子多肽或肽类结构瘤(amine precursor uptake and decarbo xylation tumor,APUD tumor),它除能分泌具有强烈生物活性的5-HT、胰舒血管素和组胺外,有的还可分泌其他肽类的激素,如促肾上腺皮质激素、儿茶酚胺、生长激素、甲状旁腺激素、降钙素、抗利尿素、促性腺激素、胰岛素、胰高血糖素、前列腺素、胃泌素、胃动素等物质。产生类癌综合征的主要物质是血清素和缓激肽,组胺也参与一部分作用。血清素对周围血管有直接收缩作用,对胃肠道节前迷走神经和神经节细胞有刺激作用,使胃肠道蠕动增加,分泌增多,缓激肽有强烈的扩血管作用,引起皮肤潮红。
正常情况下,食物中摄入的色氨酸仅2%左右被用作5-HT的合成,98%进入烟酸及蛋白合成的代谢途径。但在类癌综合征的患者中,60%的色氨酸被瘤细胞摄取,经羟化酶催化成5-羟色氨酸(5-HTP),再经多巴脱羟酶变成5-HT。血液中游离的5-HT大部分经肝、肺、脑等脏器的单胺氧化酶(MAO)降解成5-羟吲哚乙酸(5-HIAA)自尿中排出。前肠系统(支气管、胃、胰)神经内分泌肿瘤往往缺乏多巴脱羧酶,不能使5-HTP转变成5-HT,5-HTP就直接被释放进入血液内,因此患者血清内5-HTP水平升高,而5-HT不升高。患者尿中5-HTP及5-HT排出增加,而5-HIAA增加不明显,此即不典型类癌综合征。
【病理】
典型的GEP-NENs常为细小的黄色或灰白色黏膜下结节样肿块,单发或多发,黏膜表面多完整。形态不一,有结节状、息肉样或环状等表现。少数癌瘤表面可形成溃疡,外观酷似腺癌,常侵入肌层和浆膜层,一部分患者可有多源性神经内分泌肿瘤存在。
神经内分泌肿瘤细胞在显微镜下呈正方形,柱状,多边形或圆形。细胞核均匀一致,很少有核分裂象,细胞质内含有嗜酸颗粒。根据电子显微镜的观察,小肠类癌细胞内银染色反应阳性故为亲银性。胃神经内分泌肿瘤细胞银染色反应时必须加入外源性还原剂才呈阳性反应,故为嗜银性。直肠神经内分泌肿瘤细胞亲银和嗜银的染色反应均为阴性,故为无反应性。
GEP-NENs分类为NENs、神经内分泌癌(neuroendocrine carcinoma,NEC)和混合性腺神经内分泌癌(mixed adeno neuroendocrine carcinoma,MANEC)MANEC指含腺上皮和神经内分泌细胞两种成分的恶性肿瘤,这两种成分中的任何一种至少占30%。根据胃泌素水平及胃酸分泌情况将胃NENs分为三型:Ⅰ型最常见(70%~80%),血清胃泌素高,胃酸缺乏,病理分级属于NEN G1;Ⅱ型比较少见(5%~6%),血清胃泌素明显升高,胃酸高,伴有卓-艾综合征,病理分级属于NEN G1或G2;Ⅲ型占14%~24%,血清胃泌素正常,胃酸正常,诊断时多数已有转移,病理多属于NEC G3。
神经内分泌肿瘤的转移途径可以直接浸润生长,穿透浆膜至周围组织内,亦可发生淋巴转移或血行转移。血行转移以肝脏最为多见,亦可转移至骨、肺、脑及其他部位。
【胃肠道不同部位的神经内分泌肿瘤】
(一)食管神经内分泌肿瘤
罕见。常发生食管胃连接处,大多数为高度恶性未分化神经内分泌癌,典型神经内分泌肿瘤极罕见。肿瘤较大,直径>4cm,呈息肉蕈伞状或溃疡硬化型。进展快,预后差,诊断后平均仅存活6个月。
(二)胃神经内分泌肿瘤
亦罕见。常发生于萎缩型胃炎或恶性贫血背景上。胃神经内分泌肿瘤好发于胃底胃体部。常为多发的黏膜下小肿瘤,呈息肉样或结节状;息肉样神经内分泌肿瘤预后好。
(三)小肠神经内分泌肿瘤
相对较多见。占小肠肿瘤的13%~34%和小肠恶性肿瘤的17%~46%,尸检中小肠类癌的发生率为650/10万,明显高于临床发生率。
(四)阑尾神经内分泌肿瘤
较常见。在34 505例阑尾手术中占0.3%。多发生于中年人(中位数年龄为40岁)。阑尾的杯状细胞神经内分泌肿瘤(goblet cell carcinoid),或称腺类癌(adenocarcinoid)为白色黏液样肿物,直径<1cm,生物学行为介于典型类癌和腺癌之间,转移率15%,5年存活率80%。有的作者认为腺类癌是神经内分泌肿瘤的一种变异型。
(五)结肠直肠神经内分泌肿瘤
结肠神经内分泌肿瘤的发生率较低,但直肠却是NENs的好发部位之一,占10%~20%。
(六)胰腺神经内分泌肿瘤
常见的有胰岛素瘤和胃泌素瘤,比较罕见的包括胰高糖素瘤、生长抑素瘤、血管活性肠肽瘤等。
【临床表现】
GEP-NENs分为无功能性和有功能性肿瘤,大多数为无功能性肿瘤,临床可无症状多年,或表现为肿块所致压迫症状及肿瘤转移征象,尤其以肝转移多见,功能性GEPNENs临床可呈现特异性的综合征。
(一)GEP-NENs的局部症状
1.右下腹痛
阑尾神经内分泌肿瘤可引起管腔阻塞,故常导致阑尾炎,表现为右下腹痛。
2.肠梗阻症状
小肠神经内分泌肿瘤及其转移性肿块可引起肠梗阻,出现腹痛、腹胀、肠鸣、恶心、呕吐等症状。
3.腹部肿块
少数神经内分泌肿瘤可发生腹块,恶性神经内分泌肿瘤侵犯周围组织或转移,常出现腹块。
4.消化道出血
胃或十二指肠神经内分泌肿瘤可发生上消化道出血;肠道类癌也可有便血或隐性出血,并可引起贫血。
5.呼吸道症状
支气管神经内分泌肿瘤最常见的表现为咳嗽、咳痰、咯血、胸痛等。
6.低血糖相关症状
胰岛素瘤通常引起头痛、意识模糊、心悸、出汗、震颤相关症状。
(二)GEP-NENs的全身症状
大多数由恶性小肠神经内分泌肿瘤发生肝转移后引起,也可由支气管、胃、胰、甲状腺、卵巢等处的神经内分泌肿瘤产生。
1.皮肤潮红
63%~94%的患者可以有此症状,多发生于上半身,以面颈部为主。
2.胃肠症状
主要表现为肠蠕动亢进,可以引起发作性腹部绞痛、肠鸣,可以有发作性水样便的腹泻、里急后重感等。
3.呼吸道症状
可以发生小气管痉挛,引起发作性哮喘,见于8%~25%的患者。
4.心血管症状
见于11%~53%的病例。长期患病后可以发生心内膜下纤维化,影响瓣膜部,以右心明显。
5.神经内分泌肿瘤危象
神经内分泌肿瘤危象是类癌综合征的严重合并症。一般发生于前肠神经内分泌肿瘤及尿5-HIAA明显增高的患者(>200mg/d)。临床上表现为严重而普遍的皮肤潮红,常持续数小时至数日;腹泻可明显加重并伴有腹痛;中枢神经系统症状常见,自轻度头晕、眩晕至嗜睡和深度昏迷;常伴有心血管异常,如心动过速、心律失常、高血压或严重低血压。在危象发生时尿5-HIAA常可骤然增高。
6.其他表现
90%以上的患者有肝转移,常常有肝大的体征。部分病例在后期可以出现皮肤棕黄色色素沉着及过度角化,呈糙皮样改变,也可发生肌病及关节病。
【实验室检查】
1.血清嗜铬粒蛋白(又称铬粒素,Chromogranin,CgA)是NENs中最常用最有效的指标,在所有NENs中均有不同程度的升高,是一项很有价值的诊断和筛查指标,诊断NEN的灵敏度和特异度可达70%~90%。
2.各种肽类激素 如促胃液素等的测定主要用于功能性GI-NENs的诊断,对于出现各种临床综合征时应考虑相应激素的检测。
同时怀疑其他NENs存在的患者,尤其是促胃液素瘤的患者还应行甲状腺功能、甲状旁腺激素、血钙、降钙素、催乳素、AFP、CEA、β-人绒毛膜促性腺激素等的测定。
3.激素水平轻度升高者,必要时可行激发试验明确诊断。
(1)皮肤潮红激发试验:①将10ml乙醇加入15ml桔子汁中口服,3~5分钟后,约1/3患者出现皮肤潮红;②静脉注射去甲肾上腺素15~20μg,肾上腺素5~10μg。此两种激发试验对诊断有一定的帮助,但有心律失常、心功能不全、哮喘史慎重。
(2)用5肽胃泌素激发试验辅助类癌综合征的诊断。方法是:给患者静脉注射5肽胃泌素(0.6μg/kg,30秒内注射完毕),于注射前和注射后1、3、5、10、15分钟取血测5-HT。
4.5-HT及其代谢产物测定 血5-HT或其代谢产物尿5-HIAA的测定在类癌综合征的诊断中起关键性作用。正常人尿5-HIAA排量为2~8mg/d,>10mg/d可肯定为阳性。血5-HT 正常值为80μg/L,>130μg/L可作为阳性。
【辅助检查】
1.内镜及超声内镜
内镜检查是首选的检查措施,内镜检查结合病变部位的活检使很多类癌在早期能够被检出。超声内镜扫描不仅可用来诊断类癌,还可评估类癌的浸润深度及是否有淋巴结转移。超声内镜对胃肠道NET具有较好的诊断价值。若考虑病变位于小肠,胶囊内镜在发现隐匿的小肠NET方面具有优势,其不足之处在于胶囊内镜通常无法实现对小肠肿瘤的精确定位。
2.影像诊断
胃肠道X线造影、超声、CT、血管造影、PET等检查,有助于神经内分泌瘤的定位诊断,寻找原发灶和转移瘤,对根治和延长生存期有重要意义。CT和超声可检出10%的最大径<1cm的肿瘤,CT对最大径>3cm的肿瘤检出率为100%,MRI对于原发肿瘤的检出率仅为50%,对于转移灶的检出率为80%。对于肝转移瘤,超声的检出率为20%,CT为30%~80%。对于累及小肠的NET,腹部CT可显示肠系膜病灶、淋巴结和肝脏转移,CT小肠造影对于小肠病灶检测的敏感度和特异度分别为85%和97%。
正电子发射计算机断层扫描(positron emission computed tomography,PET)在GI-NET诊断中起重要作用。
SSRS检查是用单光子发射计算机断层成像术(singlephoton ernlssion computed tomography,SPECT)进行显像,不足之处在于当病灶体积较小(最大径<1cm)时,由于空间分辨力的不足,检出病灶的敏感度明显下降。
3.其他新型的核医学检查
在GI-NET定位诊断中具有很好的应用前景。
核素显像检查 131 I-MIBG( 131 I metaiodobenzyl guanidine)是一种放射标记的儿茶酚胺类似物,可通过钠依赖性神经元泵,被APUD细胞摄取。最早是用于嗜铬细胞瘤的诊断,也可用于胃肠及其他神经内分泌肿瘤的诊断,敏感度为55%。生长抑素受体核素显像(somatostatinreceptor scintigraphy,SSRS)是GI-NET首选的定位检查方法。
4.采取多途径的影像学检查
目前认为SSRS联合CT是评估GI-NET病变范围最敏感的方法,对治疗方案的选择至关重要。
【诊断】
神经内分泌肿瘤缺乏特殊征象,诊断颇为困难。当神经内分泌肿瘤出现类癌综合征时诊断较易。典型者表现为皮肤潮红、腹泻、腹痛、哮喘、右心瓣膜病变和肝大等。血清5-HT含量增加和尿中5-HIAA排出增多,对诊断有意义,肿瘤的组织学检查可获得确诊。
病理结果是诊断GI-NET的金标准,先行的WHO分级和TNM分期系统均依据病理结果制定,我国于2011年发布了对中国胃肠胰神经内分泌肿瘤病理学诊断共识,对病理诊断做出具体要求。在神经内分泌标志物上,突触素和CgA是必需选项,而胃泌素、血管活性肽则为可选项目。
【鉴别诊断】
1.阑尾神经内分泌肿瘤
应与阑尾炎或Crohn病作鉴别,消化道钡餐造影和5-HT、5-HIAA测定等,可作出鉴别。
2.小肠神经内分泌肿瘤
应与小肠其他肿瘤作鉴别,小肠钡餐造影、小肠镜检查和5-HT、5-HIAA测定等,可作出鉴别。
3.直肠神经内分泌肿瘤
应与直肠腺瘤或腺癌作鉴别,直肠镜检查并取活检,有确诊价值。
4.类癌综合征
应与系统性肥大细胞增多症作鉴别,后者皮肤潮红历时20~30分钟或更长,常伴有瘙痒和色素荨麻疹,骨髓涂片检查可查到组织嗜碱细胞异常增生。
【治疗】
(一)手术治疗
手术切除原发病灶是最有效的治疗方法。早期手术效果好,即使发生转移,切除大的原发病灶也能减轻和消除症状。
(二)内镜治疗
随着内镜技术的不断进步,内镜治疗占据了越来越重要的地位,其中,越来越多研究表明内镜下黏膜剥离术(endoscopic submucosa dissection,ESD)在 GINENs中治疗是安全有效的。2013年《中国胃肠胰神经内分泌肿瘤专家共识》建议对Ⅰ型胃NENs和≤1cm的十二指肠NENs行内镜治疗。
(三)一般内科治疗
包括支持对症治疗和控制相关症状:GEP-NENs的临床表现多种多样,一般治疗主要是支持对症治疗,预防各种并发症的出现。对于激素分泌导致的相关症状,如卓-艾综合征、类癌综合征或异位库欣综合征可分别使用PPI、生长抑素类似物和肾上腺阻断药(如酮康唑或美替拉酮)控制相关症状。
1.生物治疗
生物治疗主要包括干扰素(IFN)和生长抑素类似物(SSA)两类。生长抑素主要适用于分化良好、级别较低(G1/G2)和生长抑素受体(SSTR)阳性(G3)的患者;2013年《中国胃肠胰神经内分泌肿瘤专家共识》也建议将长效奥曲肽作为有功能或无功能进展期中肠NENs(G1)的一线治疗,干扰素也主要用于G1期和G2期的治疗,其中IFN-α应用最多。美国国立综合癌症网络(NCCN)指南推荐首选生长抑素类似物,进展后加用依维莫司,ENETS推荐生长缓慢者首选SSA,生长迅速者首选依维莫司,进展后用化疗或肽受体反射性核素治疗(PRRT)等。
(1)生长抑素及类似物的应用:
生长抑素具有抑制多种激素释放的功能,因而已用于多种内分泌肿瘤的治疗。人工合成的生长抑素八肽类似物奥曲肽,每日注射3次治疗类癌综合征可获较满意的疗效,可在数分钟内使皮肤潮红消退,数小时内腹泻停止。奥曲肽150μg皮下注射,每日3次。剂量过大可导致脂肪泻,长期应用有胆石生成等副作用。
奥曲肽对神经内分泌肿瘤危象亦有很好的疗效,静脉注射剂量为100μg。临床研究结果证实长效生长抑素类似物与安慰剂比较,能显著延长转移性高分化中肠NEN的无进展生存时间(14.3个月∶6.0个月),而且无论在是否有功能性肿瘤的患者中均能观察到类似的治疗反应。
(2)干扰素:
α-干扰素可抑制类癌生长,有效率达40%~50%,15%的肿瘤体积可缩小,主要不良反应为疲劳、类流感症状。
2.化学治疗
总体来说GEP-NENs对化疗的敏感度不高,尤其是高分化的肿瘤,对于有丝分裂率较低的肿瘤来说,化疗有效率通常低于30%。
(1)化疗方案的选择:
链脲霉素联合5-氟尿嘧啶(5-FU)和(或)表柔比星治疗G1/G2期的pNENs治疗已有较多证据。基于顺铂联合依托泊苷治疗小细胞肺癌(SCC)的作用,目前欧洲神经内分泌肿瘤学会(ENETS)及北美神经内分泌肿瘤学会(NANETS)均推荐顺铂联合依托泊苷治疗GEP-NEC。亦有专家基于在SCC中的研究,提出卡铂/顺铂和伊立替康/依托泊苷可互相替代用于进展期GEPNEC的治疗。
(2)肝脏介入治疗:
由于肝脏丰富的血供,其成为GINENs远处转移的主要器官之一,统计显示约40%发生转移的GI-NENs转移部位为肝脏,对于神经内分泌肿瘤肝转移瘤的肝动脉化疗和栓塞治疗展现了很有希望的前景,但单独应用肝动脉化疗或栓塞治疗中位数缓解期均不十分理想,而联合应用肝动脉化疗和栓塞,效果较好,最长存活达6年,pNENs肝转移者行该治疗后生存时间为20个月~36个月。
3.分子靶向治疗
目前主要用于G3期的治疗:针对哺乳动物雷帕霉素靶蛋白(mTOR)受体信号通路的靶向药物mTOR抑制剂依维莫司(everolimus)已经在晚期胰腺NET治疗中完成了Ⅲ期临床试验,结果证实与安慰剂比较能显著延长晚期患者的无进展生存期(11.0个月比4.6个月)。
GI-NENs肿瘤细胞都表达包括血管内皮生长因子(VEGF)及其受体、血小板衍生生长因子(PDGF)及其受体、成纤维细胞生长因子(FGF)及其受体等促血管生成因子,作用于VEGF受体、PDGF受体等多个靶点的受体酪氨酸激酶(RTK)抑制剂舒尼替尼(sunitinib)已经在晚期胰腺NEN中完成了Ⅲ期临床试验,结果证实与安慰剂比较能显著延长晚期高分化胰腺NEN的无进展生存期(11.4个月∶5.5个月)。
4.支持疗法
食物应富于营养和热量,补充蛋白质,给予足够维生素,避免可诱发皮肤潮红和腹泻的食物如牛奶制品、蛋类、柑橘等。
【预后】
取决于原发肿瘤的部位、转移的范围和程度、以及手术治疗的效果。近年来,对GEP-NENs的诊治取得了一定的进展,但由于起病隐匿,临床症状缺乏特异性,故多数确诊患者已有远处转移,治疗及预后效果不佳。
主要参考文献
1.李景南,张红杰,陈洁,等.中华医学会消化病学分会胃肠激素学组,胃肠胰神经内分泌肿瘤内科诊治若干建议,中华消化杂志,2014,34(6):361-367.
2.CSCO神经内分泌肿瘤专家委员会.中国胃肠胰神经内分泌肿瘤专家共识.临床肿瘤学杂志,2013,18(9):815-832.
3.Rindi G,Petrone G,Inzani F.25 Years of neuroendocrine neoplasms of the gastrointestinal tract.Endocr Pathol,2014,25(1):59-64.
第四节
消化道憩室病

孙剑勇 王吉耀
憩室(diverticulum)是消化道的局部囊样膨出,有真性(全层膨出)和假性(仅有黏膜和黏膜下层膨出)两种,绝大多数憩室向消化道腔外膨出,极少数向腔内膨出,称腔内憩室。多个憩室同时存在称为憩室病(diverticulosis),本病见于全消化道,以结肠最为常见,十二指肠次之,胃憩室最少见。
一、食管憩室
(一)咽-食管憩室(Zenker憩室)
国外多见,常位于下咽缩肌与环咽肌之间的左后方,由于咽食管连接区的黏膜在环状软骨近侧的咽后壁肌肉缺陷处膨出而成。多见于70岁以上者,男性约占2/3。其裂孔疝发病率明显高于正常人群。初期可无任何症状,随着憩室逐步增大,表现为轻度吞咽困难,食物反流,饭后及睡眠时易发生呛咳。晚期表现有喉返神经受压引起声嘶,饮水时有气过水声及反复发作吸入性肺炎。体检时可在锁骨上方颈根部发现面团样肿块,按压时发出气过水声。X线钡餐侧位检查有助诊断。
(二)食管中段憩室
国内多见,常位于肺门水平食管左侧,为牵拉性真性憩室。憩室直径多在1~2cm。多数无症状,部分病例出现胸骨后疼痛、胃灼热感,少数有吞咽困难,极少数发生纵隔脓肿或食管气管瘘。X线钡餐检查憩室多呈帐篷状突出,口大底小,引流通畅钡剂残留少。
(三)膈上食管憩室(食管中下段憩室)
最少见,多数患者在50岁以上。常发生在贲门食管连接处上方,食物易潴留,常伴食管痉挛、贲门痉挛、反流性食管炎或裂孔疝。诊断依赖X线钡餐检查,CT可鉴别纵隔肿瘤、脓肿。
(四)食管壁内假性憩室
多因黏膜下腺体炎症,炎症细胞浸润压迫造成腺体阻塞,扩张形成囊袋,多继发于食管痉挛、胃食管反流和念珠菌病等。憩室常有规则地分布于整个食管,很小,70%~90%存在食管狭窄。大部分患者表现为间隙性吞咽困难,伴胸骨后疼痛。
食管憩室小而无症状者一般不需治疗。一旦出现症状,宜进食清淡易消化饮食,伴有憩室炎或反流性食管炎时应予以抗生素及抑酸剂治疗。症状明显而上述方法无效或伴有并发症及癌变者宜外科治疗。手术治疗方法多采用食管憩室切除,并行彻底的肌层切开,必要时加上改良的Belsey抗反流手术。目前微创手术已开始用于食管憩室,如Zenker憩室。
二、胃 憩 室
绝大多数为单发。直径2~4cm,75%位于胃后壁贲门附近小弯侧,其次幽门区,胃体胃底部较少见。胃憩室多见于30~60岁。大多患者无症状,少数主诉饭后或平卧时有间歇性上腹部饱胀或下胸部疼痛,伴恶心、呕吐、胃灼热感。常见并发症为出血。诊断依赖X线钡餐检查和内镜检查。症状明显者经内科治疗未见改善,又不能除外恶性病变,或者发生大出血或穿孔等并发症时,需外科手术。
三、小肠憩室
(一)十二指肠憩室
是小肠憩室中最多见的。人群发生率为2%~22%。以50~60岁为多见。憩室好发于降部。66%~95%发生于十二指肠内侧,与胆总管开口处2.5cm范围内,亦称为十二指肠乳头旁憩室(peri-ampullary diverticula,PAD)。PAD可使胆石症和急慢性胰腺炎的发生率增加,称为Lemmel综合征。位于十二指肠球部的大多为假性憩室,为球部溃疡痊愈后瘢痕收缩及局部肠壁变弱所致。十二指肠憩室大多数无临床症状,仅10%患者主诉上腹胀痛不适,伴恶心嗳气,饱食后加重,并发炎症或溃疡时,症状较持久,憩室部位可有压痛。肝胰壶腹周围憩室约有27%伴发胆石症,亦可引起胆总管梗阻、胆管炎、复发性胰腺炎。其他并发症为出血与穿孔。十二指肠腔内憩室可并发十二指肠梗阻。十二指肠憩室的诊断以前主要依靠上消化道钡餐检查,近年来检测手段不断丰富,如十二指肠镜检查、ERCP、多层螺旋CT、MRCP等,ERCP是诊断十二指肠憩室的最佳方法。无症状的十二指肠憩室无须治疗,有症状者又与腹部其他疾患同存时,先治疗后者。如果症状确系憩室所致,则采用内科综合治疗,包括调节饮食,抑酸解痉,抗炎和胃肠减压等。除非有难以控制的并发症或癌变,一般不考虑手术。
(二)麦克尔憩室(Merkel diverticulum,MD)
位于回肠末端的真性憩室,系胚胎期卵黄管之回肠端闭合不全所致,男女发病率相当。典型的憩室是指状,长约0.5~13cm,距回盲瓣2~200cm,平均80~85cm。半数憩室含有异位组织,其中70%~80%为胃黏膜。大部分患者无症状。并发症包括出血、肠梗阻及憩室炎等,发生率15%~30%,男性多见,多发生于10岁前,1岁以内的占1/3。当憩室突向肠腔内时,可引起肠套叠及肠梗阻,症状为呕吐、腹胀、便秘或果酱样粪便。憩室炎是成人中常见的并发症,系憩室颈狭小、引流不畅所致。MD肿瘤的发生率为3.2%,其中33%为类癌。拟诊为急性阑尾炎者,在手术时如没有发现阑尾炎症,应探查有无MD。MD出血量与憩室内含异位组织有关,异位胃黏膜组织可通过 99m Tc(锝)扫描检查确诊,其准确率可达70%~80%。如有活动性出血,也可选用DSA检查、小肠镜、胶囊内镜等进行MD的诊断和鉴别诊断。大多数无症状的MD无须治疗,手术切除适应证为出血、梗阻、炎症或穿孔。
(三)空、回肠憩室
少见,X线钡餐发现率在1%左右。中年以上者多发,男性略多。多见于肠壁肌层脆弱的空肠上段及回肠末端。单个憩室多无症状,多发性憩室内有大量细菌繁殖时,可有消化不良症状。并发症少见,可有急性炎症、出血、穿孔、小肠梗阻和憩室内癌肿。无症状者不必治疗,凡出现严重并发症者应及时手术。急性炎症合并肠菌过度繁殖时可选用口服抗生素如环丙沙星及甲硝唑治疗。吸收不良者应对症治疗。
四、结肠憩室
是结肠肠壁肌层缺损,结肠黏膜经此处突出形成的囊性病理结构。结肠中存在多个憩室则称为结肠憩室病。
结肠憩室病是西方国家最常见疾病之一,发病率随年龄的增长而增加,60岁以上人群发病率30%以上。近年来在我国发病率也有增加。发病部位西方人群以乙状结肠及降结肠多见,而我国则多见于盲肠及升结肠。结肠多数憩室的直径为0.3~3cm不等,较大憩室少见。一般认为本病发生与经济水平和饮食习惯密切相关。经济发达的国家和高收入阶层发病率明显升高。低渣或无渣饮食者明显高于高渣或多渣饮食者。结肠过敏性炎症、习惯性便秘、肠易激惹综合征、肠道慢性梗阻及炎症性肠病人群有较高的发生率。
本病病因尚不清楚,肠腔经常处于高压状态、肠壁结构异常和缺陷、构成肠壁的结缔组织胶原成分的改变、结肠动力和肠神经的变化以及遗传因素与本病发生有关。
仅10%患者具有临床症状,表现为慢性间歇性左下腹痛,便秘伴腹部胀气及消化不良。体检时左下腹可有压痛,扪及充满粪块的乙状结肠,应与肠道易激综合征和结肠癌作鉴别。低张钡灌肠更易发现憩室。结肠镜检查可排除同时存在的其他病变,如结肠癌、结肠炎等。
一般认为,单纯性无并发症的憩室病无须治疗,有症状者则对症治疗。高纤维膳食和纤维补充剂麦麸、车前子制品或甲基纤维素等常被用来预防憩室病患者的并发症。有试验显示利福昔明合用补充膳食纤维治疗12个月可改善无并发症憩室病的症状,而给予曾发生轻度/中度憩室炎患者口服美沙拉嗪(400mg,2次/日)8周可减少4年内症状复发率,但腹痛发生率较高。
结肠憩室病并发症主要为憩室炎和出血。
(一)憩室炎
憩室炎起始于结肠壁微小穿孔导致的憩室周围炎。发生率在10%~25%,多见于左半结肠憩室。单纯性憩室炎占75%,有脓肿、梗阻、穿孔、腹膜炎、瘘管等并发症的憩室炎占25%。急性憩室炎的表现为急性左下腹痛,伴发热,下腹压痛及反跳痛,白细胞增高。左下腹部可扪及炎性腹块。部分或完全梗阻时有肠鸣音亢进,并发腹膜炎后,肠鸣音消失。直肠指检触及脓肿或炎性包块有助于定位。憩室膀胱瘘时,尿中可出现大量红白细胞。伴有结肠周围脓肿的憩室炎,结肠外表现包括关节炎和坏死性脓皮病。如既往钡剂灌肠已显示结肠憩室则有利于诊断,超声在回盲部憩室炎的鉴别诊断有重要意义,螺旋CT是首选的诊断憩室炎和并发症的方法。憩室炎急性期禁忌行全结肠镜检查。肠镜或钡剂灌肠检查应于6~8周后进行。
轻症患者的治疗包括休息、流质饮食和口服抗生素,症状缓解后逐渐过渡到软的低渣饮食,2周后作钡剂灌肠明确诊断,1个月后恢复高渣饮食。对出现严重症状或伴有其他并发症患者,80%无须手术即可获得满意治疗,如休息、禁食、静脉输液和抗生素治疗。可以静脉使用一次抗生素后,口服环丙沙星0.75g,每日2次和甲硝唑0.5g,每日4次,7~10天。形成脓肿者,可以在CT引导下穿刺排脓,6周后腹腔镜外科手术。弥漫性腹膜炎伴或伴穿孔、不能缓解的肠梗阻、结肠内脏瘘者需急诊手术。
既往有急性憩室炎的患者,应采用高纤维素饮食或摄入纤维素补充剂,避免使用非阿司匹林NASIDs。观察性研究表明体育锻炼人群中,发生憩室炎的风险度降低。
(二)憩室出血
5%~10%患者可发生出血,是老年人下消化道大出血最常见的原因之一。憩室的出血来源于动脉,常局限于单个憩室,多见于右半结肠。大量出血时可出现休克症状。缓慢间断性出血者,结肠镜检查是出血定位诊断的最佳方法,而大量出血者需行放射性核素及血管造影术,对出血部位进行判断,有助于外科限定结肠切除的适宜范围。
治疗以支持疗法包括输血为主。如果出血速度大于0.5ml/min,选择性肠系膜血管造影可显示造影剂自出血部位渗出,并可通过导管经动脉注入血管加压素或合成栓子,50%的患者可有效地止血。结肠镜下直接电凝止血常有效,无效者可考虑手术治疗。
主要参考文献
1.Stollman N,Smalley W,Hirano I,et al.American Gastroenterological Association Institute Guideline on the Management of Acute Diverticulitis.Gastroenterology,2015,149(7):1944-1949.
2.Humes DJ,Spiller RC.Chapter76.Diverticular disease of the colon.Yamada's Textbook of Gastroenterology.6th ed.John Wiley&Sons Ltd,2015,1522-1536.
第五节
胃肠道息肉及遗传性疾病

钱立平 陆玮
息肉(polyps)指黏膜面突出的一种赘生物。息肉与肠壁的连接方式、部位、范围、单发或多发、大小、形态和颜色等对判断其性质、有无恶变倾向及治疗有益。
【分类】
国内外广泛应用的是以Morson的组织学分类为基础的分类方法,该分类将息肉分成肿瘤性、错构瘤性、炎症性和增生性四类(表15-6-5)。并根据息肉有蒂与否,分为无蒂、亚蒂和有蒂息肉。根据息肉的数目分为单发和多发。
表15-6-5 息肉的分类
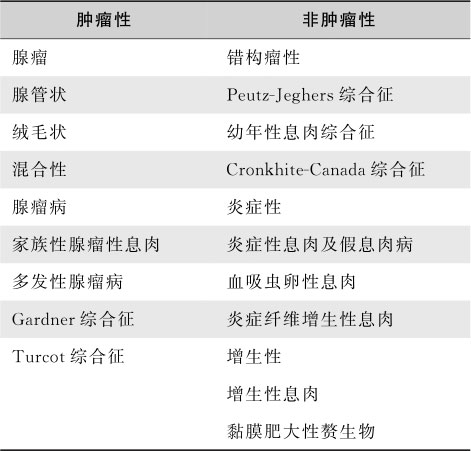
本章主要讨论腺瘤性息肉和遗传相关的胃肠道息肉综合征。
【病理】
腺瘤性息肉最常见,包括管状、绒毛状及管状绒毛状腺瘤三种。
(一)管状腺瘤
最常见,约占80%。表面呈结节状,大多有蒂,色暗红,易出血。镜下为增生的腺体组织,腺上皮排列规则,分化好,主要为管状结构,绒毛成分<20%。
(二)绒毛状腺瘤
又称乳头状腺瘤,较少见。常为单发,一般无蒂。镜下可见其表面上皮呈绒毛状增生、隆起,绒毛成分>80%,绒毛表面有柱状上皮层被覆,中间有少量间质,内含较多血管,极易出血,癌变率甚高。
(三)管状绒毛状腺瘤
兼有上述两者的表现,绒毛成分在20%~80%之间。癌变率较高。
多发性腺瘤好发于结肠,亦见于胃、小肠等整个消化道。年轻者多见,易癌变。
一、胃 息 肉
胃镜检出率2%~3%,多为增生性,单发多见,多发性恶变率较高。癌变率与组织学分型、瘤体大小有关。
早期无症状。约半数患者在钡餐造影、胃镜检查或其他原因手术时意外发现。症状以上腹部不适与隐痛最为常见。可因息肉表面糜烂或溃疡而出血。
可无阳性体征。伴出血者可有缺铁性贫血。
X线钡餐可显示充盈缺损。气钡双重低张造影可发现≥1cm的息肉。
胃镜检查可见圆形或卵圆形隆起,形状规整,表面光滑,色泽暗红。多数有蒂。直视下活检及组织学检查可了解病理类型。
可胃镜下摘除,有蒂息肉可用高频电切,无蒂息肉可采取高频电凝、激光、氩气刀、EMR治疗。一般预后良好。
二、肠道息肉
小肠息肉多见于十二指肠第三、四段,发生率远低于胃和大肠,以腺瘤和布氏腺瘤为主。以消化道出血和肠梗阻多见。恶变率27%~35%。布氏腺瘤罕有癌变。
大肠息肉约占肠道息肉80%,大多位于乙状结肠或直肠,单发多见,男性多于女性。发病率与年龄正相关。癌变率主要与组织学分型、瘤体大小及上皮异型增生有关。多无症状,少数有腹部不适、腹胀、排便习惯改变、便血或鲜血便。大的息肉可引起肠套叠、肠梗阻或严重腹泻。
诊断主要靠内镜及直视下活组织检查,但对较小的息肉有一定的漏诊率。
治疗方法同胃息肉。
三、遗传性疾病相关的胃肠道息肉综合征
本综合征是以累及结肠为主的多发性息肉病,大部分与遗传有关,伴有肠道外表现。可分为腺瘤性与错构瘤性息肉综合征两大类。
(一)腺瘤性综合征
特点是多发性腺瘤伴有结肠癌的高发率。主要有以下三种:
1.家族性腺瘤性息肉(familial adenomatous polyposis,FAP)
30%~50%的病例有APC基因突变,常染色体显性遗传,偶无家族史。发生率为万分之一。息肉分布于结肠、直肠、十二指肠和胃,多数有蒂,乳头状较少见,息肉数从一百至数千个,大小不等。其组织结构与一般腺瘤无异。多数在20~40岁时明确诊断。癌变倾向高,平均癌变年龄为40岁。
最早的症状为腹泻,可有出血、腹痛、贫血、体重减轻和肠梗阻。经结肠镜及活组织检查,并通过基因检测来确诊。
应尽早(推荐25岁前)行全结肠切除与回肠-肛管吻合术或回肠-直肠吻合术。回肠-直肠吻合术后,应每年1次直肠镜检查,如发现新的息肉可行内镜下治疗。从30岁起,有上消化道息肉者,推荐每3年进行1次胃镜检查,如果有大量息肉检查应更加频繁。大量十二指肠息肉的患者应每年行1次胃镜检查。有报道,应用低剂量选择性COX-2抑制剂可降低腺瘤性息肉的危险性。有全消化道息肉无法根治者,当出现肠套叠,大出血等并发症时可作部分肠切除术。
2.家族性多发性结肠息肉-骨瘤-软组织瘤综合征(Gardner综合征)
1958年Smith提出结肠息肉、软组织肿瘤和骨瘤三联征为Gardner综合征。常染色体显性遗传,其息肉性质和分布与FAP相似,但数目较少(一般<100),体积较大。癌变倾向亦高,但年龄稍大。骨瘤主见于头颅、上下颌、蝶骨等扁骨和四肢长骨,并有牙齿畸形。软组织肿瘤可为皮脂囊肿、平滑肌瘤、颅咽管瘤等。有甲状腺、肾上腺、十二指肠壶腹部癌变的倾向。内镜及X线检查可确定消化道息肉及骨瘤。本病结肠息肉的治疗原则与FAP相同。骨与软组织肿瘤均应手术切除,不能完全切除者,可行放疗或非激素类消炎药物治疗。
3.Turcot综合征
常染色体隐性遗传,较少见。其特征是患者有家族性腺瘤性息肉伴有其他脏器的肿瘤,通常是伴有中枢神经系统肿瘤,如脑和脊髓的胶质母细胞瘤或髓母细胞瘤,因此有胶质瘤息肉综合征之称。本病的结肠腺瘤病变与FAP相似,但多为大乳头状腺瘤,分布较稀疏,随时间推移,恶变率几乎为100%。同时合并中枢神经系统肿瘤,可并发其他部位的肿瘤,如胃、十二指肠、小肠的肿瘤,脂肪瘤等。
在恶变前本病的临床表现与FAP类似。伴发中枢神经肿瘤的症状常较突出,如头痛、头晕、恶心呕吐、视物及肢体活动障碍。诊断依赖于有家族性腺瘤性息肉史,和上述结肠及头颅病变的临床特点。结肠镜检查有助于判断结肠病变的大小、范围、有无恶变。CT、MRI有助于脑部肿瘤的诊断。
由于结肠腺瘤易恶性变,确诊后应尽早行单纯息肉切除或结肠切除术,并定期行内镜复查。中枢神经系统肿瘤可静脉化疗、伽玛刀或手术治疗,但易复发,预后差。
(二)错构瘤性综合征
包含一组疾病,其特点是某些肠段被一些组织的无规律的混合体所累及,具有非肿瘤性但有肿瘤样增生的特征。
1.黑色素斑-胃肠多发性息肉综合征(Peutz-Jeghers syndrome,PJS)
本病系伴有黏膜、皮肤色素沉着的全胃肠道多发性息肉病,40%~60%患者与LKB 1 基因突变有关。发病率约十五万分之一,可能通过单个显性多效基因遗传。外显率很高,同一家族罹病者很多(患者子女中50%发病),常在10岁前起病。
轻者无症状,严重者可有腹痛、腹泻、黏液便、便血、便秘、呕血等症状。本征有色素沉着、胃肠道息肉两大特征性表现。色素沉着多见于口唇及其四周、颊部、面部、手指皮肤,偶见于肠黏膜。色素可呈黑、棕褐、灰、蓝等。胃肠道息肉常为多发,可发生在整个胃肠道,以小肠多见。息肉大小不定,表面光滑,质硬,蒂长短、粗细不一,也可无蒂。较大息肉可呈菜花样。该病患者80%~90%有家族史,15~64岁阶段患癌的风险为93%,其中胃肠道癌约70%、乳腺癌近50%、胰腺癌11%~36%,肺、子宫、卵巢、睾丸癌亦常见。
胃肠道息肉的治疗:①较小无症状者定期随访,每隔1~2年做结肠镜检查1次;②有蒂息肉可经内镜行电凝电切,1次可摘除多个息肉;③无蒂较大息肉EMR或ESD治疗;④并发肠套叠、肠梗阻者,应行急诊手术,术中肠镜与肠切除术结合,尽可能将息肉摘除;⑤结肠、直肠内息肉较大且密集丛生无法逐个摘除者,可行全结肠切除术,保留部分直肠,行回肠直肠吻合,直肠残留息肉,可经内镜下治疗。术后终身定期癌症筛检,胃镜、小肠镜、结肠镜每2年进行1次;18岁后,每年1次胰腺CT、MRI或超声,每年1次甲状腺、子宫与卵巢或睾丸超声和体检;21岁后每半年1次乳房超声波检查或X线照相术、CA125检测。用双气囊内镜(DBE)下息肉切除术可能避免反复急诊手术和导致短肠综合征的小肠切除。
2.幼年性息肉综合征(juvenile polyposis,JP)
以多发性青少年的结直肠息肉为特征,亦见于胃和小肠。JP的发生率为FAP的十分之一,至少有2个单独的基因( SMAD 4 / DPC 4 或 BMPR 1 A / ALK 3 )突变引起,可与遗传性出血性血管扩张症共存,大部分患者的息肉呈典型的错构瘤特征,大息肉通常呈分叶状,半数不典型的JP可出现异型增生的腺瘤,引起结直肠癌的危险性增加。对JP数量较少的息肉,可通过内镜尽可能摘除被发现的所有息肉。对大量结肠息肉不能通过内镜摘除的、有症状、腺瘤样变或结肠癌家族史的患者,可考虑作全结肠切除回肠-直肠吻合术。JP危险人群,从15岁起,每1~2年应做1次全结肠镜检查,25岁起,每1~2年应做1次上消化道内镜检查,直至35岁。有相关基因改变的危险人群应监视至70岁。
3.Cronkhite-Canada综合征
1955年由Cronkhite与Canada首先报道,主要的特点有:①发病多为中老年人;②主要症状为腹泻、指(趾)甲异常、毛发脱落、色素沉着、味觉异常等;③无息肉病家族史;④胃、大肠为主的消化道息肉病;⑤病理活检示,息肉有上皮细胞覆盖,腺体增生呈囊性扩张,细胞间质水肿并可见炎性细胞浸润;⑥蛋白漏出试验异常,多有低蛋白血症。有恶变可能,病情重,预后差。治疗主要是对症处理,止泻、止痛、止血,补液,补充营养物质,保持水电解质平衡,少数患者应用皮质激素、同化激素、抗纤溶酶、抗生素和内镜下摘除局限或少量息肉可使病情得到缓解。近年来有人应用柳氮磺胺吡啶抗炎治疗。日本学者采用高能量疗法,取得一定疗效。有严重的并发症,如大量出血、脱垂、肠套叠、肠梗阻和恶变者或病变肠段较短者应手术治疗。
4.Cowden综合征
1963年Lloyd和Dennis等首先报告一种全身多脏器化生性和错构瘤性病变的疾患,并以最初被报告的患者家族之姓Cowden命名。常染色体显性遗传,病因为 PTEN 肿瘤抑制基因突变。本征以胃肠道多发性息肉伴有面部小丘疹、肢端角化病和口腔黏膜乳突样病变为特征。发病率为二十万分之一,发病年龄为13~65岁,男女之比为1∶1.5。60%患者有消化道息肉。临床表现还包括黏膜上皮病变、甲状腺异常、乳腺纤维囊性病变、早年发病的子宫肌瘤、大头畸形、智力低下以及小脑发育不良性神经节细胞瘤。合并恶性肿瘤的发生率高达40%,主要为乳腺癌、甲状腺癌、子宫内膜癌等。根据本征的特征,结合内镜检查,发现结直肠内的多发性息肉,再经病理活检证实为错构瘤病变,即可诊断。
本病胃肠道息肉可在内镜直视下,行息肉摘除术。无法内镜下摘除的可考虑手术治疗。
主要参考文献
1.Campos FG.Surgical treatment of familial adenomatous polyposis:dilemmas and current recommendations.World J Gastroenterol,2014,20(44):16620-16629.
2.Gulcin Tezcan,Berrin Tunca,Secil Ak,et al.Molecular approach to genetic and epigenetic pathogenesis of early-onset colorectal cancer.World J Gastrointest Oncol,2016,8(1):83-98.
第六节
嗜酸性粒细胞胃肠炎

刘 懿
嗜酸性粒细胞胃肠炎(eosinophilic gastroenteritis,EG)是一种少见的疾病。以胃肠道嗜酸性粒细胞浸润、胃肠道水肿增厚为特点。本病常累及胃窦和近端空肠,若累及结肠,以盲肠及升结肠多见。还可累及食管、肝脏和胆道系统,引起嗜酸性粒细胞食管炎、肝炎和胆囊炎。胃肠道外与胃肠道嗜酸性粒细胞胃肠炎合并存在的比例约50%。
【流行病学】
患者年龄跨度可从婴儿到老年人。好发年龄:30~50岁。男性发病率约为女性的2倍。
【病因和发病机制】
病因迄今未明。患者胃肠道有大量嗜酸性粒细胞浸润。有人认为与某些外源性或内源性的物质引起的机体过敏有关,但仅20%~50%的患者既往有过敏史。澳大利亚学者曾报告其发病与钩虫感染有关,但使用甲苯达唑治疗未见疗效。
20%~80%患者外周血中嗜酸性粒细胞和免疫球蛋白IgE升高。造成消化道损伤最重要的因素是嗜酸性粒细胞的浸润及脱颗粒作用。活化的T细胞产生IL-5,它具有强大的嗜酸性粒细胞趋化和脱颗粒功能。患者的胃肠道活检标本中发现嗜酸性粒细胞脱颗粒及有主要基础蛋白(major basic protein,MBP)沉积,而 MBP对许多细胞和组织均有毒性作用,因此,人们认为嗜酸性粒细胞脱颗粒,MBP沉积在本病发病中有重要作用。由于息斯敏和酮替芬对本病的治疗有一定疗效,有人推测,肥大细胞的脱颗粒与嗜酸细胞性胃肠炎发病也有关系。最新研究表明,淋巴细胞衍生的嗜酸性粒细胞趋化因子对于调节嗜酸性粒细胞聚集于胃和小肠起到重要作用。
【临床表现】
本病缺乏特异性表现,可因胃流出道梗阻而急性起病,也可表现为腹痛或不适(100%)、恶心(67%)、呕吐(33%)、肠梗阻(50%)、腹水等慢性症状,如累及肝胆系统,则可出现黄疸。有些患者的症状可持续多年。所累及的部位和浸润深度的不同决定了临床表现的差异性,80%的患者有长期反复发作病史。儿童及青少年表现为:生长发育迟缓,青春期延迟,闭经等;成人主要表现为腹痛、腹泻、吞咽困难、体重降低,严重者表现为急性消化道梗阻或穿孔。
(一)按部位分类
1.局限性
多见于中老年,病变仅累及胃,约占嗜酸性粒细胞胃肠炎的26%,此型又称为嗜酸性粒细胞性胃炎(eosinophilic gastritis)。胃窦部最常见,主要表现为上腹部的痉挛性疼痛、恶心呕吐等;胃内的肿块可以导致恶变或胃流出道梗阻。
2.弥漫性
多见于中青年,主要表现为上腹部痉挛性疼痛、恶心呕吐,发作有规律,可能与进食某些食物有关,约50%患者可出现肠梗阻表现。
(二)按浸润程度分类
Klein分型是目前常用的分类方法。
1.黏膜型
病变主要累及胃肠黏膜。患者可有过敏性病史及较高的血IgE浓度及血清白蛋白降低,其临床表现为胃肠道蛋白丢失、贫血、吸收不良、体重下降及腹泻等。
2.肌层型
此型病变主要累及肌层,其临床表现为梗阻,这种梗阻有时需要手术治疗。另外,还偶有胃肠道出血和瘘管形成。
3.浆膜型
此型病变主要累及浆膜层,其临床表现为腹痛、腹膜炎、腹水和腺体病,其中腹水较常见,对激素治疗反应较好,文献报道本型还可合并胆管炎、胰腺炎、嗜酸性脾炎、急性阑尾炎、巨大十二指肠溃疡等。
【辅助检查】
(一)血常规
血嗜酸性粒细胞计数升高,且可随疾病病程波动,但有1/3的患者嗜酸性粒细胞计数始终正常。因此,周围嗜酸性粒细胞增多并非是诊断的必要条件,无嗜酸粒性细胞增多不能除外的可能。
(二)粪便
检查可有大便隐血阳性,可以通过收集24小时的粪便检测α抗胰蛋白酶判断消化道中蛋白的丢失情况,从而分析胃肠道的消化和吸收功能,正常值为:0~54mg/dl;嗜酸性粒细胞胃肠炎患者该值往往会升高,部分患者有轻至中度脂肪泻。
(三)腹水检查
可见大量嗜酸性粒细胞。
(四)放射学检查
胃肠道钡餐造影可见胃窦部僵硬、黏膜皱壁增厚和黏膜结节样增生;小肠环状皱襞及增厚,但不伴溃疡和局部异常;有些患者可无特殊发现。CT检查可见胃肠壁增厚、肠系膜淋巴结肿大或腹水。放射学检查结果的特异性较差,其诊断价值远不如内镜检查。
(五)放射性核素
99m Tc标记白细胞行放射性核素扫描检查可以评估疾病累及的广泛性,并且对治疗的反应性,但对于协助诊断来说并没有太大的意义。
(六)内镜检查加活检
内镜检查可见受累黏膜充血水肿、糜烂、出血、增厚或有肿块。活检病理可见受累胃肠道黏膜有局灶或弥漫性嗜酸性粒细胞浸润,组织水肿及纤维化;黏膜活检病理嗜酸性粒细胞食管>15/HPF、胃、十二指肠及回肠>20~30/HPF,结肠>20~50/HPF,支持嗜酸细胞性胃肠炎诊断,高度怀疑肌层型或浆膜型者,超声内镜有助于诊断。
【诊断和鉴别诊断】
(一)诊断
嗜酸细胞性胃肠炎主要根据临床表现、血常规、放射学和内镜加活检病理检查的结果作出。常用有两种诊断标准。
1.Talley提出的标准:
①存在胃肠道症状;②活检病理显示从食管到结肠的胃肠道有一个或一个以上部位的嗜酸性粒细胞浸润,或有放射学结肠异常伴周围嗜酸性粒细胞增多;③除外寄生虫感染和胃肠道外以嗜酸性粒细胞增多的疾病,如结缔组织病、嗜酸性粒细胞增多症、Crohn病、淋巴瘤、原发性淀粉样变性、Ménétrier巨大肥厚性胃炎、淋巴瘤等。
2.Leinbach提出的诊断标准:
①进食特殊食物后出现胃肠道症状和体征;②外周血嗜酸性粒细胞增多;③组织学证明胃肠道有嗜酸性粒细胞增多或浸润。
(二)鉴别诊断
1.消化不良
嗜酸细胞性胃肠炎患者可有腹痛、恶心、呕吐、腹胀等消化不良症状,但常缺乏特异性。对于以消化不良为表现的患者要与消化性溃疡、反流性食管炎、胃癌、慢性胰腺炎等注意鉴别。
2.肠道寄生虫感染
周围血嗜酸性粒细胞增多可见于钩虫、蛔虫、旋毛虫、华支睾吸虫、包虫等所致的寄生虫病,各有其临床表现,外周血嗜酸性粒细胞绝对值明显升高;通过反复检查粪便卵不难鉴别。
3.肠梗阻
肌层型嗜酸细胞性胃肠炎,常发生肠梗阻,要注意除外胃肠道肿瘤、肠道血管性疾病等。
4.嗜酸性肉芽肿
主要发生于胃和大肠、小肠,呈局限性肿块,病理组织检查为嗜酸性粒细胞混于结缔组织基质中,病理学特点为黏膜下层的结节或息肉内有不同程度的嗜酸性粒细胞浸润。
5.腹水
多见于浆膜型嗜酸细胞性胃肠炎。腹水常规和生化检查、腹水CEA检测、腹水病理检查有助于疾病的诊断。
6.嗜酸性粒细胞性增多症(HES)
是一种病因未明的全身性疾病,可以累及胃肠道。Hardy和Anderson提出的HES的诊断标准为:①外周血嗜酸性粒细胞计数≥1.5×10 9 /L、持续6个月以上且不能用其他疾病解释;②有HES的临床表现,如血管性水肿、心脏和肺部表现或胃肠道症状。但HES和EG有时很难鉴别,HES可累及肝脏(60%),累及胃肠道(14%),弥漫性嗜酸细胞性胃肠炎也可累及胃肠道外的器官(50%)。因此有学者认为,弥漫性嗜酸细胞性胃肠炎有可能是以胃肠道表现为主的HES。
【治疗】
(一)饮食
应尽量避免引起胃肠过敏的食物。
(二)药物治疗
1.糖皮质激素
嗜酸细胞性胃肠炎对糖皮质激素的治疗反应良好,泼尼松,初始剂量15~40mg/d,连续1~2周1个疗程,治疗2个月后逐渐减量。糖皮质激素治疗缓解率可达90%,停用糖皮质激素后,文献报道有1/3的患者可复发,复发病例应用糖皮质激素治疗仍然有效。此外,还可使用吸入性的氟替卡松、泼尼松或同等剂量的其他类型激素、布地奈德。
2.色甘酸钠
可稳定肥大细胞膜,抑制其脱颗粒反应及NADPH氧化酶的活化,防止组胺、慢反应物质和缓激肽等介质的释放而发挥抗过敏作用。用法40~60mg每日3次。对糖皮质激素治疗无效或副作用较为严重者可改用色甘酸钠治疗。
3.抗过敏药物
息斯敏10mg qd~bid;酮替芬1mg~2mg qd~bid。
(三)手术治疗
嗜酸细胞性胃肠炎的手术治疗适用于有梗阻的患者,但远期效果不佳,如不使用糖皮质激素,即使作胃肠道局部切除,仍有可能复发。
【预后】
本病是一种变态反应性疾病,虽可反复发作,但长期随访未见恶变,如能及时治疗,预后良好。
主要参考文献
1.Masterson JC,Furuta GT,Lee JJ.Update on clinical and immunological features of eosinophilic gastrointestinal diseases.Curr Opin Gastroenterol,2011,27(6):515-522.
2.Furuta GT,Atkins FD,Lee NA,Lee JJ,et al.Changing Roles of Eosinophils in Health and Disease.Ann Allergy Asthma Immunol,2014,113(1):3-8.
第七节
肠道微生态和消化系统疾病

戎兰 刘厚钰
肠道微生态指在机体消化道中存在的细菌、病毒、真菌、衣原体等微小生物群体,以细菌为主。肠道内细菌总数约10 13 ~10 14 ,有400~500多菌种,近200万个基因,是机体中细胞数量最多的独特组织器官。
【肠道菌群构成】
(一)菌群演变
人体肠道菌群是一个动态变化的复杂过程,胎儿在子宫内时肠腔处于相对无菌状态,出生后由于与外界环境接触,数小时肠腔内即出现细菌定植,以双歧杆菌(Bifidobacterium)为主,具有高度不稳定性。剖宫产手术的新生儿因分娩时未接触母体微生物,肠道双歧杆菌总数明显低于阴道分娩者。随着幼儿饮食结构的变化,肠道内拟杆菌(Bacteroides)、厌氧链球菌(Streptococcus)等菌群逐步增多,双歧杆菌逐步减少。经过1~2年不断调整,逐渐形成稳定肠道微生态。菌群的建立与机体远期健康有密切相关性,分娩和喂养方式(母乳或配方乳品)、生活环境(包括抗生素使用)均影响婴儿期肠道菌群的稳定。菌群存在个体差异性,但有血缘关系且独自生活个体间肠道菌群较相似,表明宿主基因也影响肠微生态定植。健康成人一生中胃肠道菌群保持相对衡定,具有“指纹样“的独特性。进入老年后,菌群多样性降低,稳定性下降。拟杆菌和厚壁菌(Firmicutes)比率改变,双歧杆菌明显减少,梭菌(Clostridium)增高,导致持续性肠道“炎性衰老”。长寿地区老年人肠道内富含乳酸杆菌(Lactobacillus)和双歧杆菌。
(二)菌群分类
原籍菌是肠道优势菌群,为专性厌氧菌,定植在肠道黏膜表面的深部,宿主健康有益的细菌,低免疫原性,如拟杆菌、双歧杆菌、乳酸杆菌等;共生菌,为肠道非优势菌群,与原籍菌有共生关系,与外籍菌有拮抗关系,一般无传染性,如消化链球菌(Peptostreptococcus)、芽孢菌属(Bacillus)等;外籍菌大多数是病原菌,在肠腔表层可以游动的菌群,如大肠埃希菌(Escherichia coli)、肠球菌(Enterococcus)等需氧菌或兼性厌氧菌,具有高度免疫原性,长期定植的机会少。多数肠道菌群可分为:革兰阳性厚壁菌门、放线菌门(Actinomycetes),革兰阴性拟杆菌门、变形菌门(Proteobacteria),其中厚壁菌门和拟杆菌门占90%以上。
(三)菌群分布
细菌经口进入机体,首先遇到胃酸屏障,胃液有杀菌能力,进食时胃内细菌数可升高至10 4 /ml。由于小肠液量大,包含胆汁酸、消化酶和氧气等,对细菌有杀菌作用,因此小肠内细菌数相对较少。随着空肠至回肠蠕动速度的减慢,细菌数和种类随着pH梯度上升开始变化,空肠细菌浓度10 3 ~10 5 /ml,以革兰阳性需氧菌为主,回肠渐上升达10 5 ~10 7 /ml,革兰阴性菌群开始超过革兰阳性菌。过回盲瓣后,细菌浓度升高达10 10 ~10 12 /ml,98%为厌氧菌,主要为原籍菌,而潜在致病菌如梭菌和葡萄球菌(Staphylococcus)浓度较低。
(四)菌群调节
任何精神上或外界环境的变化均可引起肠道微环境的紊乱,通常机体经过自身的代偿,排泄过多异常的菌群,恢复稳定的菌群状态。若机体无法自身纠正时,某些条件致病外籍菌可以致病,次为共生菌,极少数为原籍菌。因此正常菌群和致病菌群没有严格界限,可以相互转化。
【菌群功能】
肠道菌群的定植促进肠道屏障功能建立,免疫系统的发育及机体营养代谢形成,从而达到相互依赖,和谐共生的整体。
(一)屏障功能
肠腔内菌群与肠黏膜紧密结合构成肠道生物屏障,将致病菌和毒素局限于肠腔内,避免机体炎症。参与肠上皮细胞分化增殖、隐窝结构形成及局部血管生成。多数原籍菌在营养争夺中占绝对优势,限制致病菌黏附及繁殖。菌群代谢发酵产生大量短链脂肪酸(SCFAs),为肠黏膜上皮细胞提供能量。
(二)免疫调节
肠黏膜相关淋巴组织占人体内70%的免疫细胞,由派伊尔结(peyer's patches,PP)、固有层和上皮内淋巴细胞组成。菌群刺激肠道淋巴组织发育。无菌动物的肠道淋巴组织发育受限,菌群刺激后PP内B细胞发育成熟,促进分泌免疫球蛋白IgA(sIgA),增强肠黏膜的屏障,阻止致病性菌群在黏膜表面附着。菌群刺激肠黏膜免疫细胞Toll样受体,启动先天性免疫应答,增强肠黏膜淋巴组织抵御致病菌的入侵能力。菌群参与T淋巴细胞增殖分化和辅助型T淋巴细胞的分型(Thl、Th2、Th17、Treg细胞),调节T淋巴细胞对非致病性抗原物质如食物应答,形成免疫耐受。
(三)代谢和营养
通过优势生长竞争性地消耗致病菌的营养素,将肠腔内不消化多糖,如低聚糖、非淀粉多糖、抗性淀粉等进行发酵降解为SCFAs,促进肠上皮细胞生长和分化,促进调节性T细胞分化。肠道菌群参与肠道胆盐的吸收,从而影响肝脏内胆固醇代谢。参与多种维生素和微量元素合成吸收,维生素K主要来源于大肠埃希菌的合成。参与一些药物和毒物的代谢,如柳氮磺胺吡啶经肠道菌群代谢释放出5-氨基水杨酸起治疗作用。
【菌群失调】
菌群失调使肠道内致病菌增多,黏膜上皮细胞能量代谢异常,通透性增高,肠道细菌及其毒素易位,进入肠肝循环,进一步损伤肠道肠黏膜屏障,诱发肠道异常免疫反应,表现为肠免疫系统对变化的肠道菌群不能耐受,导致持续肠黏膜和全身慢性炎症。
【微生态制剂】
补充外源性有益菌,有利于促进正常菌群的生长,抑制致病菌或条件致病菌的生长,调整微生态失衡。
微生态制剂主要有三类:益生菌(probiotics)、益生元(prebiotics)及合生元(synbiotics)。益生菌指对宿主有利无害的活菌群和(或)死菌,可以是单一菌株制成,也可以是多种菌的复合制剂。益生菌具有菌株特异性和剂量依赖性。菌株不同来源分离的同一种、同一亚种,即该菌的不同菌株,如青春型双歧杆菌、长双歧杆菌。主要的益生菌包括双歧杆菌、乳酸杆菌和嗜热链球菌、芽孢杆菌、酵母菌(saccharomycetes)等制品。益生元指一类非消化的物质,可被结肠内正常细菌分解和利用,选择性地刺激结肠内有益菌生长,改善肠道功能,它包括果糖、乳果糖、异麦芽糖和纤维素、果胶及一些中草药等,双歧因子是最早发现的益生元。合生元是益生菌与益生元合并的一类制剂,所添加的益生元能促进制剂中益生菌生长,又促进宿主肠道中原籍菌的生长与增殖。
【肠道菌群和疾病】
(一)胃肠疾病
1.腹泻
饮食不当、环境变化等因素使肠道菌群紊乱,致病菌进入机体内,导致急性腹泻。益生菌通过维护肠上皮细胞功能,抵制致病菌的侵入;另一方面促进sIgA分泌;降解多糖产生SCFAs,刺激水钠吸收。对于病毒性腹泻早期口服益生菌,可缩短病程目前报道鼠李糖乳杆菌、罗伊乳杆菌、嗜酸乳杆菌、保加利亚乳杆菌、嗜热链球菌、布拉酵母菌(borlardii yeasts)等菌株对急性感染性腹泻有确切效果,特别是病毒性水样泻。其疗效存在菌株和剂量依赖性,但对腹泻无预防作用。旅行者腹泻症状轻微,具有自限性。益生菌对旅游者腹泻有良好的预防和治疗作用。长期使用广谱抗生素或免疫能力极度低下者,肠道易菌群失调,使某些耐药的难辨梭状芽胞杆菌大量繁殖,导致抗生素相关腹泻,严重者为假膜性肠炎,产生的毒素引起严重腹泻及结肠炎症(本篇第六章九节“假膜性肠炎”)。甲硝唑、万古霉素等抗生素为常用治疗药物,但停药后肠炎容易复发。万古霉素联合益生菌,如布拉酵母菌治疗,复发率较单用万古霉素明显降低。布拉酵母菌目前已证实对假膜性肠炎具有治疗和预防作用。
2.肠易激综合征
发现患者肠道内厚壁菌对拟杆菌的比例增加,菌群多样性减少。部分腹泻或便秘型患者使用抗生素治疗有明显疗效,提示IBS可能存在着菌群紊乱及病原菌异常繁殖的两种可能性。紊乱菌群通过细菌发酵产物,增高内脏的敏感性,降低疼痛阈值,产生腹痛或腹部不适的症状;紊乱代谢产物,如高浓度的SCFAs和甲烷影响肠道固有神经或结肠平滑肌、结回肠反射等,影响肠道动力,导致腹泻和便秘的症状。菌群失调引起肠道黏膜持续低度炎症,刺激结肠黏膜内肥大细胞的增加,引起腹痛。益生菌能改善部分肠易激综合征症状,如腹胀、腹痛等。不同益生菌疗效有不一致报道。
3.功能性便秘
胃肠运动减慢导致肠道菌群繁殖,代谢产生的抑制性神经递质,如一氧化氮等,加重便秘症状,肠道菌群可反作用于脑-肠轴,影响5-羟色胺(5-HT)分泌降低,抑制肠蠕动。益生菌,如双歧杆菌促进5-HT分泌,使肠腔内pH下降,中和肠道内毒素,减少水分吸收,缓解便秘症状。
4.新生儿坏死性小肠结肠炎
肠道定植菌群对免疫耐受机制的影响是疾病的病理基础之一。部分新生儿、早产儿或极低出生体重者肠屏障功能不成熟或肠道缺血、喂养不当等,诱发致病菌过度繁殖所致。预防和治疗首选双歧杆菌,此外粪链球菌、枯草杆菌和布拉地酵母菌等对降低疾病严重程度和病死率有相关效果,但对应用安全性和有效剂量的文献报道不多。
5.肠道细菌过度生长综合征
小肠内细菌较少,若小肠上段pH梯度上升,肠道运动减弱时,小肠下段及结肠的致病菌如葡萄球菌、梭菌等出现上移,造成小肠细菌过度生长(small intestinal bacterial overgrowth,SIBO)。SIBO使结合胆酸分解为游离胆酸,影响脂肪的吸收;竞争性摄取营养物质,造成巨幼红细胞性贫血和骨质软化等疾病;代谢产气引发腹胀、腹痛等症状。小肠黏膜持续慢性炎症促进老年性疾病加速进展,如动脉粥样硬化、2型糖尿病等。
6.炎症性肠病
肠黏膜对肠腔内菌群和食物均处于“可控”的炎症反应范围内,当肠腔内菌群紊乱后,引起异常免疫应答。NOD-2基因突变是克罗恩病确切易感基因,即细胞质模式识别受体(NOD2)的表达变异,对潘氏细胞分泌抗菌肽减少,针对肠道菌群的NF-κB活性减少,抗菌免疫力降低。细菌最多的地方常为炎症最容易发生的部位,如回盲部、手术后储袋等。遗传易感者,肠道菌群异常定植是IBD发病的重要线索。IBD者肠道内菌群种类降低30%~50%,厚壁菌门和拟杆菌门数量减少,变形杆菌门和放线菌门数量的增加。
部分益生菌制剂(VSL#3,即干酪乳杆菌、植物乳杆菌、保加利亚乳杆菌、嗜热链球菌、长双歧杆菌、短双歧杆菌、嗜酸乳杆菌、婴儿双歧杆菌等不同革兰阳性细菌组成的混合菌群)可治疗轻或中度溃疡性结肠炎并维持缓解,对克罗恩病尚无确切治疗作用;益生菌能预防抗生素诱导缓解的储袋炎。多菌种、大剂量益生菌疗效可能更为突出。
7.幽门螺旋杆菌防治
体外实验发现多种益生菌可抑制Hp感染菌株的生长繁殖,乳杆菌的硫酸脑苷脂结合蛋白能与Hp竞争结合Hp糖脂受体分子,有助于机体抑制Hp的定植。Hp根治过程中大量抗生素应用后肠道内双歧杆菌数量明显减少,大肠埃希菌和克雷伯杆菌(Klebsiella)数量增加,近半数患者可发生抗生素相关性腹泻,益生菌减少药物的相关性不良反应,如腹泻、味觉障碍等,提高治疗的耐受性。
(二)内毒素血症
肠黏膜屏障有助于将细菌的内毒素局限于肠腔内。重大应激、败血症、缺血再灌注、长期禁食等因素使肠黏膜上皮细胞萎缩、凋亡,屏障功能障碍,细菌及内毒素可从肠道进入肠系膜淋巴结、腹腔外脏器(肝、脾、肾等)和血液,造成内源性感染。肠内细菌向肠外组织迁移现象,称为细菌移位。
1.慢性肝病
肠道动力障碍,胆汁分泌受损,肠道去垢作用削弱,增加了致病菌黏附和生长的机会;胃肠道淤血,肠黏膜通透性增加;抗生素的经常使用加重肠道菌群紊乱,可导致高内毒素血症,诱发自发性细菌性腹膜炎、肝性脑病、肝肾综合征和肝肺综合征等并发症。补充双歧杆菌等益生菌或乳果糖益生元后,血浆和粪便氨水平降低,内毒素血症减轻,有利于缓解疾病。
2.急性胰腺炎
长期禁食引发细菌移位是系统性炎症反应综合征及多脏器功能衰竭的因素之一。早期鼻饲伴有益生菌的肠内营养促进肠道内菌群的平衡和维持有效的肠黏膜免疫状态,减少肠源性感染,缩短住院时间。
(三)代谢性疾病
肠道菌群是导致体重增加及能量代谢异常的环境因素,高脂饮食致肠腔内拟杆菌门含量降低及厚壁菌门升高。于肥胖者低脂饮食1年后,体重下降同时肠道菌群发生逆转。菌群紊乱,肥胖者更易从食物中提取能量生成脂肪。治疗肥胖的胃旁路手术后也发现类似的菌群改变。菌群变化降低黏膜通透性,促进脂多糖与Toll-4受体结合,脂肪组织炎症细胞浸润,血清内炎症因子表达,引发一种低度炎症反应,最终引起肥胖、胰岛素抵抗、高脂血症及高血压等代谢紊乱性疾病。予肥胖人群益生菌VSL#3后,显著增加粪便中双歧杆菌和乳酸杆菌以及总厌氧菌和需氧菌的数量,能改善血脂谱,降低炎症因子。
(四)肿瘤
肠肿瘤者肠道内有害菌拟杆菌、肠球菌、大肠埃希菌、肺炎克雷伯菌、链球菌以及消化链球菌比健康对照增多,而共生菌则减少。由于肿瘤的发生发展是一个漫长的过程,菌群变化与肿瘤目前仍有大量疑问未解决。目前研究最多的促癌细菌为梭杆菌和肠杆菌,梭杆菌具有侵袭性、黏附性和致炎性的革兰阴性厌氧菌,肿瘤局部炎症因子水平与梭杆菌数量呈正相关;大肠埃希菌的毒力因子Colibactin能破坏细胞DNA双链结构,导致染色体不稳定的遗传性。益生菌定植,竞争性排除有害菌、降低致病性脱氧胆酸和石胆酸的累积触发的氧化损伤;益生菌发挥SCFAs的化学预防作用、促进结肠上皮细胞生长分化,刺激胃肠激素生成,控制原癌基因的表达,抑制酪氨酸激酶信号途径,发挥抗增殖效应。
(五)变态反应性疾病
发病率逐年增高,食品过敏临床表现多样,可累及胃肠、呼吸道和皮肤等脏器。过敏性婴儿肠道内乳酸杆菌、双歧杆菌和拟杆菌属较非过敏性婴儿明显降低。婴儿期菌群紊乱致肠道免疫系统的成熟不平衡,肠黏膜通透性增加,食物蛋白抗原穿过肠黏膜引发“过敏”。肠道菌群早期建立诱导和维持口服免疫耐受,预防变态反应性疾病。多项研究显示在孕期和出生后对于有过敏遗传背景婴儿提供益生菌或坚持母乳喂养,能降低变应性皮炎的发生率。
(六)神经系统
婴儿期接触的微生物参与调节机体对压力的适应能力及情感疾病的易感性,影响应激反应时下丘脑-垂体-肾上腺轴的活性病。脑-肠双向作用紊乱与功能性胃肠病、肥胖、自闭症、阿尔茨海默病、帕金森病、焦虑和情绪低落有关。儿童自闭症者常伴腹痛、腹胀、便秘和腹泻等肠道症状,体内乳酸菌含量明显下降,梭状芽胞杆菌含量上升。
(七)其他
可能参与了慢性疲劳综合征、慢性肝炎、酒精性肝病、骨质疏松症、风湿性关节炎、湿疹、哮喘、终末期肾病和衰老等疾病的发病。
【粪菌移植】
粪菌移植(fecal microbiota transplantation,FMT)是将健康人粪便中的功能菌群分离后移植到菌群紊乱患者胃肠道内,重建健康的肠道菌群。目前对治疗CDI、炎症性肠病、肠易激综合征有肯定疗效,对代谢性疾病、疲劳综合征、肠道免疫缺陷、帕金森病和儿童自闭症等也具有一定作用。由于难辨梭状芽孢杆菌易产生多重耐药,常规治疗经常复发,2013年美国已将FMT列入治疗复发性CDI临床指南中。但是FMT治疗中,供体治疗前和受体治疗前后肠道菌群缺乏观测,因此如何保证供体的健康性,理想的移植方法,技术标准化、安全性评估等方面尚待深入研究。
【安全性及不良反应】
益生菌药物有效性具有菌株特异性和剂量依赖性特点,选择药物应个体化。即某一菌株的治疗作用并不代表其属或种的益生菌均具有这一作用。不同菌株发挥作用所需剂量不同,同一菌株针对不同疾病所需剂量也不相同。
抗生素类药物影响益生菌在肠道的定植,通常间隔2~3小时。静注抗生素药时,慎用胆汁中排泄浓度较高的药物,防止影响肠道菌群。使用抗生素与活菌制剂的功效及活菌制剂中是否会有耐药因子传递给机体中其他细菌,造成耐药因子扩散均为必须考虑的问题。对于免疫抑制人群服用益生菌,仍然需要慎重。
主要参考文献
1.Human Microbiome Project Consortium.Structure,function and diversity of the healthy human microbiome.Nature,2012,486(7402):207-214.
2.Marchesi JR,Adams DH,Fava F,et al.The gut microbiota and host health:a new clinical frontier.Gut,2016,65(2):330-339.
第八节
急性出血性坏死性肠炎

孙剑勇
急性出血性坏死性肠炎(acute hemorrhagic necrotizing enteritis,AHNE)是以小肠广泛出血、坏死为特征的肠道急性蜂窝织炎,病变主要累及空肠和回肠,偶尔侵犯十二指肠和结肠,甚至累及全消化道。主要临床表现为腹痛、便血、发热、呕吐和腹胀。严重者可有休克、肠麻痹等中毒症状和肠穿孔等并发症,为临床上较常见的急性暴发性疾病。
【流行病学、病因和发病机制】
本病全年皆可发生,多见于夏秋季。儿童和青少年多见。男性多于女性,农村多于城市。确切病因尚不清楚,目前认为与C型产气荚膜杆菌(即产β毒素的Welchii杆菌)感染有关,它能干扰肠黏膜表面绒毛的正常功能,从而影响肠道的清洗作用,使肠道组织坏死。在长期营养不良、糖尿病或机体抵抗力下降个体中,当进食受C型产气荚膜芽胞杆菌污染或已经变质的食物时,由于胰液和蛋白水解酶减少,不能分解β毒素而致病。本病的发生还有其他饮食因素,如从多吃蔬菜转变为多吃肉食,肠道微生态环境改变,有利于C型产气荚膜芽胞杆菌的繁殖;或以甘薯为主的饮食,肠内大量存在胰蛋白酶抑制因子,β毒素破坏减少。变态反应、钩蛔虫感染亦参与本病的发病。
【病理】
主要病理改变为肠壁小动脉内类纤维蛋白沉着、栓塞而致小肠出血和坏死。病变部位以空肠及回肠为多见且严重;少数病例全胃肠道均可受累。病变呈节段性。常起始于黏膜,肿胀、广泛性出血,皱襞顶端被覆污绿色假膜,与正常黏膜分界清楚。病变可延伸至黏膜肌层,浆膜层。病变肠壁明显增厚、变硬、严重者可致肠溃疡和肠穿孔。镜下可见病变黏膜呈深浅不一的坏死改变。肠绒毛充血和变粗,多核及单核细胞浸润;黏膜下层广泛出血,炎症细胞浸润。肌层及浆膜层可有轻微出血。血管壁呈纤维素样坏死,可有血栓形成。肠系膜局部淋巴结肿大。
【临床表现】
起病急,发病前多有不洁饮食,如摄入变质肉类、腐烂水果、生甘薯等,或暴饮暴食。受冷、劳累、肠道蛔虫感染及营养不良为诱发因素。
(一)腹痛
既是首发症状又是主要症状。突然出现,多在脐周或中上腹阵发性绞痛,后逐渐转为全腹或右下腹持续性剧痛,阵发性加剧。一般在1~3天后加重,重者可产生腹膜刺激症状,在血便消失后减轻。
(二)腹泻、便血
粪便初为糊状而带粪质,其后渐为黄水样,一般每天腹泻2~8次,也有10次以上,无明显里急后重感。少数腹泻严重者可出现脱水和代谢性酸中毒等。约12~72小时后可出现血便。便血是本病特征之一,发生率可达67%~80%。出血量少者粪便呈棕褐色,稍多者呈洗肉水样,赤豆汤样,甚至可呈鲜血状或暗红色血块。严重者一天出血量多达数百毫升。粪便无黏液和脓液,有特殊的腥臭味。
(三)恶心、呕吐
常与腹痛、腹泻同时发生。呕吐物可为黄水样、咖啡样或血水样,亦可呕吐胆汁。
(四)全身症状及中毒症状
发热一般在38~39℃,少数可达41~42℃,多于4~7天渐退,而持续2周以上者少见。重症病例起病后1~2天腹痛、呕吐加剧,大量血便,高热抽搐,部分病例出现休克;或表现为明显腹胀,麻痹性肠梗阻。
(五)腹部体征
相对较少。体检可有腹部膨隆,可见肠型。脐周和上腹部,甚至全腹,可有明显压痛,还可扪及包块。腹膜炎时腹肌明显紧张,有反跳痛。早期肠鸣音可亢进,而后可减弱或消失。
【临床分型】
(一)胃肠炎型
见于疾病的早期有腹痛、水样便、低热,可伴恶心呕吐。
(二)中毒性休克型
出现高热、寒战、神志淡漠、嗜睡、谵语、休克等表现,常在发病1~5天内发生。
(三)腹膜炎型
有明显腹痛、恶心呕吐、腹胀及急性腹膜炎征象,受累肠壁坏死或穿孔,腹腔内有血性渗出液。
(四)肠梗阻型
有腹胀、腹痛、呕吐频繁,排便排气停止,肠鸣音消失,出现鼓肠。
(五)肠出血型
以血水样或暗红色血便为主,量可多达1~2L,明显贫血和脱水。
【实验室检查】
(一)血常规
外周血白细胞增多,以中性粒细胞增多为主,常有核左移。红细胞及血红蛋白常降低,嗜酸性粒细胞及血小板常减少。
(二)粪便检查
外观呈暗红或鲜红色,或隐血试验强阳性,镜下见大量红细胞,偶见脱落的肠黏膜。可有少量或中量白细胞。
(三)粪便培养
Welchii杆菌的分离培养需做厌氧菌培养。但需时较长,一般要7~10日。
(四)尿常规
可有蛋白尿、红细胞、白细胞及管型。部分病例尿液淀粉酶升高。
【特殊检查】
(一)X线检查
腹部平片可显示可见局限性小肠积气及液平面,中、晚期则可见肠麻痹或轻、中度肠扩张,肠腔内多个细小液平面,肠穿孔者可见气腹征象。急性期禁做钡餐及钡剂灌肠检查,以免诱发肠穿孔。
(二)结肠镜检查
可见全结肠腔内有大量新鲜血液,但未见出血病灶,并可见回盲瓣口有血液涌出。
(三)其他检查
轻症病例腹腔镜检查可见肠管充血、水肿、出血、肠壁粗糙及粘连等。腹腔穿刺液淀粉酶可大于5000U/L。
【诊断和鉴别诊断】
诊断主要根据临床症状。有不洁饮食、暴饮暴食史,突发腹痛、腹泻、便血及呕吐,伴有中度发热,或突然腹痛后出现休克症状或麻痹性肠梗阻,应考虑本病的可能,特别是呈腥臭味的洗肉水样便而无明显里急后重者。主要依靠临床综合分析确诊并进行临床分型。
本病需与中毒性菌痢、过敏性紫癜、急性克罗恩病、溃疡性结肠炎、绞窄性肠梗阻、肠套叠、阿米巴肠病以及肠息肉病等鉴别。
【治疗】
本病治疗以非手术疗法为主,配合病因治疗及全身支持治疗,早期联合使用抗生素,纠正水电解质平衡紊乱,解除中毒症状,积极防治中毒性休克及其他并发症。
(一)非手术治疗
1.一般治疗
完全卧床休息,疑诊时即禁食,确诊后继续禁食,禁食时间视病情而定,重症同时禁水。
2.静脉补液或全胃肠外营养(TPN)
本病失水、失钠和失钾者较多见。可根据病情酌定输液总量和成分。纠正代谢性酸中毒。重症患者及严重贫血、营养不良者,可施以TPN。患者恢复进食后可继续辅以肠内营养。
3.纠正休克
除补充晶体溶液外,应适当输血浆、新鲜全血或人体血清白蛋白等胶体液。血压不升者可适当应用血管活性药物。
4.对症疗法
严重腹痛者可予哌替啶;腹胀和呕吐严重者可作胃肠减压,并注意补钾,如有腹水形成可在放腹水后用地塞米松5mg加头孢拉定2.0g、替硝唑0.4g腹腔内注射以减少渗出和促进腹水吸收。便血量多者给云南白药、凝血酶口服。严重出血可用生长抑素及其类似物持续静滴。
5.抗生素
一般二种联合应用。常用的抗生素有:喹诺酮类如环丙沙星,头孢菌素类如头孢三嗪等以及甲硝唑、替硝唑等,静脉滴注或口服。
6.肾上腺皮质激素
有加重肠出血和促发肠穿孔危险,一般应用不超过3~5天;儿童用氢化可的松每天4~8mg/kg或地塞米松1~2.5mg/d;成人用氢化可的松200~300mg/d或地塞米松5~20mg/d,静脉滴注。
7.其他治疗
微生态制剂调节肠道菌群。思密达吸附肠道内毒素,予口服或胃管内注入。有学者采用Welchii杆菌抗毒血清42 000~85 000U静脉滴注治疗本病,取得较好的疗效,但尚未在临床上广泛使用。补充胰蛋白酶可水解β毒素,减少其吸收。常用胰蛋白酶0.6~0.9g口服,3次/天;重症者1000U肌内注射,1~2次/天。疑为或诊断为肠蛔虫感染者在出血停止、全身情况改善后应施以驱虫治疗。
(二)手术治疗
下列情况可考虑手术治疗:①肠穿孔;②严重肠坏死,腹腔内有脓性或血性渗液;③反复大量肠出血,并发出血性休克;④肠梗阻、肠麻痹;⑤不能排除其他急需手术治疗的急腹症。手术方法为:①肠管尚未坏死及穿孔者可用普鲁卡因肠系膜封闭;②肠坏死及穿孔可作肠段切除,穿孔修补及腹腔引流术。
【预后】
本病死亡率直接与败血症、DIC、腹水、极低体重儿有关,可达20%~27%。手术后的短肠综合征,吸收不良综合征等不多见,长期随访术后患儿的生长发育营养状态均较好,营养不良的发生率亦不高。
主要参考文献
Niño DF,Sodhi CP,Hackam DJ.Necrotizing enterocolitis:new insights into pathogenesis and mechanisms.Nat Rev Gastroenterol Hepatol,2016,13(10):590-600.
第九节
假膜性肠炎

陈世耀
假膜性肠炎(pseudomembranous colitis,PMC)是一种主要发生于结肠,也可累及小肠的急性肠黏膜坏死、纤维素渗出性炎症,黏膜表面覆有黄白或黄绿色假膜。临床常见于应用抗生素治疗之后,故有“抗生素相关性肠炎(antibiotic-associated colitis)”之称。现已证实假膜性肠炎主要是由难辨梭状芽孢杆菌(clostridium difficile,CD)的外毒素所致,故又称难辨梭状芽孢杆菌性肠炎。病情轻重不一,严重病例可致死亡。难辨梭状芽孢杆菌相关的腹泻(clostridium difficile associated diarrhea,CDAD)和难辨梭状芽孢杆菌感染(clostridium difficile infection,CDI)曾经被认为主要是医院内获得的疾病,但是近年来社区获得的CDI逐渐被认识,可发生于儿童和成人。
【病因和发病机制】
难辨梭状芽孢杆菌是假膜性肠炎的主要致病菌。该菌为厌氧的革兰阳性菌,广泛存在于自然界的土壤、水、各种动物粪便及人的肠道、尿道及阴道中。
假膜性肠炎的发病主要由难辨梭状芽孢杆菌的菌株、毒素、肠道微生物菌群和宿主共同决定,难辨梭状芽孢杆菌毒素是假膜性肠炎发生的主要机制。难辨芽孢梭状杆菌本身是非侵袭性的,但其产生的A毒素和B毒素可使Rho家族鸟苷三磷酸酶的成员失活,从而导致肠道上皮细胞坏死、肠道屏障功能消失、中性粒细胞浸润;A毒素和B毒素还可通过糖基化破坏细胞骨架,导致肠上皮细胞变圆、液体渗出、细胞坏死。
几乎所有的抗菌药物都能诱发产生本病,以往青霉素类、林可霉素、克林霉素以及第三代头孢菌素最为常见,近年来喹诺酮类药物引起的假膜性肠炎明显增多,曾有院内爆发流行的报道。抗生素应用抑制了肠道的正常菌群,使难辨梭状芽孢杆菌得以迅速繁殖。肠道菌群失调也与假膜性肠炎的复发相关。
基础疾病尤其是患者免疫功能低下是发病最重要的危险因素,包括胃肠道恶性肿瘤手术后,恶性肿瘤接受化疗,器官移植术后接受抗排异治疗,以及其他严重的系统疾病如尿毒症、糖尿病、心力衰竭合并感染状态。此外,环境中难辨芽孢梭状杆菌的孢子污染、年龄≥65岁、抑酸剂、患有炎症性肠病等也是常见的患病危险因素。
【病理】
假膜性肠炎主要侵犯结肠,以乙状结肠最多见,呈连续性分布,严重者可累及全结肠及远端小肠部位。病变肠腔扩张,腔内液体增加。肉眼可见病变处覆有大小不一、散在的高出黏膜面的黄白色斑块,即假膜。随病情进展假膜可由点状融合成不规则片状,严重时可出现剥脱性改变及渗血,局部呈现光剥的区域。显微镜下可见假膜系由纤维素、中性粒细胞、单核细胞、粘蛋白及坏死细胞碎屑组成。黏膜固有层内有中性粒细胞、浆细胞及淋巴细胞浸润,重者腺体破坏、细胞坏死。黏膜下层因炎性渗出而增厚,伴血管扩张、充血及微血栓形成。坏死一般限于黏膜层,严重病例可向黏膜下层伸延,极少数患者因累及肠壁全层而发生肠穿孔。病变愈合后,假膜脱落,假膜下愈合的创面发红,在假膜脱落后10天左右,内镜检查可完全恢复正常。
【临床表现】
本病多发生于50岁以上免疫功能低下的人群,女性多于男性。症状发生多见于抗生素治疗4~10天内或在停用抗生素后1~2周内。起病大多急骤,轻者仅有腹泻,重者可呈暴发型。
(一) 腹泻是最主要的症状,腹泻程度和次数不一,轻型病例,大便每日2~3次,停用抗生素后自愈。重者有大量水样腹泻,每日可达30余次。少数病例有脓血样便,或排出斑块状假膜。
(二) 腹痛通常发生在下腹部,呈钝痛、胀痛或痉挛性疼痛,有时很剧烈,可伴有腹胀、恶心、呕吐。
(三)毒血症表现 包括心动过速、发热、谵妄以及定向障碍等。严重者常发生低血压、休克、严重脱水、电解质紊乱及代谢性酸中毒,甚至急性肾功能不全。
(四)并发症 部分患者由于病情严重或诊治不及时可发生严重并发症,如中毒性巨结肠、麻痹性肠梗阻、肠穿孔等。
【诊断】
在患有严重疾病机体免疫功能低下的病例中,使用抗生素治疗期间或停用抗生素后短期内,突然出现腹泻者,均要考虑本病的可能性。实验室检查不能区分无症状菌群定植和感染,因此诊断需结合临床表现,同时符合以下两点才能诊断为假膜性肠炎:①任何近期使用抗生素并出现不明原因腹泻(24小时内≥3次不成形粪便),或影像学存在肠梗阻或中毒性巨结肠的表现;②粪便检测产毒型难辨梭状芽孢杆菌或其毒素为阳性,或内镜或组织病理检查发现假膜性肠炎。
(一)实验室检查
周围血白细胞增多,在(10~20)×10 9 /L以上,以中性粒细胞为主。粪常规检查仅有白细胞,肉眼血便少见。
疑诊病例应送难辨梭状芽孢杆菌培养。确诊需要利用产毒素培养法(toxigenic culture)检测粪便中的产毒型难辨梭状芽孢杆菌,即将粪便标本在厌氧环境中用特殊培养基培养24~48小时后进行菌株分类,分离后再培养48小时后利用细胞毒测定法(cell cytotoxicity assay,CCA)检测A毒素和(或)B毒素。
(二)内镜检查
及时进行内镜检查不仅能早期明确诊断,还能了解病变的范围和程度。一般认为即使假膜性肠炎急性期也应行结肠镜检查,但应注意结肠黏膜充血水肿,组织变脆,易造成出血或穿孔,检查应特别小心。内镜下主要表现为黄白色隆起斑块(假膜),直径2~10mm。这些小斑块能相互融合,遍布整个肠道黏膜。斑块处活检可以发现典型的顶峰样或“火山”样病变,由炎症细胞、纤维素和来自表面上皮微小溃疡分泌的黏液组成。
(三)X线检查
腹部平片可显示肠麻痹或肠扩张。结肠气钡双重造影间接显示黏膜皱襞水肿增厚,对诊断有一定参考价值,但有肠穿孔的危险,应慎用。
本病应注意与溃疡性结肠炎、克罗恩病、霉菌性肠炎以及艾滋病结肠炎等鉴别。
【治疗】
当高度怀疑重症或伴并发症的假膜性肠炎时,无论实验室结果如何,均应及早开始经验性治疗。治疗措施包括及早停用相关抗生素,加强支持治疗,调整肠道正常菌群,严重者给予抗难辨梭状芽孢杆菌抗生素或抗毒素治疗。极少病例因肠梗阻或穿孔需手术。合理使用抗生素,严格掌握用药指征是防止假膜性肠炎的关键。
(一)停用原有抗菌药物
多数患者停用相关抗生素能自行缓解而呈自限性。对必须使用抗生素患者应考虑更换。
(二)支持治疗
包括补液维持水、电解质及酸碱平衡,输入血浆、白蛋白纠正低蛋白血症。严重营养不良者可全胃肠外营养,有低血压休克者可在补充血容量基础上应用血管活性药物。肾上腺皮质激素可短期小量应用,以改善毒血症症状。
(三)微生态制剂治疗
直接或间接补充生理菌,纠正肠道菌群失调。
(四)抗生素治疗
一线用药为甲硝唑和万古霉素。
1.甲硝唑
甲硝唑适用于疾病轻中度者,对重度或伴并发症者疗效欠佳。在严重或危及生命的艰难梭菌感染中,禁止口服甲硝唑。成人剂量500mg口服,3次/天,疗程10~14天。主要不良反应包括胃肠道反应、双硫仑样反应、口腔内的金属异味,长期使用可能导致周围性神经病变。妊娠妇女禁用。
2.万古霉素
可抑制难辨梭状芽孢杆菌生长,是目前认为治疗假膜性肠炎最有效的药物,可用于甲硝唑治疗失败、耐药或过敏者,以及疾病轻中度的妊娠妇女和哺乳期妇女。成人剂量为125mg口服,4次/天,疗程10~14天。该药口服和直肠使用不吸收,对肾脏无损害,在肠道内可达到高浓度,静脉给药不宜采用。
3.非达霉素(fidaxomicin)
是一种大环内酯类杀菌药,口服不吸收,能有效对抗革兰阳性厌氧菌,与万古霉素的疗效无明显差异,但可降低非BI/NAP1/027菌株感染的复发率,对原有抗生素停用的假膜性肠炎效果更好,因此若初发患者存在复发的高危因素(≥65岁、有并发症、使用质子泵抑制剂或抗生素等),也可在首次治疗时使用。成人剂量为200mg口服,2次/天,疗程10~20天。
4.其他的抗生素
包括夫西地酸、利福昔明、硝唑尼特、雷莫拉宁、替考拉宁、杆菌肽等,但由于有限的研究并未表明其有明显的疗效优势,且花费较高、副作用大、可能存在难辨梭状芽孢杆菌耐药(尤其是利福昔明),一般不推荐常规使用,仅在上述抗生素治疗后无效或有严重不良反应时可尝试使用。利福昔明成人剂量为550mg口服,2次/天,疗程20天。
抗生素的治疗方案是根据疾病的严重程度及复发风险决定的(表15-6-6)。
表15-6-6 假膜性肠炎的抗生素治疗方案
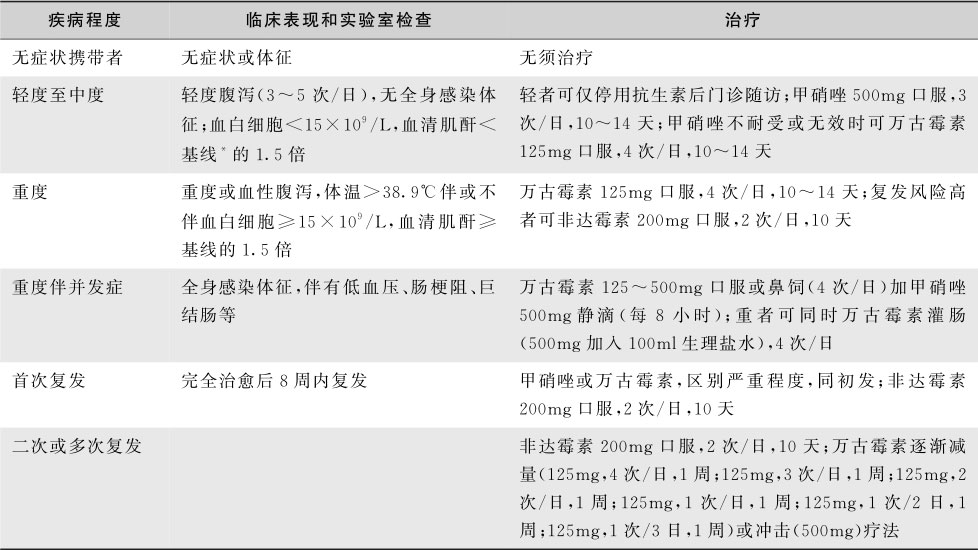
注: * 基线指发病前的血清肌酐水平
(五)抗毒素及抑制毒素吸收治疗
抗污泥梭状芽孢杆菌抗毒素可中和难辨梭菌毒素,国外已用于临床。
(六)免疫治疗
静滴丙种球蛋白可用于治疗难辨梭状芽孢杆菌感染,其机制主要为中和难辨梭状芽孢杆菌毒素A。
(七)粪便微生物移植(Fecal Microbiota Transplantation,FMT)治疗
停用所有抗生素,同时将健康、经筛选的捐献者的粪便移植至患者肠道内,可将复发性假膜性肠炎的平均治愈率提高至90%以上,疗效优于万古霉素。FMT治疗的适应证包括:①反复发作的假膜性肠炎(尤其是对万古霉素缓慢减量或冲击疗法无效者);②标准疗法(万古霉素或非达霉素)治疗1周无效的中度假膜性肠炎;③标准疗法治疗48小时无效的重度或暴发性假膜性肠炎。轻度不良反应包括一过性发热、腹泻、呕吐、便秘等,严重不良反应如穿孔、出血、窒息等主要由FMT的操作导致。
(八)手术治疗
在暴发型病例,内科治疗无效或并发肠梗阻、中毒性巨结肠、肠穿孔时,可考虑手术治疗。
【预后】
轻症病例在停用抗生素之后可自愈,重者经及时诊断及积极治疗预后良好。约10%~20%的患者在初治停药1~3周后可再次出现腹泻,其原因可能是灭菌不彻底或再感染。复发病例轻者可应用调整肠道菌群药物,重者需再次使用甲硝唑或万古霉素治疗。多次复发者可考虑应用粪便微生物移植或免疫治疗。出现严重并发症如中毒性巨结肠、麻痹性肠梗阻、肠穿孔时,病死率可达到16%~22%。
【预防】
由于疾病带来的影响及复发的难治性,假膜性肠炎的预防十分重要。一是切断传播途径,包括戴手套、穿隔离衣、手卫生、隔离、打扫环境等,防止难辨芽孢梭状杆菌的孢子与患者接触;二是减少高危因素,最重要的是抗生素的合理运用,尤其是克林霉素、头孢类、喹诺酮类抗生素的使用。
主要参考文献
1.Leffler DA,Lamont JT.Clostridium difficile infection.N Engl J Med,2015,372(16):1539-1548.
2.Bagdasarian N,Rao K,Malani PN.Diagnosis and treatment of Clostridium difficile in adults:a systematic review.JAMA,2015,313(4):398-408.
第十节
炎症性肠病

戎兰 蒋义斌
炎症性肠病(inflammatory bowel disease,IBD)是一种特发性肠道炎症性疾病,包括溃疡性结肠炎(unclerative colitis,UC)和克罗恩病(Crohn's disease,CD),以慢性、反复复发、病因不明为其特征。溃疡性结肠炎是结肠黏膜层和黏膜下层连续性炎症,疾病先通常累及直肠,逐渐向全结肠蔓延,克罗恩病可累及全消化道,为非连续性全层炎症,最常累及部位为末端回肠、结肠和肛周。
【流行病学】
IBD在西方国家较为常见,欧洲UC年发病率最高发病率分别为24.3/10万,CD为12.7/10万,UC和CD的患病率分别为505/10万、322/10万。我国发病率也呈逐年上升趋势。我国IBD协作组根据住院患者粗略推算UC患病率约为11.6/10万,CD约为1.4/10万。大部分地区UC较CD常见,CD发病率女性高于男性,UC则男性略高。青春后期或成年初期是IBD主要的发病年龄段。
【病因和发病机制】
疾病机制尚未完全明确,是近年来研究极其活跃的领域。
(一)环境因素
在经济较发达的地区发病率持续增高,如北美、北欧、继之西欧、日本、南美等。南亚裔发病率低,但移居至英国后IBD发病率增高,表明环境因素起着重要作用。食物结构与IBD的关系尚未取得统一意见。吸烟对UC者起保护作用,被动吸烟者中发病率也明显降低,而吸烟则使CD者疾病恶化。有一种假说:随着环境条件的改善,人们接触致病菌的机会减少,儿童期肠黏膜针对病原菌不能产生有效的“免疫耐受”,以致其后对肠道抗原刺激产生异常免疫调节。
(二)遗传因素
IBD者同卵双胞胎,兄弟姐妹和一级亲属发病率明显升高,IBD一级亲属的发病率是普通人群10~15倍。白种人发病率较高,黑种人、黄种人则较低;犹太人较非犹太人高。已发现IBD有超过163个基因易感性位点,其中一些基因可能与疾病诊断、严重程度,预测患病易感性及并发症有关。第一个发现与克罗恩病相关 NOD 2基因位于16q12,NOD-2/CARD15突变引起免疫激活异常,抑制炎症作用降低,导致组织和细胞发生持续性损伤,约30%CD被检测出异常的 NOD2 基因。其他较明确的基因有 ATG16L1 基因、 IRGM 基因、 toll-4 基因、 IL-23 受体基因、 H LA- Ⅱ、 OCTN1 和 DLG5 等。目前认为IBD不仅是多基因疾病,也是一种遗传异质性疾病,患者在一定环境因素作用下由于遗传易感性而发病。
(三)微生物因素
微生物参与IBD发生发展,但至今尚未找到某一特异微生物病原与IBD有恒定关系。当IBD动物模型处于无菌状态时,不能诱导肠道炎症,恢复正常菌群后,则出现肠道炎症,使用抗生素后,又可减少肠道炎症的发生。特别是菌群的改变可能通过抗原刺激引起肠组织持续性炎症。临床上粪便转流能防治CD复发。
(四)免疫因素
正常情况下,肠组织对肠腔内抗原物质(食物或微生物)处于适应性反应,即低度慢性炎症,先天性免疫是监视微环境改变,限制感染入侵的生物手段。当肠道上皮屏障破坏,黏膜通透性增加,肠组织暴露于大量抗原中,免疫耐受的丢失,而获得性免疫是IBD肠黏膜损伤最重要的原因。其中黏膜固有层的T细胞激活,Th1/Th2比例失衡,Th1升高促使IFN-γ、TNF-γ、IL-12增加,IL-4减少,Th2升高刺激IL-5和IL-13分泌增多;另外,TH17细胞通过IL-17和IL-23进一步上调和维持异常免疫反应,导致肠道免疫系统错误识别,释放大量细胞因子和炎症介质,刺激炎症免疫应答逐级放大,最终导致组织损伤。
目前认为IBD的发病机制可能为:环境因素作用于遗传易感者,当先天免疫系统无法清除肠腔内微生物或食物等抗原时,增加肠上皮细胞通透性,最终导致了过度的免疫反应。
【临床表现】
一般起病缓慢,少数急骤。病情轻重不一。易反复发作,发作的诱因有精神刺激、过度疲劳、饮食失调、继发感染等。
(一)症状
UC症状取决于疾病的程度和严重性。包括黏液血便、腹泻、里急后重、排便紧迫感、腹痛等。直肠炎或直乙状结肠炎者少数可能表现为便秘,排便困难。重度和广泛性结肠炎者可因贫血而乏力,或低白蛋白血症出现外周水肿,可有体重下降和发热,甚至恶心和呕吐。
CD症状以右下腹痛多见,腹泻、便血、乏力为常见症状。严重者表现为发热、营养不良。有些患者可出现突发性剧烈腹痛或阵发性加重性腹痛伴腹胀、恶心、呕吐等肠梗阻或肠穿孔症状。上消化道病变症状伴有吞咽困难,胸痛,上腹部疼痛,烧灼感及呕吐等。肛周累及者,伴发肛门处疼痛和脓液分泌。消化道各处均可形成腹腔内脓肿,肠道膀胱瘘,肠道阴道瘘和皮瘘等内瘘和外瘘。
(二)体征
与疾病的类型,部位和严重程度相关。UC轻型者或在缓解期可无阳性体征,重型可有发热、脉速的表现,左下腹或全腹部压痛,若出现腹部膨隆、腹肌紧张,伴发热、脱水、呕吐等,应考虑中毒性巨结肠。CD者腹部常扪及腹块伴压痛,以右下腹和脐周多见。有急性或慢性胃肠道梗阻、肠穿孔和消化道出血体征,肛门周围炎症的体征。
(三)肠外表现
与自身免疫有关。包括①骨病:是最常见的肠外表现,约10%~20%患者累及,包括外周关节痛、骨软化、关节炎、强直性脊柱炎、骶髂关节炎,严重程度可与胃肠道症状相关。②皮肤表现:结节性红斑、坏疽性脓皮病等。③眼损害:结膜炎、虹膜炎、眼色素层炎等。④肾脏结石:草酸钙结石与小肠CD脂肪吸收不良相关,尿酸结石与严重营养不良有关。⑤原发性硬化性胆管炎。⑥血栓性静脉炎、血管栓塞。⑦贫血唇炎可能由于缺铁性贫血所致,而维生素B 12 缺乏可引起周围神经病变。CD者肠外表现还包括口疱疹性溃疡、继发性肾脏淀粉样变、哮喘、儿童生长发育延迟等。
【诊断标准】
包括病史采集、体格检查、内镜、影像学、实验室及组织细胞学检查,同时应鉴别诊断以排除其他疾病。
(一)内镜检查
对腹泻、便血、腹痛等症状疑诊IBD者,内镜检查对本病诊断有重要价值,但在急性期重型患者应暂缓进行,以防穿孔。UC表现为从直肠开始,弥漫性黏膜充血水肿,质脆、自发或接触出血和脓性分泌物附着,常见黏膜粗糙、呈细颗粒状,黏膜血管纹理模糊、紊乱,多发性糜烂或溃疡;慢性病变见假性息肉,结肠袋变钝或消失。CD早期表现表面阿弗他溃疡,随着疾病发展,溃疡变深变大,成纵形和匍匐形溃疡,炎症黏膜非对称性分布,周围鹅卵石样增生,肠腔狭窄,偶见瘘口等改变,病变为节段性,从食管至肛门均可累及,但在回结肠部位多见。通常认为,若发现小肠多发性阿弗他溃疡,环形、线形或不规则溃疡≥3个,或发现狭窄,则应当考虑CD的诊断。胶囊内镜检查结果仍应遵循由小肠镜活检进一步证实。因其创伤性,应遵循胶囊内镜优先原则,若有狭窄等并发症不考虑胶囊内镜检查。少部分CD病变可累及上消化道,胃镜检查应列为CD的常规检查,尤其伴有上消化道症状者。
(二)病理组织学检查
黏膜活检组织学检查建议多段多点活检。
UC病理表现为上皮细胞坏死,固有层急性炎症细胞浸润,隐窝炎,隐窝脓肿,隐窝结构改变,杯状细胞减少,浅溃疡形成和肉芽组织增生。慢性病变则表现为淋巴细胞的浸润和隐窝结构变形紊乱,腺上皮和黏膜肌层间隙增宽、潘氏细胞化生。
CD改变包括裂隙状溃疡和阿弗他溃疡、固有膜炎性细胞浸润,黏膜下层增宽、淋巴细胞聚集,隐窝炎,隐窝脓肿,隐窝结构扭曲、分支和缩短。手术切除的肠段可见穿透性肠壁炎症,纤维化以及系膜脂肪包绕,局部淋巴结有肉芽肿形成。非干酪性肉芽肿是诊断CD的标准之一,活检标本中发现率约15%和手术标本多达70%左右。
(三)影像学检查
结肠钡剂灌肠可显示UC者结肠黏膜粗乱和(或)颗粒样改变;肠管边缘呈锯齿状阴影,肠壁有多发性小充盈缺损;肠管短缩,袋囊消失呈铅管样。急性期及重型患者应暂缓检查,以免诱发中毒性巨结肠,甚至穿孔。用CT或MR肠道显像(CT/MR enterography,CTE/MRE)检查也可显示肠道病变。结肠钡剂灌肠已被结肠镜检查所代替,当CD者肠腔狭窄内镜无法检查时仍有诊断价值。而小肠钡剂造影敏感性低,已被CTE或MRE代替。
CTE或MRE是评估CD小肠炎性病变的标准影像学检查,活动期CD表现为肠壁明显增厚(>4cm),肠黏膜明显强化伴有分层改变,呈“双晕征”,即黏膜内环和浆膜外环明显强化,提示黏膜下层水肿,早期肠壁增厚以肠系膜侧为重,称偏心性增厚,随着病情发展,对侧肠壁也明显增厚;肠壁的炎症呈节段性分布,有不规则扩张和狭窄(炎症活动性或纤维性狭窄);肠腔外并发症如瘘管形成、腹腔脓肿或蜂窝织炎等,肠系膜血管增多、扩张、扭曲,呈“木梳征”;相应系膜脂肪密度增高、模糊;肠系膜淋巴结肿大等;MRE是诊断CD复杂性瘘管和脓肿的重要手段,并能评价肛门内外扩约肌的完整性。由于MRI无电离辐射,特别是对年轻及儿童IBD患者,更适合作为长期随访手段。
腹部超声对发现肠壁厚度、瘘管、脓肿和炎性包块具有一定价值,缺点是结果判断带有一定的主观性。
(四)实验室检查
1.血液检查
贫血常见,主要由消化道出血引起缺铁或吸收不良所致叶酸和维生素B 12 等缺乏,也可能与溶血有关。急性期中性粒细胞可增高。血浆Ⅴ、Ⅶ、Ⅷ因子活性和纤维蛋白原增加,血小板数常明显升高,引起血栓性栓塞现象。严重者白蛋白降低。血沉增快,C反应蛋白升高,与疾病活动有关。
2.粪便检查
镜检可见红、白细胞,隐血阳性。钙卫蛋白主要存在于中性粒细胞内,肠道炎症时,粪便中钙卫蛋白明显增高,与疾病炎症程度有较好相关性,可重复检测和量化。
3.免疫学检查
抗中性粒细胞核周胞质抗体(antineutrophil cytoplasmic,pANCA)在UC患者中阳性率约55%,CD者仅20%,但系统性血管炎、原发性硬化性胆管炎、自身免疫性肝炎、胶原性结肠炎、嗜酸性粒细胞性结肠炎等疾病也可检出,因此应用价值有一定限制。CD者抗酿酒酵母菌抗体(antisaccharomces cerevisiae antibody,ASCA)阳性率40%~70%,UC者则低于15%。ASCA阳性pANCA阴性者诊断CD敏感性55%,特异性达93%。抗埃希氏大肠埃希菌外膜孔道蛋白C抗体(OmpC抗体)、抗荧光假单胞菌抗体(I2抗体)和抗鞭毛样抗体(Cbir1抗体)阳性提高诊断CD的准确性,其与疾病复杂的临床表现相关。
【诊断步骤】
有典型临床表现疑诊IBD者,若符合结肠镜或影像学检查中一项,可为拟诊者,若有病理学特征性改变,可以确诊。初发病例、临床表现和结肠镜改变均不典型,应列为“疑诊”随访;为明确诊断推荐进行3~6个月密切随访。内镜诊断中由于肠黏膜组织活检受到取材广度和深度的限制,病理诊断确有很大困难,因此诊断有时需要建立在排除诊断的基础上。
(一)鉴别诊断
需与感染性肠炎鉴别,包括细菌(空肠弯曲杆菌、艰难梭状芽胞杆菌、结核分枝杆菌、沙门氏菌、出血性大肠埃希菌、耶尔森氏鼠疫杆菌等),病毒(巨细胞病毒、单纯疱疹病毒、人类免疫缺陷病毒),真菌(组织胞浆菌),寄生虫(阿米巴、血吸虫);与系统性疾病鉴别,包括白塞病、变应性肉芽肿血管炎、过敏性紫癜、系统性红斑狼疮、结节性多动脉炎、淀粉样变等;与药物性/毒素性肠炎鉴别:非甾体类抗炎药,胰酶、盐类泻剂、放射性肠炎;与炎症性疾病鉴别,阑尾炎、憩室炎、嗜酸性胃肠炎、脂泻病;肿瘤:淋巴瘤、类癌、原发性或转移性癌、恶性组织细胞增生症;其他还包括缺血性肠炎、子宫内膜异位症、末端回肠孤立性溃疡等。
1.感染性结肠炎
各种致病菌感染通常在4周后均能恢复正常。急性发作时可有发热,腹痛,腹泻,黏液血便等,但粪便检查分离致病菌阳性率较低。内镜检查炎症分布多不均匀,呈片状充血水肿、糜烂,大小不一,形态多变的溃疡。直肠炎应鉴别性传播疾病,如淋病、梅毒、衣原体等感染。
2.肠结核
与CD相互误诊率较高,治疗和预后迥异。肠结核常伴有结核病史,内镜多见浅表性不规则形环行溃疡、边缘不整如鼠咬状,盲肠病变多于回肠、回盲瓣常受累,呈张口状。CD者常为纵行溃疡或阿弗他溃疡、鹅卵石样表现、回肠病变多于盲肠、回盲瓣狭窄或有溃疡形成。影像学检查结核常见腹水、肿大肠系膜淋巴结多>1cm伴有钙化及中心衰减。CD者多见病变处脂肪包裹、腹腔内淋巴结约3~8mm、肠系膜血管束梳样征扩大。当不能除外肠结核时应抗结核诊断性治疗。
3.白塞病
以反复发作口腔溃疡,生殖器溃疡,眼部病变和多形性的皮疹为主要特征,也可以末端回肠和回盲部溃疡为主要症状。白塞病病变常累及回盲部(上、下50cm),溃疡表现为单发或多发,深浅不一溃疡,可致肠壁穿孔,边界清楚,溃疡间不融合,无纵形溃疡、鹅卵石样表现、肠腔狭窄及瘘管形成等表现。
4.UC和CD
两者临床表现、内镜和组织学特征均明显不同,特别是裂沟、瘘管、穿透性炎症、肛门病变、肠腔狭窄和非干酪样性肉芽肿等特征具有重要的鉴别诊断价值。当肠道病变不典型时,较难鉴别,可暂诊断为未定型结肠炎(indeterminate colitis)。经长期随访才能最终诊断。
(二)疾病评估
包括疾病类型、病情程度、活动性、病变范围、并发症和肠外表现,以便选择治疗方案,用药途径和评估预后。
UC疾病评估
1.临床类型
分为初发型、慢性复发型。
2.病变范围
分为直肠炎、左半结肠炎、广泛性结肠炎。
3.疾病活动性的严重程度
UC病情分为活动期和缓解期,改良的Tmelove和 Witts严重程度分型标准,见表15-6-7。
4.并发症
中毒性巨结肠、肠穿孔、消化道大出血、上皮内瘤变和癌变。
CD疾病评估
1.临床类型
推荐按蒙特利尔CD表型分类法进行分型,见表15-6-8。
2.疾病活动性的严重程度
分成缓解期和活动期,常选用Harvey和Brashow标准判定疾病活动指数(CDAI),见表15-6-9。
表15-6-7 改良Truelove和Witts疾病严重程度分型(溃疡性结肠炎)

注:中度为介于轻、重度之间
表15-6-8 克罗恩病的蒙特利尔分型
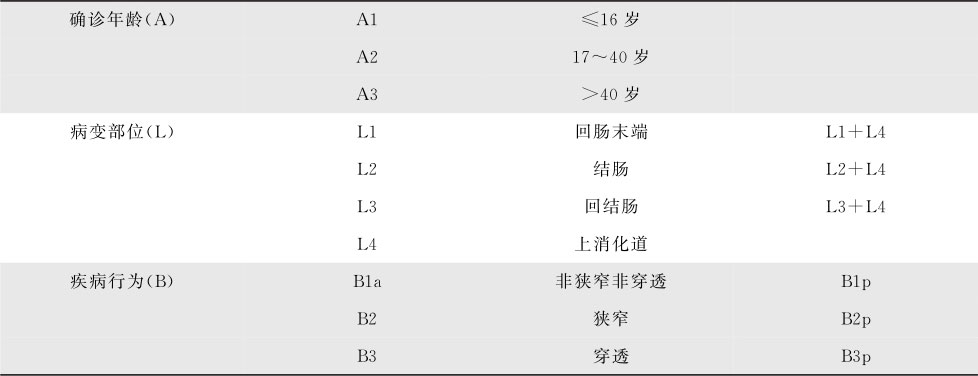
注:a随着时间推移B1可发展为B2或B3;L4可与L1、L2、L3同时存在;p为肛周病变,可与B1、B2、B3同时存在
表15-6-9 简化CDAI计算法

注:≤4分为缓解期;5~8分为中度活动期;>9分为重度活动期
3.并发症
40%以上病例有程度不等的肠梗阻,且可反复发生。急性肠穿孔占10%~40%。可有肛门区和直肠病变以及瘘管、脓肿、出血和癌变等。
【治疗】
(一)一般治疗
慢性疾病常伴有营养不良,主张高糖、高蛋白、低脂饮食,少渣饮食能减少排便次数。适当补充叶酸、维生素和微量元素,全肠外营养适用于重症患者及中毒性巨结肠、肠瘘、短肠综合征等并发症者。CD戒烟有益于疾病控制。应用止泻剂(洛哌丁胺)可减轻肠道蠕动,但严重结肠炎时,止泻剂与解痉剂需禁用,有诱发中毒性巨结肠的可能。因疾病反复发作,迁延终生,患者常见抑郁和焦虑情绪,需予心理问题的防治。
(二)治疗常用药物
1.氨基水杨酸制剂
包括不同制剂的美沙拉嗪(5-aminosalicylic acid,5-ASA)和传统的柳氮磺胺吡啶(Sulfasalazine,SASP),是治疗UC的主要药物,对CD治疗作用较小。活动性病变予3~4g/d,维持期予2g/d。SASP在结肠内由细菌分解为5-ASA和磺胺,长期服用SASP者需补充叶酸并关注磺胺药相关的副作用。5-ASA具有肠腔局部抗炎作用,理想剂型应尽量减少肠道内吸收使局部疗效作用更大。常用的美沙拉嗪制剂:前体药物有奥沙拉嗪(偶氮二聚体)和巴柳氮(偶氮异二聚体),在结肠中释放起效;pH值依赖包衣制剂在回肠末端pH值5~7时溶解释放,大部分仍进入结肠;时间依赖的制剂起效范围从远端空肠至结肠。5-ASA肛栓剂和灌肠剂对溃疡性直肠和乙状结肠炎均有效。不良反应较少,包括恶心、消化不良、脱发、头痛、腹泻和过敏反应。
2.糖皮质激素
适用于急性活动的中重度UC和CD者,无维持缓解作用。另一方面因其不良反应,限制长期应用。常用剂量泼尼松0.75~1mg/kg,2个月左右病情缓解。起始剂量需足量,否则疗效降低。布地奈德是一种局部作用强而系统生物利用度较低(10%)药物,提高治疗疗效,减少治疗的不良反应。若使用激素常用剂量超过4周,疾病仍处于活动期提示激素无效;若激素治疗有效后停用激素3个月内复发或激素治疗3个月后,泼尼松减量至10mg/d复发者提示激素依赖。
3.免疫调节剂
适用于激素依赖或无效以及激素诱导缓解后的维持治疗。硫唑嘌呤(azathioprine,AZA)是维持缓解最常用的药物,AZA不能耐受者可换用6-巯基嘌呤(mercaptopurine,6-MP)或甲氨蝶呤(methotrexate,MTX)。国内IBD协作组推荐AZA剂量为1mg/kg,欧洲共识推荐的目标剂量1.5~2.5mg/kg,由于AZA存在量效关系,剂量不足会影响疗效,因此可在治疗观察中逐渐增加剂量。AZA通常3~4个月才能达到稳态血药浓度,治疗时可先与激素联用,待免疫调节剂起效后,激素再逐渐减量。服药1个月内骨髓抑制不良反应最常见,但是也可迟发1年以上,同时还需随访肝功能。甲氨蝶呤和沙利度胺(thalidomide)适合不耐受巯嘌呤药物者,目前临床经验尚少。诱导缓解期常推荐MTX 25mg/w肌肉或皮下注射,缓解后改为15mg/w肌肉或皮下注射,口服疗效降低。环孢素(cyclosporin,CsA)1周内快速起效,2~4mg/kg,因不良反应大,适于短期治疗严重UC且激素无效者,促症状缓解,避免急诊手术。临床症状缓解后可改为CsA口服(4~6mg/kg)或转为巯嘌呤药物。
4.生物制剂
主要适用于经激素及免疫调节剂治疗无效或不能耐受者;合并瘘管经传统治疗无效者。英夫利昔单抗(infliximab,IFX)是抗肿瘤坏死因子(TNF-α)抑制剂,目前治疗IBD应用时间最长的生物制剂,对大部分IBD患者有效。IFX是人-鼠嵌合型单克隆抗体,静脉推荐滴注5mg/kg,在0、2、6周作为诱导缓解,随后每隔8周给予相同剂量维持缓解。规律用药的缓解率优于间断给药,联合免疫调节剂可减少生物机制抗体形成,增加疗效。单次使用IFX 5mg/kg的有效率可达58%,使用IFX3次后,55%CD者瘘管可愈合。若治疗产生了抗IFX抗体,可换用全人重组抗TNF阿达木单抗(adalimumab)或赛妥珠(certolizumab pegol)。另一类生物制剂是针对白细胞黏附分子的靶向治疗药物,如Natalizumab,vedolizumab,已被证明是一种有效的能诱导缓解对抗TNF无应答的患者。生物制剂有激活潜在的结核菌及乙型肝炎(HBV)感染的危险,抑炎作用可能影响机体免疫监视功能,特别是联合免疫调节剂,有诱发淋巴瘤报道。其他不良反应包括多发性硬化、脱髓鞘病变和视神经炎等。
5.抗生素类
肠道菌群为慢性肠道炎症提供刺激。抗生素常用于CD并发症的治疗,即肛周病变、瘘管、炎性包块及肠道狭窄时细菌过度增长等。推荐使用4~8周的甲硝唑或环丙沙星,部分患者症状可缓解,但停药后会复发。近来发现利福昔明对轻中度CD有一定治疗效果。甲硝唑能预防CD术后的复发。抗生素长期应用将增加艰难梭状芽孢杆菌相关疾病的风险。
6.益生菌
为肠道防御系统构建正常肠道菌群,但尚无确切证据支持其疗效。有研究示双歧杆菌和乳杆菌减少的菌群紊乱可能是引起储袋炎原因之一,益生菌(probiotics)能维持缓解部分储袋炎患者。
7.干细胞移植
造血干细胞移植会重置免疫系统,去除自身反应性T淋巴细胞和记忆细胞,从而诱导长期的免疫耐受。目前治疗的病例数有限,干细胞来源各异,输注的方式和剂量也不相同。因此仍需要严密谨慎的研究。
(三)治疗原则和方案选择
治疗方案应对病情进行综合评估,包括病变累积范围、部位,病程的长短,疾病严重程度以及全身情况,给予个体化、综合化治疗。原则上应尽早控制疾病的症状,维持缓解,促进黏膜愈合,防治并发症和掌握手术治疗时机。
UC直肠炎选择5-ASA栓剂治疗,联合口服5-ASA疗效优于单口服者,5-ASA栓剂优于局部激素应用,局部激素适用于5-ASA治疗无效者。局部泡沫剂和灌肠剂用于治疗左半结肠炎。广泛性结肠炎口服5-ASA联合栓剂或灌肠剂治疗可提高疗效。复旦大学附属中山医院消化科30多年来应用配制的药方(曲安奈德40mg,SASP 2g,锡类散1支,利多卡因0.1g,生理盐水100ml)灌肠,对于血便等症状的改善效果优于其他激素类型及5-ASA灌肠。重度UC者可暂禁食,予补液、胃肠外营养,中毒症状明显者予抗生素,口服或静脉激素为首选治疗,若甲泼尼龙40~60mg静脉滴注5天症状无好转时,排除继发感染后,药物可更替为Cs A或生物制剂治疗,必要时手术切除。激素治疗症状缓解后可每1~2周减5mg泼尼松至停药,快速减量易导致早期复发。维持治疗首选5-ASA,原诱导剂量的全量或半量,远段结肠炎以5-ASA局部治疗为主,联合口服疗效更佳。若激素依赖者,应更改为免疫调节剂或生物制剂。维持治疗疗程5年或更长。
5-ASA和布地奈德(9mg/d)对轻中度回结肠和结肠型CD有一定作用,对上消化道CD(空肠、十二指肠、胃和食管)则无效,对长期维持治疗疗效则不肯定。中重度CD首选激素或生物制剂诱导疾病缓解,随后继用免疫调节剂或生物制剂维持缓解。广泛性小肠病变(累计长度>100cm)者因肠腔多处狭窄,小肠细菌过度生长、营养不良、手术造成短肠综合征等复杂的情况,建议早期使用免疫调节剂和生物制剂IFX积极治疗,营养治疗应作为重要的辅助手段。
(四)手术治疗
在治疗过程中,大多数CD者将因纤维狭窄所致的梗阻,复杂性肛瘘、肠皮瘘、各种内瘘,腹腔脓肿,急性穿孔和大出血,癌变等均面临着手术缓解症状的问题,但手术治疗不能治愈疾病,接受多次手术的概率相当常见。因此术后应定期内镜复查,吸烟,穿透性疾病,肛周病变及既往有肠切除史者复发率更高,5-ASA、AZA对术后预防复发有一定作用,AZA疗效更佳,若发现内镜下复发,建议转换为生物制剂。内科积极治疗下无效重度UC,特别是中毒性巨结肠需手术治疗,手术回肠贮袋-肛管吻合术(IPAA)。IPAA手术后40个月约50%出现储袋炎,可选择抗生素(如甲硝唑)或5-ASA和激素局部治疗。
内科医生因对手术有充分认识,避免贻误手术时机。术前术后使用激素者应尽可能减少激素剂量,以防止手术并发症。AZA不增加围术期并发症发生率。IFX单抗治疗对手术后并发症尚无明确报道。
(五)肿瘤检测
广泛性UC和CD者,发生肠癌的概率比一般人群增高约为5%~10%。建议起病8~10年开始每1~2年1次结肠镜检查,随机取样活检。如发现高度异型增生,建议手术切除全结肠。低度异型增生需3~6个月随访。
IBD的发病率在我国呈逐渐上升的趋势,越来越受到人们重视。炎症性肠病是慢性终身性肠道炎症,一生中将面临各种复杂临床变化,需要内外科医生,放射科,病理科及营养科的密切协作,避免肠道功能的进展性损伤。
主要参考文献
1.中华医学会消化病学分会炎症性肠病协作组.对我国炎症性肠病诊断治疗规范的共识意见.中华消化杂志,2012,(51):818-831.
2.Lichtenstein GR.Inflammatory bowel disease-Goldman's.Goldman L,Ausiello O.Cecil Medicine,25th ed.Elsevier saunders,2016.935-943.
第十一节
吸收不良综合征

陈世耀
吸收不良综合征(malabsorption syndrome)是一种因小肠对营养物质消化、吸收功能障碍,造成营养物质不能正常吸收,而从粪便中排泄,引起营养物质缺乏的临床综合征。临床上常表现为腹泻,粪便稀薄而量多、油腻多等脂肪吸收障碍症状,故又称脂肪泻。
吸收不良综合征可分为原发性和继发性两大类。原发性吸收不良综合征是指小肠黏膜具有某种缺陷,从而影响营养物质吸收以及脂肪酸在细胞内的再酯化而发病。继发性吸收不良综合征见于多种因素造成的消化不良或吸收障碍。
【小肠吸收生理】
小肠是人体营养物质消化吸收的主要部位,成人平均长度约5~7m。营养物质的吸收在小肠各段有所不同。小肠近段(包括十二指肠远端和空肠近端)主要吸收铁、钙、水溶性维生素(叶酸、维生素C、B族,但不吸收维生素B 12 )、脂肪酸、甘油-酯和部分单糖。小肠中段主要吸收部分单糖和大部分氨基酸。小肠远段(回肠末端)对胆盐和维生素B 12 有选择性吸收作用。
【病理】
吸收不良综合征的病理特点是小肠绒毛萎缩。肉眼所见的黏膜可从正常的海虎绒毛状变为平绒状。显微镜下可见柳叶状绒毛缩短,形态不规则,尖端变钝,互相融合,有时绒毛可消失。表层环状细胞减少,上皮下层炎性细胞增多、腺体增生。黏膜柱状上皮细胞变低平,胞质有核细胞减少,上皮下层炎性细胞增多、腺体增生。黏膜柱状上皮细胞变低平,胞质有空泡,核大小不一,微绒毛模糊不清。有些病例可见黏膜粗厚,呈慢性炎症改变,绒毛仍存在,但杂乱无章。肠腔可有不同程度的扩大,这在幼儿乳糜泻中尤为明显。
【病因与分类】
吸收不良综合征的病因很多,分类也很不一致,消化吸收过程中任何环节障碍均可引起吸收不良综合征。吸收不良综合征的病因分类见表15-6-10。
表15-6-10 吸收不良综合征的病因分类

续表

【临床表现】
吸收不良综合征由于营养物质、维生素以及电解质、矿物质等吸收障碍,引起一系列病理生理改变(表15-6-11)。
表15-6-11 吸收不良综合征的临床表现及病理生理机制
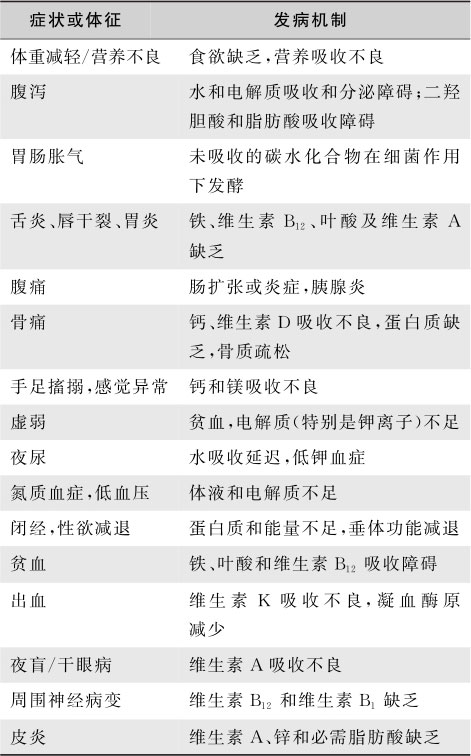
【病理生理】
(一)消化功能障碍
主要指对脂肪、糖和蛋白质的消化不良,其中脂肪消化不良尤为突出。
(二)黏膜摄取和细胞内加工障碍
具有完整结构和功能的吸收细胞依靠细胞脂类组分的溶解性,将与胆盐组成微胶粒复合体的脂肪摄入胞内,形成乳糜微粒。在热带性口炎性腹泻、麦胶性肠病、病毒性肠炎时,吸收细胞受损,较不成熟的隐窝细胞增生以替代受损的吸收细胞。这些细胞加工脂肪的结构与功能并不健全。
(三)淋巴血流转运障碍
Whipple病、α重链病、溃疡性结肠炎、小肠多发性淋巴瘤、小肠淀粉样变等可致肠壁受损,小肠绒毛剥脱或肿胀变形,导致肠淋巴回流障碍和脂肪吸收不良。
(四)肠黏膜异常
肠黏膜酶缺乏如乳糖酶、蔗糖酶、海藻糖酶缺乏,以及单糖转运障碍等均可影响小肠消化和吸收过程,从而导致吸收不良。
(五)小肠运动障碍
动力过速如甲状腺功能亢进等,影响小肠吸收时间;动力过缓,如假性小肠梗阻、硬皮病,导致小肠细菌过度生长。
(六)小肠细菌过度繁殖
细菌分解营养物质产生小分子脂肪酸、羟基长链脂肪酸,分解胆盐,使小肠吸收水和电解质障碍,肠黏膜细胞向肠腔分泌水和电解质增加,进而引起腹泻。
【辅助检查】
(一)粪脂测定
1.苏丹Ⅲ染色法
将一新鲜标本涂在载玻片上,滴冰醋酸微微加热数秒钟后即可形成脂肪小滴,用苏丹Ⅲ染色后可在光镜下观察着色的脂肪滴。正常时粪中不出现脂肪滴,>10滴/高倍视野为阳性反应,即存在脂肪吸收不良。
2.粪脂定量检测和脂肪吸收试验
一般采用Van de kamer测定法。试验方法:连续进食标准试餐(含脂肪60~100g/d),连续4~6天,同时测定后3天粪脂含量,取后3天每日平均值或计算脂肪吸收率=(摄入脂肪量 粪脂量)/摄入脂肪量×100%。若粪脂量>6g/24h或脂肪吸收率<95%,提示有脂肪吸收不良。
3. 14 C-甘油三油酸酯呼气试验
三油酸酯是甘油三酯的一种,正常在小肠被胰酶水解,吸收后进一步代谢成CO 2 ,从肺中呼出。脂肪吸收不良患者口服 14 C标记的甘油三油酸酯后,6小时内由肺部呼出的 14 C标记的CO 2 减少。本法对轻度胰源性吸收不良敏感性较差。
(二)蛋白质吸收试验
怀疑蛋白丢失性肠病时,可通过测定血清和24小时收集的粪便中α 1 -抗胰蛋白酶浓度计算α 1 -抗胰蛋白酶清除率(清除率=粪便中浓度×24小时粪便总量/血浓度)。当清除率>25ml/d时,考虑有肠道蛋白丢失。
(三)D-木糖(D-xylose)吸收试验
D-木糖为一种戊糖,口服后不经消化酶分解,直接经空肠黏膜吸收。D-木糖不在体内代谢,几乎全部在小肠近段吸收,最后经肾排出。如肾功能正常,测定尿液中D-木糖排出量可反映小肠吸收功能。
(四)维生素B 12 吸收试验(schilling test)
应用放射性钴标记维生素B 12 可测定回肠下段的吸收功能。肌注维生素B 1 2 1000μg,使体内饱和,同时口服 60 钴标记的维生素B 12 2μg,收集48小时尿液,测定尿液中放射性含量。维生素B 12 吸收正常者,48小时能排出口服放射性钴的5%~40%;维生素B 12 吸收有缺陷者则只有5%以下。
(五) 14 C-甘氨胆酸呼气试验
口服 14 C甘氨胆酸10微居里,正常人绝大部分在回肠吸收,循环至肝脏再经胆管进入小肠,仅极小部分排到结肠而从粪中排出;另一部分则在体内代谢成 14 CO 2 通过肺排出。正常人口服 14 C-甘氨胆酸后4小时内粪内 14 CO 2 的排出量低于总量的1%,24小时排出量<8%。小肠内细菌过度繁殖、回肠病变或外科手术切除者呼气中 14 CO 2 和粪内 14 CO 2 的排出量明显增多,可达正常人的10倍。
(六)H 2 呼气试验
口服的葡萄糖(50~75g,1g/kg)或乳果糖(10g)在进入结肠之前,即被小肠过度生长细菌发酵分解产生氢气,2小时内呼气中氢浓度较对照明显升高。阳性结果可诊断为小肠细菌过度生长。
一、麦胶性肠病
麦胶性肠病(gluten-induced enteropathy)又称乳糜泻(celiac disease,CD),是一种由于摄入麦胶蛋白而引起的慢性小肠疾病,通常以多种营养物质吸收不良、小肠绒毛萎缩和去除饮食中麦胶蛋白后症状改善为特征。目前认为这是一种全球性疾病,我国尚缺乏明确的流行病学资料。该病女性发病多于男性,各年龄段均可发病,发病高峰年龄主要是儿童与青年,但近年来老年人发病率有增高趋势。
【病因和发病机理】
CD的发病主要是由于遗传、麦胶饮食和环境因素相互作用的结果。CD具有遗传易感性,其发病与人类HLAII型基因密切相关,主要的易感基因有两种:HLA-DQ2(DQA1*05-DQB1*02)和 HLA-DQ8(DQA1*03-DQB1*0302)。大约95%的CD患者携带有HLA-DQ2和(或)HLA-DQ8,这些分子的表达对CD的发生是必要的但不是决定性的。部分健康人群中也有易感基因携带者,因此尚不足以将其作为诊断的依据。
CD患者对含麦胶(俗称麸质或面筋)的麦粉食物异常敏感,大麦、小麦、黑麦中的麦胶可被分解为麦胶蛋白(gliadin)和麦谷蛋白(glutinen)。麦胶蛋白是导致乳糜泻的主要抗原蛋白,含有丰富的谷氨酰胺和脯氨酸,脯氨酸与抗原递呈细胞表面的HLA-DQ2和(或)HLA-DQ8分子相互作用,递呈给CD4 + T细胞,从而产生促炎症因子,进而诱导肌动蛋白重新分布,肠上皮细胞骨架改变,导致细胞损伤。
虽然遗传基因和麦胶饮食的摄入对CD的发生发展起了重要作用,但大多数HLA-DQ2/DQ8携带者摄入麦胶后并不发病,事实上仅有1%携带者发病,提示了环境因素的重要性。胃肠道感染、肠道菌群改变、药物和手术也可能诱发本病。此外,有CD家族史、1型糖尿病、自身免疫性甲状腺炎、唐氏综合征、Turner's综合征患者均为本病的高危人群。
【病理】
主要病理变化在小肠,表现为小肠黏膜结构的改变以及炎症细胞的浸润。病变的程度和范围有很大的差异。
目前多采用Marsh分期对麦胶性肠病的肠黏膜损伤情况进行评估。Ⅰ期,上皮内淋巴细胞数量增加;Ⅱ期,除上皮内淋巴细胞增加外,还有隐窝深度的增加,但不伴有绒毛高度下降;Ⅲ期,出现绒毛萎缩,根据绒毛萎缩程度分为Ⅲa期(部分绒毛萎缩)、Ⅲb期(次全绒毛萎缩)、Ⅲc期(全部绒毛萎缩)。
【临床表现】
本病的临床表现实质上是由于营养物质消化吸收障碍,从而导致的营养不良综合征群,临床表现差异很大,症状可不典型,部分患者症状较轻,不易察觉。常见的症状和体征如下:
(一)腹泻、腹痛
80%~97%患者可有腹泻,典型患者呈脂肪泻。
(二)体重减轻、乏力
虽然程度不一,但几乎为必有症状。严重者可呈恶病质。
(三)维生素缺乏及电解质紊乱
(四)水肿、发热及夜尿增多
水肿常见,发热多由于伴发感染所致。发病期夜尿量多于昼尿量,可有IgA肾病、不育症、出血倾向等。
【辅助检查】
(一)血清抗体检查
对于可疑CD患者或高危人群应行血清学抗体筛查,目前已经证实的特异性抗体有抗麦胶蛋白抗体(AGA)、去酰胺麦胶蛋白肽抗体(DGP)、抗平滑肌肌内膜抗体(EMA)以及抗组织谷氨酰胺转移酶抗体(TG2或t TG)。以上抗体均有IgA和IgG两种,IgA抗体敏感性较高,IgG抗体在IgA缺陷者中起重要作用。
2014年英国胃肠病协会(BSG)成人CD诊断和管理指南指出,血清抗TG2抗体是诊断CD的首选方法,EMA是检测CD特异性抗体的参考标准,但是血清学诊断在敏感性和特异性方面的试验数据还有待完善。
(二)内镜及病理活组织检查
内镜及内镜下取材活检取得病理学证据是诊断CD的重要方法之一,活检部位建议取十二指肠远端,至少获得四个相关活检标本包括十二指肠近端的活检,以提高诊断率。由于进食无麸质食物可能会使肠黏膜组织的病理学结果显示为正常,因此建议可疑患者在行内镜检查前仍需保持进食含麦胶食物。
近年来胶囊内镜的应用为小肠疾病提供了有效的无创性检查方法。胶囊内镜可探测到小肠黏膜微小病变,对于不愿接受胃镜或小肠镜检查,或者对胃镜、小肠镜检查有禁忌证的疑似病例,胶囊内镜或可替代,但是胶囊内镜无法进行取材活检,因而不能取得病理组织学依据。
【诊断】
对长期腹泻、体重减轻的患者,应警惕小肠吸收不良的存在。根据粪脂、胃肠X线检查以及小肠吸收试验对吸收不良的性质作出初步判断,并与其他肠道器质性疾病、胰腺疾病等所致的吸收不良病因进行鉴别。血清特异性抗体阳性和小肠黏膜绒毛萎缩是诊断的金标准。对于临床高度怀疑CD而且特异性抗体阳性的患者,建议进行HLA-DQ2和HLA-DQ8检测,加强诊断的力度。对于无症状的个体也可进行HLA检测,以决定是否需进行CD特异性抗体检测。
【治疗】
(一)饮食治疗
严格的终生无麸质饮食是当前对CD的唯一治疗方法。应避免含有小麦、黑麦和大麦的食品。大豆或木薯粉、大米、玉米、荞麦和马铃薯是安全的。仔细阅读预制食品和调味品的标签,尤其注意食品添加剂,例如稳定剂或乳化剂,它们可能含有麸质。蒸馏得来的酒精饮料、醋和葡萄酒不含麸质。然而,应避免饮用啤酒、麦芽酒、淡啤酒和麦芽醋,因为它们通常是由含麸质的谷物制成且未经蒸馏。由于许多乳糜泻患者可有继发性乳糖不耐受,所以其最初可能不能较好地耐受乳制品。因此,对于含有乳糖的食品可能使症状恶化的患者,最初应避免食用此类食品。
对无麸质食物治疗无效的CD称为无反应型,少部分患者可最终发展为难治性CD(指尽管严格遵守无麸质饮食12个月后,绒毛仍持续出现萎缩),这种状况较为罕见,可能是肠相关淋巴瘤的癌前病变。
(二)并发症及支持治疗
CD潜在的并发症可通过严格的无麦胶饮食达到预防目的,相关疾病包括淋巴瘤、骨质疏松、脾功能减退、贫血及微量元素缺乏等。对于骨密度减低或维生素D缺乏的患者,应积极补充钙剂和维生素D。贫血者应及时补充铁剂、叶酸、维生素B 12 等。长期禁食麦胶的患者易继发铁、锌、铜等微量元素不足,因此对那些经饮食结构调整仍不能改善者,建议根据同年龄、同性别的人群水平进行相应补充。
(三)其他
近年来,新的治疗方案不断被提出,包括转基因小麦、治疗性疫苗、谷氨酰胺转移酶抑制剂等,但其疗效和安全性尚缺乏大规模的流行病学调查资料证实。
二、热带口炎性腹泻
热带口炎性腹泻(tropical sprue)又称热带脂肪泻,是一种可能由感染导致的慢性腹泻病,可累及小肠,以营养素(尤其是叶酸和维生素B 12 )吸收不良为特征。见于热带人群(以南美、非洲、印度及东南亚地区最为常见)或近期热带旅行者。任何年龄均可患病。
【病因和发病机制】
由于本病经广谱抗生素治疗有效,现有共识认为可能是由一种或多种病原微生物或寄生虫(蓝氏贾第鞭毛虫)引起的慢性小肠感染,与麦胶饮食无明确关系,但确切的病因和发病机制仍不明确。空肠黏膜活检有时可发现多种可能的致病微生物,但各研究间缺乏一致性。
【病理】
小肠黏膜绒毛变形、不规则,粗大或变平;呈舌形、脊状或扁平、卷曲状。空肠黏膜活组织检查可见腺窝变长,腺窝细胞核肥大,嗜银细胞增多,上皮细胞呈方形或扁平形,杯状细胞减少。上皮细胞酶活力减低。电镜检查见微绒毛不规则,成团且分叉多,微粒体和线粒体均有增加。
【临床表现】
本病除有舌炎、口角炎体征外,尚有乏力、腹痛、腹泻、乏力,大便每日1~2次,或10余次不等,粪便量多,呈糊状,色淡恶臭,油腻泡沫状,约30%患者有脂肪泻及低白蛋白血症,口服蛋白耐量试验显示吸收延缓。50%患者可有葡萄糖耐量异常,90%患者木糖吸收试验显示尿液中D-木糖尿排出量减少。维生素A及维生素B 12 吸收试验亦不正常。
【诊断】
根据发病地区、临床表现、小肠吸收功能减损以及小肠黏膜活检可作出诊断。本病还应与肠阿米巴病、炎症性肠病,麦胶性肠病以及维生素B 12 缺乏症相鉴别。
【治疗】
广谱抗生素和叶酸治疗最为有效。四环素(250mg,口服,每日4次)加叶酸(5mg/d)治疗3~6个月维生素B 12 缺乏者应给予肌肉注射(1000μg/周)。叶酸和维生素B 12 治疗时间一般要维持一年,常与抗生素同时服用。平时饮食宜注意营养均衡,适当补液,纠正电解质平衡失调。腹泻次数过多的患者应及时给予止泻药物治疗。
三、Whipple病
Whipple病又称肠源性脂肪代谢障碍症,是一种由Whipple杆菌引起的慢性、复发性、累及多系统的感染性疾病,病变部位主要位于小肠,其他如淋巴结、关节、肝脏、脾脏、心脏、肺、脑等器官亦可受累。特点为小肠黏膜和肠系膜淋巴结内含有糖蛋白的巨噬细胞浸润,可导致腹痛、腹泻、体重减轻等消化吸收不良综合征。
【病因和发病机理】
现已明确本病由Whipple菌感染所致。Whipple菌为杆状,宽2.0μm,长1.5~2.5μm,在其细胞壁外有三层革兰染色阴性的浆膜样结构,具有特征性。病原菌主要经粪-口途径传播,可侵犯全身各器官。在Whipple病患者中存在持续或暂时性的免疫缺陷,提示免疫反应在本病发生中起一定作用。
【病理】
小肠是最主要的受累部位,主要累及十二指肠第一、二段及空肠,很少累及整个小肠,罕见累及结肠。可累及邻近结构如肠系膜增厚伴肠系膜、腹主动脉周围和腹腔淋巴结病变。光镜下见绒毛呈杵状,近段小肠黏膜内巨噬细胞增多,PAS染色阳性,其中有镰状颗粒。电镜下见其为杆状细菌组成,广泛存在于小肠上皮细胞,淋巴细胞、毛细血管上皮细胞、平滑肌细胞、多形核粒细胞、浆细胞以及肥大细胞内。除小肠黏膜外,心、肺、脾、胰、食管、胃、后腹膜以及全身淋巴结均可累及。
【临床表现】
起病隐匿,症状无特异性,最常见的消化道症状为腹泻、消瘦,20%~30%患者可有肠黏膜隐性出血,5%可出现腹水。部分患者以关节痛为首发症状,通常为游走性,累及大多数关节,但以对称性踝、膝、肩和腕关节最常见。关节痛与胃肠道症状无关。个别患者可无腹泻,仅表现为腹痛和低热。其他症状包括全身淋巴结肿大、脾大等,少数可累及中枢神经系统,出现定位体征和神经精神症状。
【诊断】
长期有关节痛伴有腹泻,或同时有全身淋巴结肿大者,应考虑本病可能。诊断主要依赖小肠镜检查和病理活检。内镜下可见十二指肠及空肠黏膜充血白斑、溃疡及出血。病理活组织检查可见本病特征性的含有糖蛋白(可被PAS染色)的泡沫状巨噬细胞,电子显微镜检查可见巨噬细胞内有小棒状杆菌。若在淋巴结、中枢神经系统、心脏、胃、结肠、肝脏、肌肉、肺等组织中发现PAS染色阳性的巨噬细胞,则提示本病的多系统损害。应注意排除艾滋病(AIDS)、巨球蛋白血症以及全身性网状内皮细胞真菌病。
【治疗】
除对症支持治疗外,主要是抗生素治疗。治疗予长程广谱抗生素:青霉素G 120万U,链霉素1g,每日1次,静脉滴注10~14天,或头孢曲松2g,静脉滴注,每日1次,或美罗培南1g,静脉滴注,每8小时1次,10~14天,以后甲氧苄啶(TMP)160mg和磺胺甲
 唑(SMZ)80mg,每日2次,共1年。可复发,复发大多发生于疗程少于6个月的患者。但前期用头孢曲松或美罗培南者复发率低。PAS阳性巨噬细胞在治疗成功后仍可持续存在,巨噬细胞外致病菌则提示感染持续可能是疾病复发的早期征象。同时伴有中枢系统症状的患者应行脑脊液检查,确诊后治疗持续两年。早期诊断结合有效的治疗或可治愈。症状完全消失需数月至数年,组织学恢复则更慢。
唑(SMZ)80mg,每日2次,共1年。可复发,复发大多发生于疗程少于6个月的患者。但前期用头孢曲松或美罗培南者复发率低。PAS阳性巨噬细胞在治疗成功后仍可持续存在,巨噬细胞外致病菌则提示感染持续可能是疾病复发的早期征象。同时伴有中枢系统症状的患者应行脑脊液检查,确诊后治疗持续两年。早期诊断结合有效的治疗或可治愈。症状完全消失需数月至数年,组织学恢复则更慢。
主要参考文献
1.Kelly CP,Bai JC,Liu E,et al.Advances in diagnosis and management of celiac disease.Gastroenterology,2015,148(6):1175-1186.
2.Ludvigsson JF,Bai JC,Biagi F,et al.Diagnosis and management of adult coeliac disease:guidelines from the British Society of Gastroenterology.Gut,2014,63(8):1210-1228.
3.Marth T.Systematic review:Whipple's disease(Tropheryma whipplei infection)and its unmasking by tumour necrosis factor inhibitors.Aliment Pharmacol Ther,2015,41(8):709-724.
第十二节
原发性小肠肿瘤

沈锡中 董玲
小肠约占全消化道长度的75%,但发生在小肠的肿瘤仅占消化道肿瘤的3%~6%。其中良性肿瘤和恶性肿瘤比例国外为1∶1.9;国内为1∶3.7。小肠肿瘤(small intestinal tumors)发病率低可能与下列因素有关:①液状食糜对小肠黏膜机械性刺激小;②小肠蠕动快,使小肠黏膜接触潜在的致癌物质时间减短;③碱性小肠液减少亚硝胺的合成;④小肠黏膜内高浓度的苯并芘羟基化酶可以降解苯并芘类致癌化合物;⑤小肠黏膜内有大量浆细胞和密集的淋巴细胞,具有强大的免疫功能。其他可能的因素如小肠腔内细菌较少,由细菌参与胆酸的代谢而产生的潜在致癌物浓度低;小肠黏膜干细胞位于隐窝基底层深处,接触致癌物较少等。
【分类】
小肠肿瘤根据其组织发生来源及良、恶性可分类(表15-6-12)。
表15-6-12 原发性小肠肿瘤分类
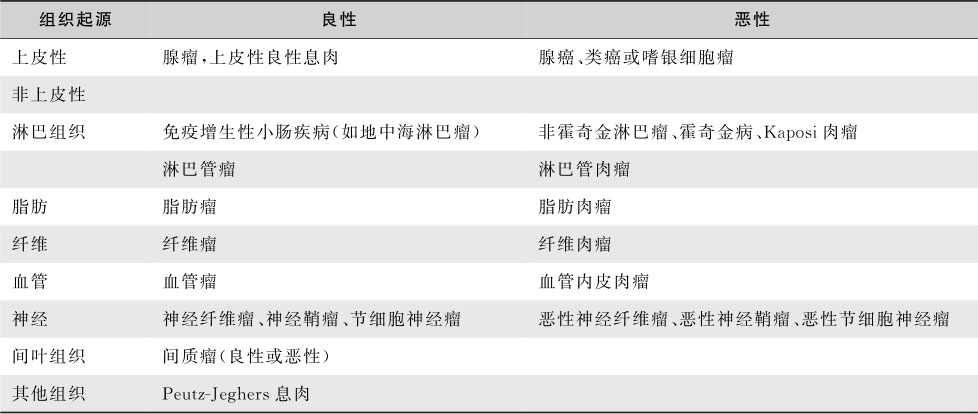
(一)小肠间质瘤
属胃肠间质瘤(gastrointestinal stromal tumors,GIST),起源于胃肠道间叶组织(详见本篇第六章第二节)。
(二)小肠良性肿瘤
小肠良性肿瘤(benign tumors of small intestine)较少见,好发于回肠,空肠其次,十二指肠最少见。良性肿瘤通常根据组织来源分类,分为上皮性肿瘤如腺瘤,最常见,发病年龄多见于40岁左右,男女发病率相近;非上皮性来源的肿瘤有脂肪瘤、血管瘤、神经纤维瘤、纤维瘤和淋巴管瘤等。
1.腺瘤
起源于小肠上皮细胞。瘤体上有分化程度不同的腺泡、腺细胞。腺瘤可以是单个或多个大小不等,也可成串累及整个小肠段。绒毛状腺瘤容易癌变。
2.脂肪瘤
好发于回肠末端,起源于黏膜下层,肿瘤有明显的界限,为一脂肪组织肿块。自黏膜下膨胀性长大而压迫肠腔,也可向浆膜层生长而突出肠壁外。
3.纤维瘤
是较少见的一种界限清楚的小肠肿瘤,由致密的胶原囊及多少不等的成纤维细胞所组成,可累及黏膜下层、肌层或浆膜层。纤维瘤有纤维肌瘤、神经纤维瘤、肌纤维瘤等类型。
4.错构瘤样病变
最常见的是Peutz-Jeghers综合征,有家族史。参见第六章第五节“胃肠道息肉及遗传性疾病”。
5.十二指肠腺黏液囊肿
很少见的一种良性肿瘤,好发于中老年,肿瘤大小不一,可为多个,直径约2cm,囊肿位于十二指肠黏膜下,可有小孔与肠腔相通,分泌出正常的黏液。病理表现为立方形或柱状上皮细胞。
(三)小肠恶性肿瘤
小肠恶性肿瘤(malignant tumor of small intestine)约占胃肠道全部恶性肿瘤的1%~3%。男性多于女性约2倍,在45岁以后患病率上升,60~70岁较多。原发性小肠恶性肿瘤分为四类:癌、类癌、恶性淋巴瘤和肉瘤。其他少见的尚有黑色素瘤、浆细胞瘤等。
1.腺癌
占小肠恶性肿瘤的半数,65%发生于十二指肠,其次为空肠上段。多为高、中分化型腺癌。往往呈息肉样增生或浸润型,并可引起腹块、梗阻、出血或黄疸等4个主要临床症状。除可向局部淋巴结转移外,还可转移到肝、肺、骨和肾上腺。小肠腺癌有时还可同时有两个原发癌灶,另一个癌灶可位于结肠、乳房、胰、肾、子宫颈、直肠或乙状结肠。
2.类癌
占小肠恶性肿瘤的30%~40%,多起源于远端回肠,30%为多灶性。参见第六章第三节“胃肠道神经内分泌肿瘤”。
3.恶性淋巴瘤
原发性小肠恶性淋巴瘤多为非霍奇金淋巴瘤,发生部位以回肠最多,十二指肠少见。主要症状为腹痛、腹块、间歇性黑便,肠段如被广泛浸润或肿瘤压迫,淋巴管阻塞则可出现吸收不良综合征。本病须与肠结核、克罗恩病、继发性小肠恶性肿瘤和小肠α重链病鉴别。
4.其他
如恶性黑色素瘤等。
【临床表现】
小肠肿瘤缺乏特异性临床表现。良性肿瘤多数无症状,部分以急腹症或腹部包块而就诊,过去主要靠手术和尸解意外发现。恶性肿瘤常在中晚期才出现症状,临床表现多样、复杂且无规律,主要临床表现有:
(一)腹痛
腹痛为最常见症状,出现较早,轻重不一,隐匿无规律,呈慢性、间歇性和进行性加重的过程。腹痛可因肠梗阻、肿瘤牵拉、肠管蠕动失调以及瘤体中心坏死继发炎症、溃疡、穿孔引起。腹痛部位与肿瘤位置有关。
(二)腹块
是常见体征之一,约占40%。恶性肿瘤腹部肿块发生率高于良性肿瘤。
(三)消化道出血
约占18%~27.9%。主要是由于肿瘤表面糜烂、溃疡、坏死所致,以腺癌最常见,间质瘤和淋巴瘤次之,血管瘤也可发生。
(四)肠梗阻
约占21.4%~31.5%,多为不完全性肠梗阻,呕吐,腹胀症状不十分明显。若肿瘤带动肠管扭转,可造成绞窄性肠梗阻。
(五)肠穿孔及腹膜炎
穿孔发生率为8.4%,其中恶性肿瘤发生穿孔者12%~19.4%,良性肿瘤为2%。穿孔的主要原因是肠壁溃疡、坏死、感染。可导致腹膜炎,死亡率高。除上述临床表现外,小肠肿瘤常可出现腹泻、发热、腹胀、乏力、贫血、消瘦等症状。恶性肿瘤广泛浸润可压迫淋巴管引起乳糜泻、小肠吸收不良、低蛋白血症、水肿、恶病质、腹水及远处转移等症状。
【诊断】
小肠肿瘤病灶隐匿且症状非特异,常被延误诊断。对于常规胃肠镜检查阴性的腹痛、消化道出血和肠梗阻的患者,应考虑是否存在小肠肿瘤的可能。不明原因的营养不良、贫血、体重下降也要考虑该病可能。目前常用的小肠肿瘤诊断方法有小肠CT/MRI成像(CT/MR enterography)、小肠镜、胶囊内镜、选择性血管造影术、腹腔镜、术中内镜等。小肠CT成像,具有无创伤性、费用较低、对病灶空间分辨率高等优点,可作为小肠肿瘤诊断的首选方法;小肠MRI成像对小肠肿瘤性质判断方面优于CT。如无梗阻存在,胶囊内镜是可以选择的诊断手段。小肠镜对小肠肿瘤的诊断具有明确的价值,随着气囊辅助小肠镜和螺旋式小肠镜的发展,理论上能观察到整个小肠,且能进行病理活检。 18-F-FDG PET/CT可应用于GIST、淋巴瘤、小肠类癌的病情评估。选择性肠系膜上动脉造影对血管瘤、血管丰富的间质瘤、腺癌等诊断意义较大。如造影时出血量≥0.5~1ml/min,可显示造影剂从血管内溢出,对病灶部位的判断有一定的帮助。诊断流程图如图15-6-1所示。
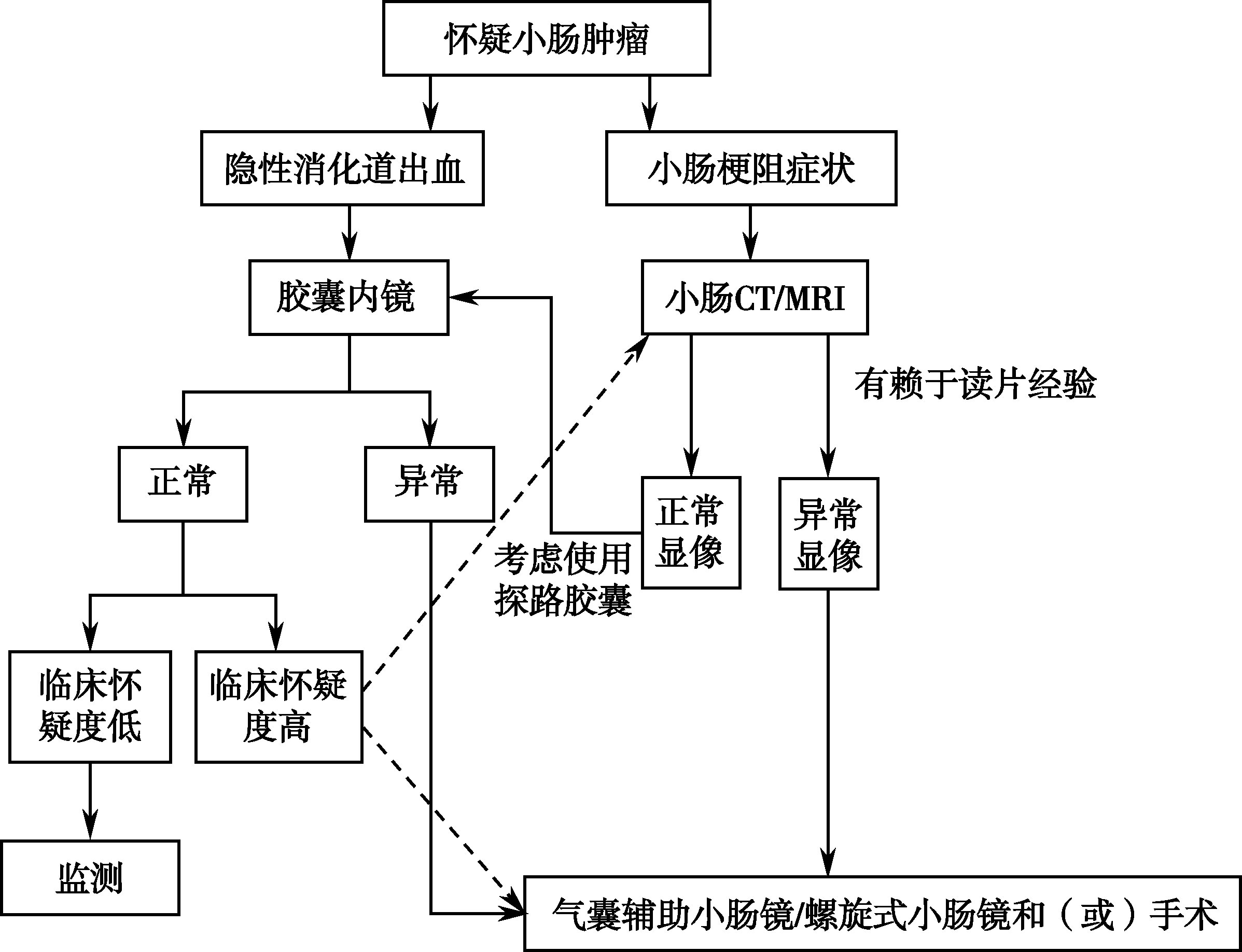
图15-6-1 小肠肿瘤诊断流程
【治疗】
小肠肿瘤治疗原则以手术切除为首选,良性肿瘤切除率可达100%。对小肠恶性肿瘤,应尽可能行根治手术。腺癌恶性程度高,其手术切除后的5年生存率也仅15%~35%。对可疑小肠肿瘤的患者手术探查是必要的,并要与回肠末端多见的克罗恩病相区分。小肠恶性肿瘤对放疗不敏感,且正常小肠黏膜放射反应较大,所以除淋巴瘤和一些转移性肿瘤外,一般不主张放疗。小肠恶性肿瘤化疗有效率也仅50%,建议采用联合化疗方案。
主要参考文献
1.Charles DB,Douglas OF.Neoplasms of the small and large intestine.In:Lee Goldman,Andrew I Schafer ed.Goldman's Cecil Medicine 25th ed.USA.Elsevier Saunders,2015,1320-1322.
2.Williamson JM,Williamson RC.Small bowell tumors:pathology and management.J Med Assoc Thai,2014,97(1):126-137.
第十三节
大肠癌

陈世耀
大肠癌(colorectal carcinoma,CRC)包括结肠癌和直肠癌,是常见的消化道恶性肿瘤。我国大肠癌发病率升高趋势明显,尤其城市。且发病年龄以40~50岁居多,发病中位年龄约为45岁。男性大肠癌的发病率高于女性,约为1.6∶1。
【病因】
(一)生活方式
研究认为,吸烟、食用红肉和加工肉类、饮酒、低运动量以及肥胖/高体质指数是大肠癌发病的危险因素。
(二)遗传因素
遗传因素在大肠癌发病中具有相当重要的角色。约20%左右的大肠癌归因危险度与遗传背景有关。近亲中有患大肠癌者,其本身患此病的危险度增加,更多亲属有此病的危险度更大。目前已有两种遗传性易患大肠癌的综合征被确定:第一为家族性腺瘤性息肉病(familial adenomatous polyposis,FAP);第二为遗传性非息肉病性大肠癌(hereditary nonpolyposis colorectal cancer,HNPCC)。
大肠癌的发生发展是一个多阶段的、涉及多基因改变的逐渐积累的复杂过程,即由正常上皮转化为上皮过度增生、腺瘤的形成,腺瘤伴不典型增生,并演进至癌及癌的浸润与转移,先后发生了许多癌基因的激活、错配修复基因( MMR )的突变以及抑癌基因的失活与缺如。最常见的有: APC 、 MCC 基因的突变, MMR 基因失活, K-ras 基因突变,抑癌基因 DCC 的缺失,抑癌基因 p 53的突变与缺失,以及 nm23 改变等(图15-6-2)。
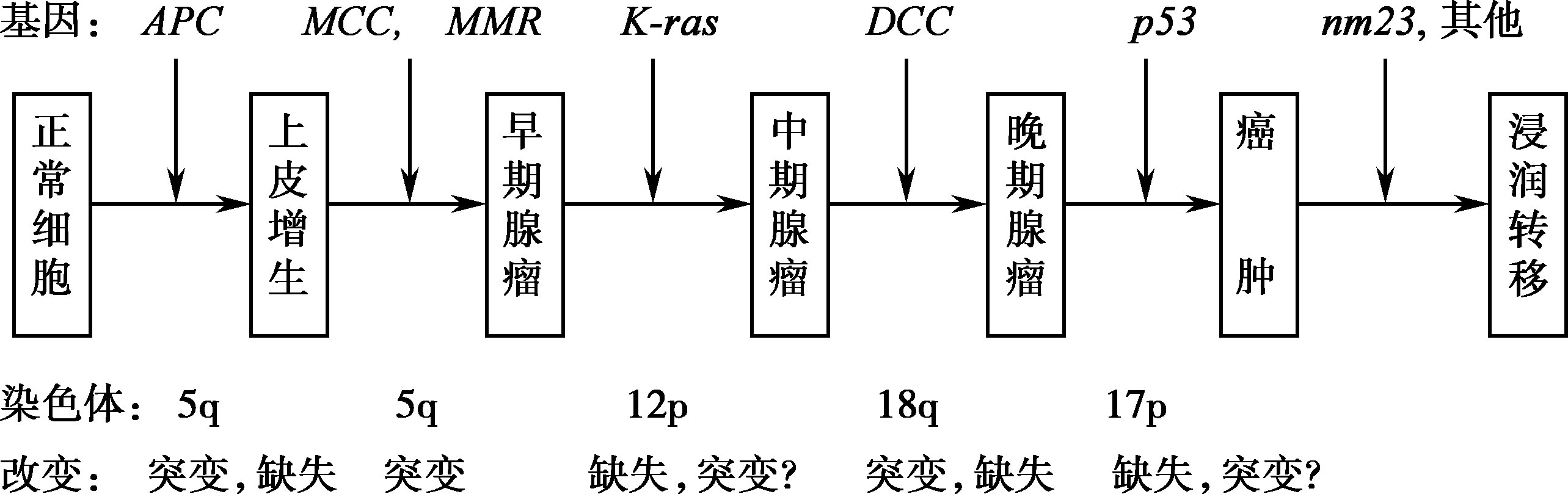
图15-6-2 大肠癌发生发展的分子遗传学模式图
(三)大肠腺瘤
从腺瘤演变为大肠癌大约需要5年以上,平均10~15年,但也可终生不变。根据腺瘤中绒毛状成分所占比例不同,可分为管状腺瘤(绒毛成分在20%以下)、混合性腺瘤(绒毛成分占20%~80%)和绒毛状腺瘤(绒毛成分在80%以上,又称乳头状腺瘤)。临床发现的腺瘤中管状腺瘤约占70%,混合性腺瘤和绒毛状腺瘤分别占10%与20%。管状腺瘤、混合性腺瘤及绒毛状腺瘤的癌变率分别为5%~9%、20%~30%及40%~45%。
(四)大肠慢性炎症
炎症性肠病(如溃疡型结肠炎、克罗恩病)患者的结直肠癌风险升高。慢性非特异性溃疡性结肠炎,特别是合并有原发性硬化性胆管炎的患者大肠癌发生率比正常人高出5~10倍,病程愈长癌变率愈高。血吸虫病、慢性细菌性痢疾、慢性阿米巴肠病以及克罗恩病发生大肠癌均比同年龄对照人群高。
(五)其他因素
亚硝胺类化合物中致癌物也可能是大肠癌的致病因素之一。宫颈癌放射治疗后患直肠癌的风险提高,放射后15年危险性开始上升。胆囊切除术后的患者大肠癌发病率显著高于正常人群,而且多见于近端结肠。原发性与获得性免疫缺陷症也可能与本病发生有关。
【病理】
大肠癌绝大部分为单个,少数病例同时或先后有一个以上癌肿发生,即多原发大肠癌。据文献资料,2%~9%的大肠癌患者为多原发大肠癌。大肠癌最好发部位是直肠与乙状结肠,约占75%~80%,其次为盲肠及升结肠,再其次为结肠肝曲、降结肠、横结肠及结肠脾曲。大肠癌的大体形态随病期而不同,可分为早期大肠癌和进展期大肠癌:
(一)早期大肠癌
早期大肠癌是指原发灶肿瘤限于黏膜下层者(pT1)。其中限于黏膜层者为“黏膜内癌”。由于黏膜层中没有淋巴管,很少发生淋巴结转移。癌限于黏膜下层但未侵及肠壁肌层者为“黏膜下层癌”,也属早期大肠癌,但因黏膜下层内有丰富的脉管,因此部分黏膜下层癌可发生淋巴结转移或血道转移。早期大肠癌大体分类可分为3型:①息肉隆起型(Ⅰ型)又可进一步分为有蒂型(1p)、广基型(1s)两个亚型,此型中多数为黏膜内癌;②扁平隆起型(Ⅱ)肿瘤如分币状隆起于黏膜表面,此型中多数为黏膜下层癌;③扁平隆起伴溃疡型(Ⅲ型)肿瘤如小盘状,边缘隆起,中心凹陷,此型均为黏膜下层癌。
(二)进展期大肠癌
当癌浸润已超越黏膜下层而达肠壁肌层或更深层时归于进展期大肠癌。其大体分型可分为4型,其中以隆起型和溃疡型多见,胶样型少见:
(1)隆起型:
癌体大,质软,又称髓样癌,肿瘤的主体向肠腔内突出,呈结节状、息肉状或菜花样隆起,境界清楚,有蒂或广基,可发生于结肠任何部位,但多发于右半结肠和直肠壶腹部,特别是盲肠。
(2)溃疡型:
癌体一般较小,早期形成溃疡,溃疡底可深达肌层,穿透肠壁侵入邻近器官和组织,好发于直肠与远段结肠。
(3)浸润型:
肿瘤向肠壁各层弥漫浸润,伴纤维组织异常增生,肠壁增厚,形成环形狭窄,易引起肠梗阻,好发于直肠、乙状结肠及降结肠。
(4)胶样型:
癌体较大易溃烂,外观及切面均呈半透明胶冻状,好发于右侧结肠及直肠。
组织病理学类型有腺癌(管状腺癌、乳头状腺癌、黏液腺癌、印戒细胞癌)、未分化癌、腺鳞癌、鳞状细胞癌、小细胞癌和类癌。临床上以管状腺癌最多见,约占67%,鳞癌少见,见于直肠与肛管周围。
大肠癌转移途径有:①直接浸润:癌肿浸润浆膜层而累及附近组织或器官,并可能发生直肠-膀胱瘘和胃-结肠瘘;②淋巴转移:大肠癌如侵犯黏膜肌层,就有淋巴转移的危险;③血行转移:大肠癌发生血行转移的情况相当常见。癌肿侵犯血管(主要是静脉)后,癌栓易通过门静脉转移到肝脏,也可经体循环到肺、脑、肾、肾上腺、骨骼等处;④癌肿浸润大肠浆膜层时,脱落癌细胞可种植到所接触的组织,如直肠膀胱或直肠子宫陷窝,或手术肠吻合口等处。广泛种植时可出现癌性腹水。
【分期】
TNM分期参照美国癌症联合委员会(AJCC)/国际抗癌联盟(UICC)关于结直肠癌TNM分期系统(2010年第七版),以及中国结直肠肿瘤筛查、早诊早治和综合预防共识意见(2012年)。
【临床表现】
早期大肠癌常无症状,随着癌肿的增大或并发症的发生才出现症状。主要症状有:①排便习惯与粪便性状改变:常为最早出现的症状,多表现为排便次数增加,腹泻,便秘,或腹泻与便秘交替;有黏液便、血便或脓血便,里急后重,粪便变细;②腹痛:由于癌肿糜烂、继发感染刺激肠道,表现为定位不确切的持续隐痛,可仅为腹部不适或腹胀感;③腹部肿块:大肠癌腹部肿块以右腹多见,肿块质硬,结节状;④肠梗阻症状:一般为大肠癌晚期症状,多表现为低位不完全性肠梗阻,可出现腹胀、腹痛和便秘。完全梗阻时,症状加剧;⑤全身症状:由于慢性失血、癌肿溃烂、感染、毒素吸收等,患者可出现贫血、消瘦、乏力、低热等;⑥肿瘤外侵、转移的症状:肿瘤扩散出肠壁在盆腔广泛浸润时,可引起腰骶部酸痛、坠胀感,当浸润腰骶神经丛时常有腰骶尾部持续性疼痛。肿瘤通过血道、淋巴道及种植转移时,可出现肝、肺、骨转移,左锁骨上、腹股沟淋巴结转移,直肠前凹结节及癌性腹水。晚期可出现黄疸、水肿等。据国内资料,大肠癌患者的首诊主诉症状以便血最多(48.6%),尤其直肠癌患者,其次为腹痛(21.8%),以结肠癌患者为多。
(一)右侧结肠癌
右侧结肠腔径较大,以吸收功能为主,肠腔内粪汁稀薄。故右侧结肠癌时,可有腹泻、便秘,腹泻与便秘交替、腹胀、腹痛、腹部压痛、腹块、低热及进行性贫血。晚期可有肠穿孔、局限性脓肿等并发症。以肝内多发转移为首发表现也不在少数。
(二)左侧结肠癌
由于左侧结肠腔不如右侧结肠宽大,乙状结肠腔狭小并与直肠形成锐角,且粪便在左侧结肠已形成,因此左侧结肠癌时容易发生慢性进行性肠梗阻。由于梗阻多在乙状结肠下段,所以呕吐较轻或缺如,而腹胀、腹痛及肠型明显。
(三)直肠癌
主要表现为大便次数增多,粪便变细,带黏液或血液,伴有里急后重或排便不净感。当癌肿蔓延至直肠周围而侵犯骶丛神经,可出现剧痛。如癌肿累及前列腺或膀胱,则可出现尿频、尿急、尿痛、排尿不畅和血尿等症状,并可形成通向膀胱或女性生殖器的瘘管。
(四)肛管癌
主要表现为便血及疼痛,疼痛于排便时加剧。当癌侵犯肛门括约肌时,可有大便失禁。肛管癌可转移至腹股沟淋巴结。
【诊断】
大肠癌除早期可无症状之外,绝大多数均有不同程度的症状存在。详细询问病史、认真体格检查辅以实验室、内镜和X线检查,确诊一般并无困难。大肠癌检查手段包括:
(一)直肠指诊
直肠指诊简便易行,一般可发现距肛门7~8cm以内的中下段直肠肿瘤。是早期发现直肠癌的重要检查方法,应引起临床重视。
(二)内镜检查
多采用全结肠镜检查,可观察全部结肠,直达回盲部,并对可疑病变进行组织学检查,有利于早期及微小结肠癌的发现。对内镜检查发现的病灶,除需要活检确定性质之外,可采用病灶上下缘金属夹定位,有利进一步治疗。
(三)钡灌肠X线检查
应用气钡双重造影技术,可清楚显示黏膜破坏,肠壁僵硬、结肠充盈缺损、肠腔狭窄等病变,现多为肠镜检查替代。但腹部平片检查对判断肠梗阻的作用不可忽略。
(四)腔内超声、CT、MRI
结直肠腔内超声扫描可清晰显示肿块范围大小,深度及周围组织情况,可分辨肠壁各层的微细结构。可作为中低位直肠癌分期诊断依据。CT及MRI检查对了解肿瘤肠管外浸润程度以及有无淋巴结或远处转移更有意义。CT检查提供结直肠恶性肿瘤的分期;发现复发肿瘤;评价肿瘤对各种治疗的反应。MRI检查提供直肠癌的术前分期;结直肠癌肝转移的评价;腹膜以及肝被膜下病灶。
(五)大便隐血检查(FOBT)
对本病的诊断虽无特异性,但方法简便易行,可作为大规模普查时的初筛手段,或提供早期诊断的线索。
(六)血清癌胚抗原(CEA)测定
CEA非结肠癌所特有,但多次检查观察其动态变化,对大肠癌的预后估计及监测术后复发有一定的意义。
(七)PET/CT
不推荐常规使用,但对于常规检查无法明确的转移复发病灶可作为有效地辅助检查。
在鉴别诊断上,右侧结肠癌应与阑尾脓肿、肠结核、血吸虫病肉芽肿、肠阿米巴病以及克罗恩病相鉴别。左侧结肠癌的鉴别诊断包括血吸虫肠病、慢性细菌性痢疾、溃疡性结肠炎、结肠息肉病、结肠憩室炎等。直肠癌应与子宫颈癌、骨盆底部转移癌、粪块嵌塞等相区别。
【预防】
对高危人群进行结肠镜筛查是早期诊断的重要措施。高危人群可以包括定期粪隐血试验阳性人群。预防措施包括改变生活方式如戒烟、保持体质指数、锻炼身体增加纤维膳食,积极防治癌前病变如炎症性肠病、处理结肠及直肠腺瘤和息肉病。化学药物阿司匹林、塞来昔布等尚未常规推荐。
【治疗】
(一)手术治疗
根治手术,包括癌肿、足够的两端肠段及区域淋巴结清扫。区域淋巴结清扫必须包括肠旁、中间和系膜根部淋巴结三站。
1.结肠癌
结肠具有宽长系膜,易将整个相关的系膜淋巴引流系统全部切除,预后较直肠癌为好。手术方法和范围的选择取决于肿瘤部位、拟切除肠段及其动脉血供范围和淋巴引流范围。腹腔镜下结肠切除术已经被列为治疗结肠癌的一种手术方式。对于结肠癌手术淋巴结的清扫是非常重要的,至少应该检测到12枚淋巴结。对于pN0患者,若初始检查不能找到12枚淋巴结,推荐病理医师重新解剖标本。被判定为N0但是送检淋巴结少于12枚的患者分期是未达到标准的,视为高危人群。
2.直肠癌
直肠癌原发灶的手术治疗方法众多,主要取决于肿瘤的部位以及肿瘤的广泛程度。这些手术方法包括局部切除法,如经肛门局部切除和经肛门显微手术(TEM);经腹手术方法,包括低位前切术(LAR),行结肠-肛管吻合的全直肠系膜切除术(TME)或腹会阴联合切除术(APR)。术前新辅助放化疗可能使肿瘤体积缩小,让保肛手术成为可能。“全直肠系膜切除(total mesorectal excision,TME)”手术可使中下段直肠癌术后复发率由传统的12%~20%降至4%左右。
3.肝转移的处理
确诊大肠癌时,15%~25%已有肝转移。在大肠癌切除后的患者随访中另有20%~30%将发生肝转移。如果大肠癌患者除肝脏转移外无其他远处转移,原发灶又能作根治性切除者,则应对肝脏转移灶作积极的治疗。判定肝转移瘤是否适合手术在于保留正常肝储备功能的基础上,是否能获得阴性手术切缘。
对于肝转移灶无法根治手术的患者选择以肝脏为导向的治疗方法作为补充或替代。主要方法如下:肝脏动脉灌注(HAI);经动脉的化疗栓塞(TACE);肿瘤消融术。消融技术包括射频消融(RFA)、微波消融、冷冻消融、经皮无水酒精注射和电凝固技术。同时以肝脏为导向的放疗方法包括微球体动脉放射栓塞术以及适形(立体)外照射放疗。
4.并发症的处理
结直肠癌发生完全性肠梗阻占8%~23%,患者预后一般较差,死亡率及并发症发生率也较高。梗阻时,应当在进行胃肠减压、纠正水和电解质紊乱以及酸碱失衡等准备后,早期施行手术。右侧结肠癌,可行右半结肠切除一期回肠结肠吻合术。如患者情况不许可,则先作盲肠造口解除梗阻,二期手术行根治性切除。如肿瘤已不能切除,可切断末端回肠,行近切端回肠横结肠端侧吻合,远切端回肠断端造口。左侧结肠癌并发急性肠便阻时,一般应在梗阻部位的近侧作横结肠造口,在肠道充分准备的条件下,再二期手术行根治性切除。对肿瘤已不能切除者,则行姑息性结肠造口。
近年来内镜技术得到肯定和广泛应用,结肠梗阻尤其左半结肠梗阻的患者,可在灌肠等准备后经内镜行结肠支架放置术或结肠引流,解除梗阻,减少肠壁水肿,在梗阻解除1~2周后再行Ⅰ期肿块切除+肠吻合术。
结直肠癌穿孔的手术和围术期的并发症发生率和死亡率均较高,5年生存率低于10%。可能与穿孔后结肠癌细胞在腹腔种植有关。手术原则与结直肠癌性梗阻相同。
(二)化学药物治疗
临床诊断的大肠癌患者中,20%~30%已属晚期,手术已无法根治,必须考虑予以化疗。化疗药物为5Fu/LV、伊立替康、奥沙利铂、卡培他滨和靶向药物,包括西妥昔单抗(推荐用于全RAS基因野生型患者)、贝伐珠单抗、帕尼单抗、瑞戈非尼及阿柏西普。治疗的选择主要取决于治疗目标、既往治疗的类型和时限以及治疗方案构成中各种药物不同的毒不良反应谱。在考虑不同给药方案对具体患者的疗效和安全性时,不但要考虑药物构成,还要考虑药物的剂量、给药计划和途径,以及外科根治的潜在性和患者的身体状况。对于适合接受高强度治疗的转移性患者(即,对该方案能够良好耐受,而获得的高治疗反应性可能具有潜在的临床获益),推荐5个化疗方案作为初始治疗的选择:FOLFOX(即mFOLFOX6),FOLFIRI,CapeOX,输注5-FU/LV或卡培他滨,或FOLFOXIRI。
术后辅助化疗选择根据分期而定。Ⅰ期患者不需要辅助化疗。Ⅱ期患者是否需要辅助化疗存在争议。存在高危因素的Ⅱ期大肠癌患者可以从辅助化疗中获益。高危Ⅱ期患者定义为:T4、组织学分化差(3/4级)、脉管浸润、神经浸润、肠梗阻、肿瘤部位穿孔、切缘阳性或情况不明、切缘安全距离不足、送检淋巴结不足12枚。证据表明微卫星不稳定性(MSI)是Ⅱ期结肠癌预后良好的一个标志物,也是患者不能从氟尿嘧啶单药辅助化疗获益的疗效预测指标。对于存在临床高危因素且非MSI-H的Ⅱ期肠癌患者可选择的化疗方案包括5Fu/LV、卡培他滨、FOLFOX或卡培他滨/奥沙利铂(Cape Ox)或FLOX方案。Ⅲ期患者根治手术后进行6个月的辅助化疗。方案可选用:FOLFOX或CapeOX。对于不能使用奥沙利铂的患者可选择卡培他滨或5Fu/LV。含伊立替康的方案不适合作为术后辅助治疗方案。不推荐贝伐珠单抗、西妥昔单抗作为辅助治疗选择。
T 3~4 或N 1~2 据肛缘≤12cm的直肠癌,推荐术前新辅助放化疗,如术前未行新辅助放疗,建议术后辅助放化疗,其中同步化疗方案推荐氟尿嘧啶类单药。术中或术后区域性缓释化疗与腹腔热灌注化疗目前不常规推荐。
(三)放射治疗
直肠癌放疗或放化疗为辅助治疗和姑息治疗,适应证为肿瘤局部区域复发和(或)远处转移。对于某些不能耐受手术或保肛意愿强烈的患者,可以尝试根治性放疗或放化疗。
(四)内镜下治疗
限于黏膜层的早期大肠癌,腺瘤癌变,采用内镜下黏膜切除术(EMR)或者黏膜剥离术(ESD)可将癌变腺瘤完整切除;直肠类癌局限病变也可以考虑内镜下治疗。在不能进行手术治疗的晚期病例,可通过内镜放置金属支架预防或者解除肠腔狭窄和梗阻。
(五)其他治疗
包括:基因治疗、导向治疗、免疫治疗、中医中药治疗,均作为辅助疗法。
【预后】
大肠癌预后与其生物学行为有关。结肠癌根治术后5年生存率达到60%以上,直肠癌5年生存率也达到50%以上。年龄小、浸润型和胶样型、分化程度低的大肠癌预后较差。结肠癌的预后比直肠癌好,直肠癌位置越低,局部复发率越高。除针对肿瘤治疗外,积极处理并发症可提高患者生存质量和延长患者的寿命。
主要参考文献
1.中华人民共和国卫生和计划生育委员会医政医管局.中国结直肠癌诊疗规范(2015版).中华消化外科杂志,2015,14(10):783-799.
2.中华医学会消化内镜学分会消化系早癌内镜诊断与治疗协会.中国早期结直肠癌及癌前病变筛查与诊治共识意见(2014年11月·重庆).中华内科杂志,2015,54(4):375-389.
3.Edge DR,Compton CC,Fritz AG,et al.AJCC Cancer Staging Manual.7thed.New York:Springer,2010.
Dan LL,Strum WB.Colorectal Adenomas.New England Journal of Medicine,2016,374(11):1065-1075.
第十四节
肠道血管性疾病

丁伟群 陆玮
肠道的动脉血供主要来自腹腔动脉、肠系膜上动脉(SMA)及肠系膜下动脉(IMA)。SMA除供应胰腺、十二指肠外,还供应全部小肠、右半结肠的血液,IMA主要供应左半结肠血液。肠道静脉分布大致与相应动脉并行,最后流入门静脉。直肠肛管的血供主要来自直肠上、下动脉及骶中动脉。
侧支血管因人而异,包括肠系膜弯曲动脉、位于肠系膜基底部的Riolan弓和沿着肠系膜边缘的Drummond边缘动脉(均连接SMA和IMA)、胰十二指肠弓和Barkow弓、Buhler弓(均连接腹腔动脉及SMA)。这些侧支在肠系膜局限性缺血时可迅速扩张。低动脉血流状态下,分水岭区域如脾区为距离动脉血供最远区域,最易缺血。与之相反,当大动脉血管如IMA突然闭塞时由于有来自SMA的侧支循环,脾区较不容易累及。
肠道血供约占心输出量的10%,餐后可上升至25%。一般情况下,肠系膜毛细血管20%开放就能维持正常氧供。肠系膜缺血时,肠道血流受交感神经系统和全身(血管紧张素Ⅱ、加压素)或局部(前列腺素、白三烯)体液因子调节,可自行下调正常血供的75%长达12小时。通过新开放的侧支血管及提高氧合的解离有助于代偿。随缺血程度加剧,广泛的肠系膜血管收缩将不可逆,即使纠正了潜在疾病,低氧及再灌注损伤、氧自由基产生、内皮合成一氧化氮减少、细胞炎症反应上调可导致微血管及终末器官的损害。起初,终末器官的损害累及黏膜,但损害可迅速进展至透壁性坏死(坏疽)。一些缺血肠段可通过纤维化而愈合(狭窄)。
肠缺血临床表现取决于受累肠管范围、程度、持续时间、吻合支丰富程度与可能形成的侧支循环状况等。
一、慢性肠系膜缺血
慢性肠系膜缺血(chronic mesenteric ischemia,CMI)又称腹(肠)绞痛,内脏动脉粥样硬化狭窄是导致绝大多数CMI的病因。
【病因】
主要是高龄及能引起粥样硬化的各种高危因素。血管炎及主动脉动脉瘤偶尔也可成为慢性肠系膜缺血的病因。粥样硬化狭窄通常累及供应肠道血供的2支或所有3支内脏动脉的起始部。
【临床表现】
临床表现为发作性的缺血性腹痛。腹痛常位于上腹部或中腹部,一般在餐后15~30分钟发作,持续1~3小时。由于惧怕进食后腹痛,因此进食减少伴体重明显减轻。恶心、呕吐、腹胀、腹泻、便秘也会出现。一些患者表现吸收不良伴脂肪泻,或不能解释的胃十二指肠溃疡,小肠活检发现微绒毛萎缩,非特异性上皮细胞变扁平。腹部柔软,疼痛发作期亦无压痛。腹部检查可能听到收缩期杂音。
【诊断】
多普勒彩超发现病灶常在血管近端,血流通过明显狭窄区域时流速会增快。应用多普勒超声或MRI检测餐后腹腔动脉和肠系膜上动脉血流,本病不增加。气囊张力测定法可检测到肠缺血者肠壁内pH减低。动脉造影可见2支或3支腹主动脉大分支有明显狭窄及侧支循环证据,确认解剖学发现与症状是否相吻合非常重要。
【治疗】
内科治疗包括扩血管药物,如钙通道阻滞剂(硝苯地平等)对部分患者有效。外科手术包括旁路术,动脉内膜切除术和血管重建术等。气囊导管扩张术和(或)放置支撑管提供了非手术治疗的可能性。
二、急性肠系膜缺血
急性肠系膜缺血(acute mesenteric ischemia,AMI)不常见,随着人口老龄化及心血管疾病的增加,本病发病率也在增长。
急性肠系膜缺血中肠系膜上动脉栓塞(SMAE)最常见(占40%~50%),其他依次为非闭塞性肠系膜缺血(NOMI)(占25%)、肠系膜上动脉血栓形成(SMAT)(占10%)、肠系膜静脉血栓形成(MVT)(占10%)、局灶性节段性小肠缺血(FSI)占5%左右。
【病因】
SMAE栓子一般来自心脏的附壁血栓,心内膜炎患者的瓣膜赘生物或血栓、动脉粥样硬化斑块,偶见细菌栓子。SMAT主要的病变基础为动脉硬化,其他尚有主动脉瘤、血栓闭塞性脉管炎、结节性动脉周围炎和风湿性血管炎等。低血容量或心排血量突然降低、心律不齐、血管收缩剂或过量利尿剂为常见的诱因。NOMI起病多于低血容量性休克、充血性心衰、严重心律失常致收缩压降低或血管痉挛引起小肠动脉血流不足。MVT常伴有高凝状态(如抗凝血酶Ⅲ、蛋白C和S缺乏及真性红细胞增多症、癌症)、肠系膜上静脉损伤(外伤、手术、放疗、门-腔静脉分流术后)、腹腔感染和长期服用避孕药等。近半数患者有周围静脉血栓性炎症病史。FSI一般由粥样硬化性栓子、绞窄疝、血管炎、腹部钝性外伤、放射及口服避孕药等引起。
【临床表现】
(一)肠系膜上动脉栓塞(superior mesenteric artery embolus,SMAE)
SMA主干口径较大,与腹主动脉呈倾斜夹角,栓子易于进入。大约15%栓子位于SMA开口处,50%左右在结肠中动脉开口处(SMA最大的分支)。1/3患者以往有栓塞史。
本病起病急,早期有脐周或上腹部突然发作的剧痛,但腹软,甚至无压痛,“症征不符”是其典型临床表现。6~12小时后,肠肌麻痹、持续性腹痛,肠鸣音减弱,肠黏膜可发生坏死或溃疡,导致便血或呕咖啡样物。此时如解除血管阻塞,肠缺血尚可恢复。12小时后如出现腹膜刺激征或腹块,肠鸣音消失,发热、脉速等,提示病变已不可逆。如栓塞发生在分支,侧支循环较好,急性发病后可自行缓解。
(二)肠系膜上动脉血栓形成(superior mesenteric ar-tery thrombosis,SMAT)
血栓形成最常见于SMA开口处附近。由于发病前SMA已有病变,进展较慢,有一定程度侧支循环形成。临床上可分为慢性、亚急性和急性三种类型。慢性者常表现为餐后腹痛、体重下降。急性者临床表现可与SMAE相类似,但腹痛程度没有SMAE剧烈。近1/3的患者在急性发作前有慢性肠系膜缺血的症状及病史。如果SMA或重要的侧支血管阻塞,则缺血或梗死的部位较广,病变范围可从十二指肠到横结肠。
(三)非闭塞性肠系膜缺血(non-occlusive mesenteric ischemia,NOMI)
肠系膜血管血流量下降,血管床呈收缩状态。如时间稍长,即使原发因素已被解除,但系膜血管仍持续收缩。临床上有腹痛、胃肠道排空症状。少数患者无腹痛,但有明显腹胀。如出现严重腹痛,呕咖啡样物或便血,尤其有腹膜刺激征时,常提示病变已进入肠梗死阶段,甚至已有穿孔或腹膜炎。
(四)肠系膜静脉血栓形成(mesenteric venous thrombosis,MVT)
起病有急性、亚急性和慢性之分。急性MVT发病与SMAT相似,但症状持续时间更长。亚急性MVT常有腹部不适、厌食、大便习惯改变等先驱症状,最常见的临床表现是发热、腹胀、大便隐血试验阳性。随病情进展而腹痛加剧(下腹部最常见)、呕吐、血便、呕咖啡样物,腹膜刺激征甚至循环衰竭。腹腔穿刺如抽到血性腹水,提示肠管已有坏死。慢性MVT多数无症状,如门静脉被累及,则可见门脉高压征象。
(五)局灶性节段性小肠缺血(focal segmental ischemia,FSI)
临床表现多样,因有丰富的侧支循环,不会引起全层坏死,无致命性并发症。有三种临床表现:①急性小肠炎酷似阑尾炎;②慢性小肠炎酷似克罗恩病;③肠梗阻,常伴细菌过度生长和盲袢综合征。
【诊断】
(一)血管造影
选择性肠系膜血管造影是AMI诊断的金标准,不仅可诊断AMI及其病因,还可经导管应用血管扩张剂以松弛收缩的内脏血管,如是闭塞性疾病,还有助于制定血管再通方案。闭塞性病变的血管造影可见充盈缺损。NOMI造影显示动脉本身无阻塞,但其主干或其分支有普遍或节段性痉挛,肠壁内血管充盈不佳为其特征性表现。
(二)CT/CT血管成像和MR/MR血管成像
1.常规CT检查
对AMI,特别是MVT有一定诊断价值,但是早期表现无特异性,而坏死和坏疽则是后期表现,也可发现节段性肠壁增厚、黏膜下出血、肠系膜合股、肠系膜静脉血栓形成、肠积气、门静脉气体等表现。
2.CT血管成像(CTA)
可能发现3支主要分支中的栓子或血栓,并有可能替代动脉造影作为诊断AMI首选方法。
3.磁共振成像(MRI)
主要显示动脉主干病变。
4.MR血管成像(MRA)
是另一种诊断肠系膜缺血的新方法。MRA与CTA或动脉造影相比较,其主要优点是没有肾毒性。然而对继发于低血容量NOMI,或远端栓塞性疾病的诊断价值有限。
(三)腹部平片
腹部平片对AMI的敏感性很低(30%),而且是非特异的,其主要目的是除外其他腹痛原因。
(四)多普勒超声
对肠系膜缺血的诊断特异性强,但它的敏感性受以下因素所限制:①只能显示主要内脏血管近端;②无法诊断NOMI。
(五)内镜
对肠系膜缺血的诊断价值有限,但可排除其他病变。肠镜已成为常规,对结肠缺血有诊断价值。
【治疗】
(一)AMI的治疗原则
恢复血容量、纠正AMI可能病因。静脉应用广谱抗生素覆盖革兰阴性菌及厌氧菌以预防细菌通过缺血肠黏膜转位引起败血症。
(二)血管扩张剂
当临床拟诊为AMI,并排除其他急腹症者,立即经导管罂粟碱灌注,以60mg作为初始剂量,随后30~60mg/h持续输注12~48小时,以扩张肠系膜血管,改善血流,可避免肠切除或减少切除范围。
(三)溶栓抗凝治疗
药物有链激酶、尿激酶和组织型纤溶酶原激活剂等。
任何确诊SMA栓塞的患者术前均需全身抗凝治疗(如静脉用肝素)以预防血块围绕栓子扩展并防止其进一步栓塞至小肠或其他器官(如脑、冠状动脉、肾、四肢)。抗凝一般术前终止,术后24~48小时恢复使用,具体视术中情况而定。由于MVT病变有复发性,故常规给予抗凝治疗,有主张在关腹前或术后12小时内开始肝素抗凝治疗,而后改为口服抗凝剂,治疗3~6个月。抗凝治疗期间要定期监测凝血酶原时间。
(四)外科手术
当AMI患者出现腹膜刺激征时,应进行剖腹探查。外科干预包括切除坏死和穿孔的肠段、栓子摘除、血管成形、内膜切除和旁路手术等。如手术时,对某些肠段能否存活不能肯定,则应进行第二次手术,术前应用抗生素、补液和纠正严重并发症,以最大限度保住存活肠段。FSI的治疗是切除累及的肠段。
【预后】
AMI发展到肠坏死,死亡率可高达60%~70%。如能早期诊断治疗,生存率可明显改善。总体而言,结肠缺血比小肠缺血预后好得多。肠系膜静脉血栓形成比急性原发的动脉性肠系膜缺血累及小肠预后也好得多。
三、结肠缺血(缺血性结肠炎)
结肠缺血(colon ischemia,CI)是指由于各种原因引起结肠某肠段血供减少,不足以维持细胞正常代谢,从而引起结肠缺血的疾病状态。90%以上的CI患者年龄大于60岁,女性患者相对多见。
【病因】
体循环变化或肠系膜血管器质性/功能性病变均可导致结肠缺血,而直接病因多为局部灌注不足及再灌注损伤。危险因素包括合并有心血管疾病、糖尿病、肠易激综合征和便秘史。相对少见的病因包括高凝状态、医源性结扎IMA、栓塞、血管炎(特别是SLE)、镰状细胞病以及任何能引起结肠梗阻的病因,包括肠道肿瘤、粪石、腹腔嵌顿性疝、肠扭转、肠套叠等。其他更少见的相关因素包括长途奔跑、腹腔内炎症或感染性疾病。药物(可致便秘药物、免疫调节剂、违禁药品等)也可导致与CI相同或类似的损伤。
【分类】
CI肠道损伤类型分为可逆性与非可逆性损伤。可逆性损伤包括结肠病(上皮下出血或水肿)和结肠炎(溃疡)。非可逆性损伤包括肠壁坏疽、暴发性结肠炎、肠腔狭窄等。慢性缺血性结肠炎和细菌移位所致复发性脓毒血症为罕见的肠道非可逆性损伤表现。
【临床表现】
CI常表现为左下腹部突发痉挛性疼痛,排便急迫感,24小时内排鲜红色或暗红色血便甚或血性腹泻。腹痛常先于便血出现,通常为轻中度腹痛,而孤立性右半结肠缺血(IRCI)常仅表现为急性、严重腹痛。受累肠段部位可有压痛。大多数患者临床症状于2~3日内缓解,结肠病变在1~2周内痊愈。坏疽型结肠炎的特点是进行性加重的腹部压痛、反跳痛、肌卫、体温升高及麻痹性肠梗阻。暴发性全结肠炎可表现为突发的、急速进展的腹膜炎征象。
【诊断与鉴别诊断】
腹部CT检查为可疑CI的首选影像学检查方法,同时可评估病变范围,肠壁增厚、水肿及“拇纹征”提示诊断。发现肠壁积气和门静脉肠系膜静脉气体,则提示透壁性梗死的存在。疑诊IRCI可行CTA或血管造影。
如疑为CI且CT发现节段性肠壁增厚,应在发病48小时内实施结肠镜检查。疾病早期可仅见黏膜充血、水肿和黏膜质脆,随着病变的加重出现广泛糜烂、出血、溃疡和肠腔狭窄,暗紫色肠黏膜伴紫蓝色出血性结节常提示坏疽。沿结肠纵轴分布的孤立线性红斑伴糜烂和(或)溃疡(CSSS)则更倾向于诊断CI。
CI好发于左半结肠,其由IMA供血,管径相对狭窄,与腹主动脉呈锐角,影响血流速度,尤其是在各动脉供血相交区域,如结肠脾曲和乙状结肠,前者存在SMA、IMA的吻合点(Griffith's point),后者为IMA的乙状结肠最末分支(Sudeck's point)。这些部位血管发育不全或缺如,易狭窄,故缺血好发于此。直肠由IMA和直肠动脉双重供血,较少发生缺血性梗死。
约10%的CI累及右半结肠(IRCI),右半结肠的动脉血供来自SMA的回结肠动脉分支,发病时可同时伴有末端回肠缺血并导致小肠坏死。IRCI过程常为亚急性,死亡率可高达50%以上。
CI需与克罗恩病、溃疡性结肠炎、感染性肠炎和结肠癌等引起腹痛、便血的疾病相鉴别。本病与溃疡性结肠炎的区别在于直肠很少受累,且病变黏膜与正常黏膜分界清楚。
【治疗】
确诊IC患者应结合病因、并发症等,视病情缓急给予相应治疗。大部分CI患者可在控制原发病和去除危险因素的基础上常规支持治疗,禁食、停用可疑药物(包括缩血管药物)、补液、扩血管和改善微循环等,必要时胃肠减压、肛管排气等。对中、重度CI应考虑应用广谱抗生素治疗。有症状及体征提示肠坏死、穿孔、大量出血或狭窄形成时考虑外科手术治疗。
四、其他肠道血管疾病
(一)肠系膜上动脉压迫征
见本篇第五章第六节“十二指肠壅积症”。
(二)血管炎
许多血管炎综合征可以累及胃肠道,同时常伴有其他内脏累及。
1.结节性多动脉炎
以节段性的微动脉瘤为特征,常累及小到中动脉,其特征是肝、肾和内脏血管常呈1cm左右扩张的血管瘤,小肠比大肠易累及。大约有2/3患者有胃肠道症状,包括腹痛、恶心、畏食和腹泻。许多患者可有发热、高血压及多器官受累。某些患者可因血管阻塞引起缺血,继而引发溃疡、梗死、胃肠道出血或穿孔。动脉造影可显示动脉瘤而提示结节性多动脉炎,其阳性率约75%。
2.过敏性紫癜
是IgA介导的系统性血管炎,以皮肤紫癜、关节炎、腹痛和肾脏疾病为特征性临床表现。累及胃肠道者占29%~69%,症状包括腹痛、腹泻、便血和呕吐。
3.Wegener肉芽肿
是原因未明的全身性血管炎,累及中小动脉,肉芽肿性炎症累及胃肠道并不多见,但可能引起肠道缺血、出血或穿孔。
4.系统性红斑狼疮
胃肠道症状常见,半数以上有腹痛、恶心和呕吐。然而,肠道血管炎只占2%左右,主要累及小动脉,可引起溃疡、出血和梗死,也可引起黏膜下和肌层的静脉炎而导致蛋白丢失性肠病。
5.类风湿性血管炎
在类风湿关节炎患者中约占1%,其中有胃肠道症状者只占10%。胃肠道血管累及时可引起缺血性溃疡、梗死、结肠炎和胃肠道出血。
6.血栓闭塞性血管炎(Buerger's disease)
累及中小血管,可导致远端肠系膜动脉的多发闭塞。
7.白塞病
是一种全身性慢性血管炎性疾病,主要表现为反复发作的口腔生殖器溃疡、眼炎、皮肤损害。其中肠白塞病可累及全消化道,回盲部最易受累,镜下表现以溃疡为主,腹痛、腹泻、消化道出血及穿孔常见。
8.超敏性血管炎
常累及小动脉、小静脉及毛细血管,发病与一系列药物、感染、化学品有关,此病偶可累及胃肠道。
9.冷球蛋白血症
可伴有小血管上免疫复合物沉着,有时可累及消化道。此类患者常伴有丙肝感染。
(三)结肠和小肠杜氏病(dieulafoy disease)
其病理特点是小的黏膜缺损伴其基底部有一支粗大扭曲的小动脉,穿破黏膜进入肠腔内,通常位于胃食管连接部近端6cm范围内。类似的病灶还可见于直肠、结肠、小肠,食管很少见。此病临床表现为反复的、突发的大出血。急诊内镜可发现很小的血管瘤样突起,但出血停止后马上可变得很不明显。未发现溃疡者需反复行内镜检查以明确诊断。结合病史及动脉造影显示粗大扭曲动脉可考虑本病。内镜下治疗包括注射、电凝、环扎或止血钳夹,有时需手术治疗。
(四)肠道血管发育不良(angiodysplasia,AD)
又称动静脉畸形或血管扩张症,是一种位于肠道黏膜层或黏膜下层的薄壁的、扩张的红色血管结构,常累及邻近的小静脉、毛细血管及小动脉。
临床特点是反复发作消化道出血和缺铁性贫血。大多数病变(54%~100%)位于盲肠、升结肠,40%~75%患者有多发病灶,11%~20%患者同时存在小肠病变。
AD的内镜检查阳性率为60%左右。在无严重失血情况下,内镜可见病变平坦或稍高出黏膜,红色,一般为2~10mm,圆形、星状或有明显的蕨样边缘,可有显著的供血血管。内镜检出病变且有活动性出血或有血块黏附是AD出血的依据。对大量出血者,动脉造影为首选,其主要征象有:①动脉期可见血管丛;②动脉后期可见静脉早期显影;③充盈的静脉延迟排空。动脉造影在肠腔内看到外溢的造影剂可确定它是出血原因。
单发病变可采用内镜下APC、注射硬化剂、激光及止血夹等治疗。药物治疗包括雌孕激素、沙利度胺治疗,但疗效有待进一步肯定。对急性大量出血或经内科治疗无效者应考虑手术治疗。
(五)先天性动静脉畸形(arteriovenous malformation,AVM)
本病是在胚胎发育期间生长缺陷所致。病变可发生在任何部位,以四肢多见。肠道病变主要在直肠和乙状结肠。病灶可很小,也可累及一段肠段。组织学改变是黏膜下动脉和静脉之间有持续性的先天性的交通,特征性改变是静脉的“动脉化”,病程较长时可见动脉扩张伴萎缩和硬化。动脉造影是主要的诊断方法。伴有出血的大病灶需要切除累及的肠段,较小病灶可内镜治疗。
(六)其他血管扩张
1.遗传性出血性毛细血管扩张(Osler-Weber-Rendo病)
本病是一种常染色体显性的家族性病变。特点是皮肤、黏膜的毛细血管扩张和反复消化道出血。80%患者有家族史。血管扩张易累及口唇、黏膜(尤其是口腔及鼻部)、消化道(尤其是胃、小肠)、肝、肺、视网膜以及中枢神经系统。典型临床表现为婴幼儿时有反复鼻出血,10岁以前半数患者有消化道出血。内镜检查易作出诊断。可采用雌激素、氨基己酸等药物治疗,无效者可内镜下止血或手术切除肠段。
2.胃窦血管扩张(GAVE)或西瓜胃
可累及小静脉和毛细血管,伴有血栓形成或血管扩张。典型的酷似西瓜图案的红斑性条纹可从胃窦辐射至幽门。患者大都有粪隐血阳性或黑便,多与SLE、混合结缔组织病、硬皮病、恶性贫血有关。
3.其他
累及小静脉及毛细血管的血管扩张还可见于门脉高压患者的胃,表现为多发的针尖样红点状突起或与幽门螺杆菌相关性胃炎相似的马赛克样图案,在胃的近端甚于远端。降低门脉压力的治疗可以减轻或消除这些病灶。
(七)胃肠道血管瘤
胃肠道任何部位都可发生血管瘤,最多见于空肠,其次为回肠、结肠。病变常来自黏膜下血管丛,但有时可累及肌层甚至浆膜层。直径大多<2cm,但直肠病变可较大。
胃肠道血管瘤有不同的分类方法,一般分为毛细血管瘤、海绵状血管瘤和混合型血管瘤。
胃肠道血管瘤临床表现主要为消化道出血,有时从幼年始有慢性间歇性消化道出血,随年龄增长加重。腹部平片见多个移动性钙化点,提示可能存在血管瘤。内镜检查和胶囊内镜可显示蓝紫色黏膜下肿块或息肉样改变,动脉造影可发现异常血管丛或充盈缺损及静脉相延迟。对孤立的或数量较少的小病灶可内镜治疗,大的或多发病灶需要手术治疗。
(八)皮肤和肠道海绵状血管瘤
1860年有作者描述了皮肤血管痣、肠道病变和消化道出血之间的关系,以后称之为blue rubber bleb syndrome。血管瘤呈蓝色,高出表面,直径0.1~5cm,直接压迫可排空血管瘤内血液而留下带皱纹的囊是本病的特点。病变单发或多发,常见于躯干、四肢和面部,可累及胃肠道任何部位,但以小肠最常见,如在结肠常在远端。诊断和治疗同胃肠道血管瘤。
主要参考文献
1.Brandt LJ,Feuerstadt P,Longstreth GF,et al.ACG clinical guideline:epidemiology,risk factors,patterns of presentation,diagnosis,and management of colon ischemia(CI).Am J Gastroenterol,2015,110(1):18-44.
2.Feuerstadt P,Brandt LJ.Update on colon ischemia:recent insights and advances.Curr Gastroenterol Rep,2015,17(12):45.
第十五节
肠梗阻

蒋 炜
肠梗阻(intestinal obstruction)指由于病理因素发生肠内容物在肠道中通过受阻,为临床常见急腹症之一。起病之初,梗阻肠段先有解剖和功能性改变,继而发生体液和电解质的丢失、肠壁循环障碍、坏死和继发感染,最后可致毒血症、休克、死亡。如能及时予以诊疗大多能逆转病情的发展,最终治愈。
【分类】
(一)按梗阻的原因可分为三类
1.机械性肠梗阻
最为常见,是指肠壁本身、肠腔内或肠管外的各种器质性病造成肠腔狭窄或闭塞,致使肠内容物通过受阻。
2.动力性肠梗阻
是指各种原因导致肠壁肌肉舒缩紊乱,失去蠕动能力,肠内容物不能有效排出而产生的梗阻,而肠壁本身并无解剖上的病变。
动力性肠梗阻又可分为:
(1)麻痹性肠梗阻:
亦称无动力性肠麻痹。因感染、中毒、低钾血症、脊髓炎、甲状腺功能减退、腹部手术等原因影响到肠道自主神经系统,致使肠道平滑肌收缩障碍,使肠管扩张,蠕动消失,肠内容物无法推进。
(2)痉挛性肠梗阻:
任何原因引起的肠道副交感神经兴奋,而使肠道处于异常的高动力状态致痉挛,肠内容物不能运行,多为短暂性。
3.缺血性肠梗阻
是指由于肠系膜血管病变引起肠壁缺血,继而引起蠕动障碍造成肠梗阻。
(二)按肠壁血供情况分为两类
1.单纯性肠梗阻
仅有肠腔阻塞而无肠壁血供障碍,多见于肠腔内堵塞或肠外肿块压迫所致的肠梗阻。
2.绞窄性肠梗阻
在肠腔阻塞时,肠壁因血管被压迫而引起缺血坏死,多因肠扭转、肠套叠、嵌顿疝、肠粘连等引起。
(三)按梗阻发生的部位分为两类
1.小肠梗阻
又可分为:高位小肠梗阻,主要指发生于十二指肠或空肠的梗阻;低位小肠梗阻,主要是指远端回肠的梗阻。
2.结肠梗阻
多发生于左侧结肠,以乙状结肠或乙状结肠与直肠交界处为多见。
(四)按梗阻的程度
可分为完全性梗阻与不完全性(或部分性)梗阻。
(五)按起病的缓急
可分为急性肠梗阻与慢性肠梗阻。
各种分类之间是相互关联的,也可随病理过程的演变而转化:例如由单纯性变为绞窄性、由不完全性变为完全性等;机械性肠梗阻长时间存在,梗阻以上部位肠襻由于过度膨胀以及毒素的吸收,血运障碍等,也可转化为麻痹性肠梗阻。
【病因】
(一)机械性肠梗阻常见的病因
1.肠管外病因
(1)粘连与粘连带压迫:先天性粘连带较多见于小儿,而腹盆腔手术、结核性腹膜炎及非特异性腹腔内感染产生的粘连是成人最常见的原因,但少数病例可无腹部手术及炎症史。
(2)疝:腹股沟斜疝、股疝、内疝的嵌顿。
(3)肠扭转:可为原发性及继发性肠扭转,常由于粘连所致。
(4)肠外肿瘤或腹块压迫。
2.肠腔内阻塞
由胆石、粪石、异物、蛔虫等引起。
3.肠壁病变
(1)先天性狭窄和闭孔畸形。
(2)炎症、肿瘤、吻合手术及其他因素所致的狭窄,例如炎症性肠病、肠结核、放射性损伤、肿瘤(尤其是结肠癌)、肠吻合术等。
(3)肠套叠:多见于儿童,因息肉或其他肠管病变引起。
(二)动力性肠梗阻常见的病因
1.麻痹性肠梗阻
可并发于:①腹部大手术后;②腹腔内炎症;③电解质紊乱;④腹膜后炎症或出血破裂等;⑤肠缺血,如肠系膜栓塞等;⑥肾和胸部疾病,如肾周围脓肿、心肌梗死等;⑦全身性脓毒血症;⑧应用某些药物:如吗啡类药物、抗胆碱药物等。
2.痉挛性肠梗阻
肠道炎症及神经系统功能紊乱均可引起肠管暂时性痉挛。
(三)血管性肠梗阻病因
肠系膜动脉栓塞或血栓形成和肠系膜静脉血栓形成为主要病因。
【病理解剖】
单纯性完全性机械性肠梗阻时,梗阻部位以上的肠腔扩张、肠壁变薄,黏膜糜烂和溃疡发生,肠壁可因血供障碍而坏死穿孔,而梗阻以下部分肠管多呈空虚塌陷。麻痹性肠梗阻时肠管扩张、肠壁变薄。绞窄性肠梗阻早期,静脉回流受阻,小静脉和毛细血管可发生瘀血、通透性增加,甚至破裂而渗血;继而动脉血流受阻、血栓形成,肠壁因缺血而坏死,肠内细菌和毒素可通过损伤的肠壁,进入腹腔。坏死肠管呈紫黑色,最后可自行破裂。
【病理生理】
肠梗阻病理生理改变的严重程度视梗阻部位的高低、梗阻时间的长短以及肠壁有无血液供应障碍而不同。慢性肠梗阻多为不完全性,梗阻近端肠管长时期的蠕动加强,导致肠壁代偿性增厚和肠腔膨胀,远端肠管变细萎缩;全身性病理生理改变主要表现为营养不良。而急性肠梗阻可引起以下变化:
(一)局部病理生理变化
1.肠蠕动增加
梗阻近端的肠管蠕动频率和强度增加,肠鸣音亢进;而远端肠管可正常蠕动,伴随肠内容物排出,肠管塌陷空虚,两者交界处即为梗阻所在部位。病情进展时,近端肠管进一步膨胀,终使肠壁平滑肌收缩力减弱直至麻痹。
2.肠腔扩张、积气积液
梗阻近端积聚大量液体和气体,抑制肠壁黏膜吸收水分并刺激其分泌增加,导致肠腔膨胀进行性加重。
3.肠壁充血水肿,通透性增加
随着梗阻时间的延长,肠管内压力增高,致使肠壁静脉回流障碍,引起肠壁通透性增加,甚至引起细菌腹膜炎,严重时肠管可因缺血坏死而溃破穿孔。
(二)全身病理生理变化
1.水、电解质丢失
高位小肠梗阻时呕吐频繁,当梗阻位于幽门或十二指肠上段,呕吐过多胃酸,则易产生脱水和低氯低钾性碱中毒;若梗阻位于十二指肠下段或空肠上段,则重碳酸盐丢失严重。低位肠梗阻时,呕吐虽不多见,但因肠黏膜吸收功能降低而分泌液量增多,肠腔中大量积液。此外,过度肠膨胀可引起肠壁水肿和血浆外渗,严重时可导致低血压和低血容量休克。
2.感染和毒血症
当单纯性梗阻转变为绞窄性时,梗阻近端的肠内容物淤积,细菌繁殖产生大量毒素,可透过肠壁引起肠源性的腹腔内感染,并经腹膜吸收导致全身性中毒。
3.休克
急性肠梗阻若不及时治疗,大量的水、电解质丧失引起血容量减少,加之感染和中毒,极易导致中毒性休克。
4.心肺功能障碍
肠腔扩张致腹压增高时,横膈上升,影响肺内气体交换;同时腹压增高亦使下腔静脉血液回流障碍,加之血容量减少,进一步影响到心输出量。
总之,高位肠梗阻容易引起水、电解质紊乱,低位肠梗阻易产生肠腔膨胀、感染和中毒。绞窄性肠梗阻容易导致休克,闭襻性肠梗阻容易引起肠穿孔和腹膜炎。而在不同类型肠梗阻后期,各种病理生理变化均可出现。
【临床表现】
(一)临床症状
1.腹痛
常为首发症状,多为阵发性绞痛。十二指肠及上段空肠梗阻时因呕吐起减压作用、低位回肠梗阻因肠胀气抑制肠蠕动,患者绞痛较轻。急性空肠梗阻时绞痛较剧烈,常每2~5分钟即发作1次。不完全性肠梗阻腹痛在一阵肠鸣或排气后可见缓解。慢性肠梗阻亦然,且间歇期亦长。结肠梗阻时除阵发性绞痛外可有持续性钝痛,此种情况的出现应注意有闭襻性肠梗阻即肠段两端梗阻的可能性。若腹痛的间歇期不断缩短,或疼痛呈持续性伴阵发性加剧,则肠梗阻可能是单纯性梗阻发展至绞窄性肠梗阻,若肠壁已发生缺血坏死则呈持续性剧烈腹痛。肠梗阻晚期,梗阻部位以上肠管过度膨胀,收缩能力减弱,则阵痛的程度和频率都降低;当出现麻痹性肠梗阻,则无绞痛发作,而呈持续性胀痛。
2.呕吐
肠梗阻的早期为反射性呕吐,而后期则为反流性呕吐。梗阻部位越高,呕吐出现愈早、愈频繁,呕吐物为胃液、十二指肠液和胆汁;低位肠梗阻时,呕吐出现较晚,呕吐物为粪样液体,或有粪臭味。绞窄性肠梗阻时,呕吐物为血性或棕褐色。而麻痹性肠梗阻的呕吐往往为溢出性。结肠梗阻呕吐少见,但后期回盲瓣因肠腔过度充盈而关闭不全时亦有较剧烈的呕吐,吐出物可含粪汁。
3.腹胀
高位小肠梗阻呕吐频繁多无明显腹胀;低位小肠梗阻或结肠梗阻晚期常有显著的全腹膨胀。肠扭曲引起的闭襻性梗阻的肠段膨胀很突出,常呈不对称的局部膨胀。麻痹性肠梗阻时,全部肠管均膨胀扩大,故腹胀显著。
4.便秘和停止排气
完全性肠梗阻时,患者排便和排气现象消失。但在高位小肠梗阻的最初2~3天,如梗阻以下肠腔内积存了粪便和气体,则仍有排便和排气现象,不能因此否定完全性梗阻的存在;同样,在绞窄性肠梗阻如肠扭转、肠套叠以及结肠癌所致的肠梗阻等都仍可有血便或脓血便排出。
5.全身症状
单纯性肠梗阻患者一般无明显全身症状,但呕吐频繁和腹胀严重者必有脱水。血钾过低者有疲软、嗜睡、乏力和心律失常等症状。绞窄性肠梗阻患者全身症状最显著,早期即有虚脱,很快进入休克状态。伴有腹腔感染者,腹痛持续并扩散至全腹,同时有畏寒、发热、白细胞增多等感染和毒血症表现。
(二)体征
1.全身情况
一般表现为急性痛苦面容,神志清楚,呼吸受限、急促;有酸中毒时,呼吸深而快。当有脱水情况时,患者可表现为唇干舌燥,眼窝及两颊内陷,皮肤弹性消失。若出现休克症状,可出现神志萎靡、淡漠、恍惚,甚至昏迷。此时患者可有脉快、面色苍白、出冷汗、四肢厥冷、血压下降等表现。
2.腹部体征
(1)腹部膨胀:
高位小肠梗阻多在上腹部,低位小肠梗阻多在中腹部,麻痹性肠梗阻则呈全腹膨隆。
(2)肠型和蠕动波:
在慢性肠梗阻和腹壁较薄的病例,肠型和蠕动波特别明显。
(3)肠鸣音(或肠蠕动音)亢进或消失:
机械性肠梗阻绞痛发作时,在梗阻部位经常可听到肠鸣音亢进,如一阵密集气过水声;肠腔明显扩张时,蠕动音可呈高调金属音性质。在麻痹性肠梗阻或机械性肠梗阻并发腹膜炎时,肠蠕动音极度减少或完全消失。
(4)腹部压痛:
常见于机械性肠梗阻,压痛伴肌紧张和反跳痛主要见于绞窄性肠梗阻,尤其是并发腹膜炎时。
(5)腹块:
在成团蛔虫、肠套叠或结肠癌所致的肠梗阻,往往可触到相应的腹块,压痛明显的部位往往为病变所在。蛔虫性肠梗阻时可为柔软索状团块,回盲部肠套叠时腊肠样平滑包块常在右中上腹,腹外疝嵌顿多为圆形突出腹壁的压痛性肿块,而癌肿性包块多坚硬而压痛较轻。直肠指检时可触及直肠内外的肿块或肠套叠的底部。
(三)实验室检查
单纯性肠梗阻早期各种化验检查变化不明显,梗阻晚期或有绞窄时,血红蛋白与血细胞比容因脱水和血液浓缩而升高。单纯性肠梗阻时白细胞计数正常或轻度增高,绞窄性肠梗阻时明显升高,中性粒细胞数也增加。血气分析及血清钾、钠、氯的变化可反映酸碱平衡和电解质紊乱的情况。呕吐物和粪便检查有大量红细胞或隐血阳性,应考虑肠管有血运障碍。
(四)影像学检查
1.X线腹部平片
肠管的气液平面是肠梗阻特有的X线表现,摄片时最好取直立位,若体弱不能直立时可取侧卧位。一般在肠梗阻发生4~6小时后,即可见肠腔内积气,立位片可见多个液平面,呈阶梯状,伴有倒“U”形扩张的曲影。空肠梗阻时,扩张的小肠影位于腹部中央,呈横向排列,空肠黏膜皱襞展平消失、肠皱襞呈环形伸向腔内,环形皱襞呈“鱼肋骨刺状”。而回肠梗阻时,皱襞黏膜较平滑,至晚期时小肠肠襻内多个液平面出现,典型的呈阶梯状。而结肠梗阻时梗阻近端肠腔内扩张积气,回盲瓣闭合良好时形成闭襻样梗阻,结肠扩张十分明显,尤以右半结肠更为显著。结肠梗阻时小肠充气和液平面常不明显,由于结肠胀气,腹腔外形呈“镜框形”。
2.X线造影
多用于慢性不完全性肠梗阻或缓解期。肠梗阻时因钡剂通过时间长,可加重或延误治疗,多不宜采用钡剂造影检查。而水溶性碘油造影,视梗阻部位,特别是高位梗阻时,可以了解梗阻的原因及部位。
3.CT检查
小肠梗阻时,其梗阻近端腔内有较多潴留液,口服钡剂造影与内镜检查常难以作出诊断。而多排螺旋CT小肠造影(MDCTE)却可利用潴留液可作为阴性对比剂,对梗阻部位、程度的确定以及梗阻病因的估计体现出诊断优势,特别对怀疑腹部恶性肿瘤所致梗阻。
(五)纤维结肠镜检查
慢性不完全性结肠梗阻患者在钡剂灌肠不能明确诊断时,可考虑结肠镜检查。
【诊断和鉴别诊断】
典型的肠梗阻不难诊断。其诊断要点为:①有腹痛、腹胀、呕吐、肛门停止排气排便四项主要症状;②腹部检查可见肠型,腹部压痛,肠鸣音亢进或消失;③X线腹部透视或摄片检查可见肠腔明显扩张与多个液平面。符合上述诊断要点的病例,肠梗阻可以确诊,但要重视其病因的分析判断。例如有腹部手术或外伤史、有结核性腹膜炎或腹腔内其他炎症病史者应考虑粘连性肠梗阻可能。如在便秘或餐后劳动或剧烈活动后发生急性腹痛、呕吐、腹胀者,应考虑肠扭转可能。如出现痉挛性腹痛、腹部肿块、黏液血便者,尤其发生于小儿,应考虑肠套叠可能。腹部检查应包括腹股沟部以排除腹外疝嵌顿;直肠指检应注意有无粪块充填、直肠内肿瘤等。
病因判断虽然重要,但从临床治疗的角度来说,判别梗阻的类型与治疗方案的选择更密切相关。应考虑的鉴别如下:
1.机械性肠梗阻和动力性肠梗阻的鉴别
机械性肠梗阻的特征是阵发性肠绞痛、肠鸣音亢进和非对称性腹胀;而麻痹性肠梗阻的特征为无绞痛、肠鸣音消失和全腹均匀膨胀;痉挛性肠梗阻可有剧烈腹痛突然发作和消失,间歇期不规则,肠鸣音减弱而不消失,但无腹胀。X线腹部平片有助于鉴别:机械性梗阻的肠胀气局限于梗阻部位以上的肠段;麻痹性梗阻时,全部胃、小肠和结肠均有胀气,程度大致相同;每隔5分钟拍摄正、侧位腹部平片以观察小肠有无运动更有助于两者鉴别。而痉挛性梗阻时,肠无明显胀气和扩张。
2.单纯性肠梗阻和绞窄性肠梗阻的鉴别
绞窄性肠梗阻常发生于单纯性机械性肠梗阻的基础上,出现下列征象应疑有绞窄性肠梗阻:①腹痛急骤发生且持续不减,或由阵发性绞痛转变为持续性腹痛,疼痛部位较为固定,若伴背部牵涉痛更提示为绞窄性肠梗阻;②腹部有压痛、反跳痛和腹肌强直,肠鸣音亢进可不明显;③腹胀不对称,腹部触及有压痛的肿块;④呕吐物、胃肠减压引流物、腹腔穿刺液含血液,亦可有便血;⑤全身情况恶化出现早、进展快,毒血症表现明显,病情急剧恶化可出现休克征象,若梗阻不能解除,抗休克治疗改善将不显著;⑥经胃肠减压后,腹胀减轻,但腹痛发作无明显减少;⑦X线平片检查可见孤立、凸出胀大的肠襻,不因时间而改变位置,或有假肿瘤阴影。临床不能除外绞窄性肠梗阻者,应在积极准备下,及时手术探查为宜。
3.小肠梗阻和结肠梗阻的鉴别
高位小肠梗阻呕吐频繁而腹胀较轻,低位小肠梗阻则反之。结肠梗阻的临床表现与低位小肠梗阻相似。但X线腹部平片检查则可区别。小肠梗阻时充气的肠襻遍及全腹,液平较多,而结肠则不显示。若为结肠梗阻则在腹部周围可见扩张的结肠和袋形,小肠内积气则不明显。
4.完全性肠梗阻和不完全性肠梗阻的鉴别
完全性肠梗阻多为急性发作而且症状明显,不完全性肠梗阻则多为慢性梗阻,症状不明显,往往为间隙性发作。X线平片检查完全性肠梗阻者肠襻充气扩张明显,不完全性肠梗阻则否。
【治疗】
肠梗阻的治疗方法取决于梗阻的病因、性质、部位、病情和患者的全身情况。但不论采取何种治疗方法,纠正肠梗阻所引起的脱水、电解质和酸碱平衡的紊乱,行胃肠减压以改善梗阻部位以上肠段的血液循环以及控制感染等皆属必要。
(一)纠正脱水、电解质丢失和酸碱平衡紊乱
首先根据病程、临床表现等估计液体丢失量和欠缺的正常需要量,一般成人症状较轻的约需补液1500ml,有明显呕吐的则需补液3000ml,而伴周围循环衰竭和低血压时则需补液4000ml以上。再根据心、肾功能、血清电解质和血气分析结果加以调整,并应监测尿量及中心静脉压的变化。单纯性肠梗阻早期,上述生理紊乱较易纠正,但在绞窄性肠梗阻和机械性肠梗阻晚期,尚需补给全血或血浆、白蛋白等方能有效地纠正循环障碍。
(二)胃肠减压
胃肠插管减压可减轻腹胀,有利于肠壁循环的恢复,避免吸入性肺炎的发生。少数轻型单纯性肠梗阻经有效的减压后肠腔可恢复通畅。对拟手术治疗的患者胃肠减压可减少手术操作困难,增加手术的安全性。结肠梗阻发生肠膨胀时,插管减压无效,常需手术减压。
(三)控制感染和毒血症
肠梗阻时间过长或发生绞窄时,肠壁和腹膜常有多种细菌感染,积极地采用以抗革兰阴性杆菌及厌氧菌为重点的广谱抗生素静脉滴注治疗十分重要,可以显著降低肠梗阻的死亡率。
(四)解除梗阻、恢复肠道功能
1.非手术治疗
对一般单纯性机械性肠梗阻,尤其是早期不完全性肠梗阻可作非手术治疗。早期肠套叠、肠扭转引起的肠梗阻亦可在严密的观察下先行非手术治疗,动力性肠梗阻除非伴有外科情况,一般不需手术治疗。
(1)中药:复方大承气汤,适用于一般肠梗阻、气胀较明显者;甘遂通结汤,适用于较重的肠梗阻、积液较多者。上述中药可煎成200ml,分次口服或经胃肠减压管注入。
(2)油类:可用石蜡油、生豆油或菜油200~300ml分次口服或由胃肠减压管注入。适用于病情较重,体质较弱者。
(3)麻痹性肠梗阻如无外科情况可用新斯的明注射、腹部芒硝热敷等治疗。
(4)内镜治疗:内镜不仅可实施乙状结肠扭转纤维肠镜复位,并通过肛管对扭转部位进行减压;还可进行内镜取异物及嵌顿物治疗。近年来,多种新技术应用于肠梗阻内镜治疗:①X线透视或胃镜引导下经鼻型肠梗阻导管的置入,不仅可用于急性单纯性、黏连性小肠梗阻以及用作小肠造影,还可于广泛肠粘连松解术中,小肠内放置肠梗阻导管行肠排列术,以预防术后小肠再次发生粘连性梗阻。但食管狭窄、幽门狭窄、肠坏死及绞窄性肠梗阻为其禁忌证。②经肠镜支架置入,既可作为肿瘤无广泛或远处转移、可进行肿瘤根治术的结直肠癌肠梗阻的术前过渡,以改善整体情况,增加对手术的耐受性;又可主要应用于肿瘤已远处转移无法行肿瘤根治术结肠癌患者,或者其他肿瘤腹腔转移压迫肠管引起肠梗阻患者的姑息治疗。
(5)若为肠套叠亦可用空气钡灌肠法使之复位解除梗阻。
(6)针刺足三里、中脘、大枢、内关、合谷、内庭等穴位可作为辅助治疗。
2.手术治疗
绝大多数机械性肠梗阻需作外科手术治疗,缺血性肠梗阻和绞窄性肠梗阻更应及时手术处理。
(1)手术指征:
①积极非手术治疗无效,临床症状不缓解或有加重者;②绞窄性肠梗阻及不能除外绞窄性肠梗阻者也应及时手术处理;③有腹膜刺激体征者。
(2)外科手术的主要内容为:
①松解粘连或嵌顿性疝,整复扭转或套叠的肠管等,以消除梗阻的局部原因;②切除坏死的或有肿瘤的肠段,引流脓肿等,以清除局部病变;③肠造瘘术可解除肠膨胀,肠吻合术可绕过病变肠段,恢复肠道的通畅。
【预后】
单纯性肠梗阻的死亡率约在3%左右,而绞窄性肠梗阻则可达10%~20%。改善预后的关键在于早期诊断、及时处理。
[附]慢性假性肠梗阻
假性肠梗阻(intestinal pseudo-obstruction,IPO)是一种有肠梗阻的症状和体征,但无机械性梗阻证据的综合征。按发病的急缓分为急性和慢性(复发性)两类,前述的麻痹性肠梗阻即为急性假性肠梗阻,此处介绍慢性假性肠梗阻。
原发性假性肠梗阻的病因主要是肠壁平滑肌或肠肌神经丛病变所引起,主要为常染色体显性遗传,可表现为家族性或散发性发病。继发性假性肠梗阻可继发于多种基础疾病,如结缔组织病、淀粉样变性、原发性肌病、神经系统疾病、内分泌病以及药物因素(吩噻嗪类、三环类抗忧郁药、抗帕金森病药等)、手术因素(如空回肠旁路术等)等。
患者的症状多始于儿童或青春期,少数在30~40岁时才出现。病程通常是急性发作与缓解反复交替。发作时有程度不等的恶心、呕吐、腹痛、腹泻或脂肪泻;缓解期可无或只有较轻的症状。并可影响到全消化道或某一局部,如只累及十二指肠,可表现为巨十二指肠,常有大量呕吐和体重减轻,易被误诊肠系膜上动脉综合征;如只累及结肠则主要表现为慢性便秘和反复粪块嵌塞。有的病例有膀胱排空障碍。X线检查可见受累的食管与胃肠道显著扩张、运行迟缓。
假性肠梗阻的诊断应结合病史、体征、实验室、影像学及内镜检查等,继发性假性肠梗阻患者可查出神经系统的症状与体征。除外机械性肠梗阻是诊断假性肠梗阻的重要条件。
假性肠梗阻治疗原则主要是缓解临床症状,减少并发症,保持营养与维持电解质平衡,改善和恢复肠动力。急性结肠假性肠梗阻患者易引起肠穿孔,死亡率高,在保守治疗无效情况下可采用结肠镜下减压术。除对病变局限的假性肠梗阻如巨十二指肠和巨结肠采用节段性肠切除外,应尽量避免外科手术治疗。
主要参考文献
1.Jackson PG,Raiji MT.Evaluation and management of intestinal obstruction.Am Fam Physician,2011,83(2):159-165.
2.Cirocchi R,Farinella E,Trastulli S,et al.Safety and efficacy of endoscopic colonic stenting as a bridge to surgery in the management of intestinal obstruction due to left colon and rectal cancer:a systematic review and meta-analysis.Surg Oncol,2013,22(1):14-21.

