第八章
肝脏疾病
第一节
肝硬化及其并发症

王吉耀
肝硬化(hepatic cirrhosis)是一种由不同病因长期作用于肝脏引起的慢性、进行性、弥漫性肝病。是在肝细胞广泛坏死基础上产生肝脏纤维组织弥漫性增生,并形成再生结节和假小叶,导致肝小叶正常结构和血液供应遭到破坏。病变逐渐进展,晚期出现肝衰竭、门静脉高压和多种并发症,每年约有100万患者死亡。
【病因】
(一)病毒性肝炎
乙型、丙型和丁型肝炎病毒引起的慢性肝炎是我国肝硬化的主要病因,占50%~60%。慢性乙型肝炎演变为肝硬化的年发生率为0.4%~14.2%。病毒的持续存在、中到重度的肝脏坏死炎症以及纤维化是演变为肝硬化的主要原因。乙型和丙型或丁型肝炎的重叠感染或酗酒常可加速肝硬化的进展。
(二)慢性酒精性肝病
在欧美国家慢性酒精中毒为肝硬化最常见的原因(约50%~90%),我国较为少见(约10%),但近年来有升高趋势。长期大量饮酒可导致肝硬化。如合并乙型和丙型肝炎的感染,可加速病情的进展。
(三)非酒精性脂肪性肝病
由非酒精性脂肪性肝炎引起的肝硬化逐年增多,尤其合并代谢综合征者。是仅次于上述两种病因的最为常见的肝硬化前期病变。
(四)长期胆汁淤积
包括原发性胆汁性胆管炎和继发性胆汁性肝硬化。后者由各种原因引起的肝外胆道长期梗阻所致。高浓度胆酸和胆红素对肝细胞的毒性作用可导致肝细胞变性、坏死、纤维化,进而发展为肝硬化。
(五)药物或毒物
由各种药物、化学毒物或保健品引起的肝损伤可演变为肝硬化。
(六)肝脏血液循环障碍
慢性右心心力衰竭、慢性缩窄性心包炎和各种病因引起的肝静脉阻塞综合征(巴德-吉(基)亚利综合征)、肝窦阻塞综合征/肝小静脉闭塞病(hepatic sinusoidal obstruction syndrome/hepatic veno-occlusive diseace,HSOS/HVOD)引起肝窦长期淤血、缺氧,导致肝小叶中心区肝细胞坏死、纤维化,演变为肝硬化。
(七)遗传和代谢性疾病
由遗传和代谢疾病的肝脏病变发展成肝硬化,又称代谢性肝硬化。在我国,以由铜代谢障碍所致的肝豆状核变性(Wilson病)最多见。其他少见的有肝糖原累积症和由铁代谢障碍引起的血色病(hemochromatosis)。α1-抗胰蛋白酶(α 1 -Antitrypsin, α1-AT )基因异常引起α1-AT缺乏症、酪氨酸代谢紊乱造成酪氨酸血症极为少见。
(八)免疫紊乱
自身免疫性肝炎最终可发展为肝硬化。
(九)血吸虫病
血吸虫卵在门静脉分支中堆积,造成嗜酸性粒细胞浸润、纤维组织增生,导致窦前区门静脉高压,在此基础上发展为血吸虫性肝硬化。
(十)隐源性肝硬化
由于病史不详,组织病理辨认困难、缺乏特异性的诊断标准等原因未能查出病因的肝硬化,约占5%~10%。其他可能的病因包括营养不良、肉芽肿性肝损、感染等。
【发病机制】
上述各种病因均可引起肝脏的持续损伤。致病因素作用于肝脏,首先由库普弗细胞和肝免疫细胞产生的细胞因子激活位于肝窦的肝星形细胞(hepatic stellate cell,HSC),后者转化为成纤维细胞,产生大量胶原和炎性因子。细胞外间质(extracellular matrix,ECM)成分合成增加、降解减少,总胶原量增加为正常时的3到10倍,同时其成分发生变化、分布改变。在血管内皮生长因子(VEGF)等的调控下,内皮细胞上窗孔直径变小、数量减少、细胞间隙变窄、消失和基质蛋白沉淀,最终导致肝窦内皮细胞下基底膜形成,称为肝窦毛细血管化(sinusoid capillarization)。肝细胞表面绒毛变平以及屏障形成,肝窦内物质穿过肝窦壁到肝细胞的转运受阻,直接扰乱肝细胞功能,导致肝细胞的合成功能障碍。肝窦变狭窄、肝窦血流受阻、肝内阻力增加影响门静脉血流动力学,造成肝细胞缺氧和养料供给障碍,加重肝细胞坏死,使始动因子得以持续起作用。肝细胞广泛坏死、坏死后的再生以及肝内纤维组织弥漫增生,导致正常肝小叶结构的破坏。正常门管区消失,代之以增生的肝细胞结节,被增生的纤维组织重新分割,形成假小叶。肝实质结构的破坏还引起了肝内血管分流,例如从门静脉分支到肝静脉的短路,肝硬化时约1/3的肝血流分流,加重了肝细胞的营养障碍。缺氧引起VEGF增加,导致新生血管形成也增加了分流。纤维隔血管交通吻合支的产生和再生结节压迫以及增生的结缔组织牵拉门静脉、肝静脉分支,造成血管扭曲、闭塞,使肝内血液循环进一步障碍,假小叶的肝细胞没有正常的血流供应系统,可再发生坏死和纤维组织增生。如此病变不断进展,肝脏逐渐变形、变硬,功能进一步减退,形成肝硬化。以上病变也是出现硬化的肝脏进一步发生肝功能不全和门静脉高压的基础(图15-8-1)。
近年来研究提示肝纤维化是ECM合成和降解失平衡的动态过程,通过治疗,特别是去除病因,可以逆转肝纤维化和早期肝硬化。
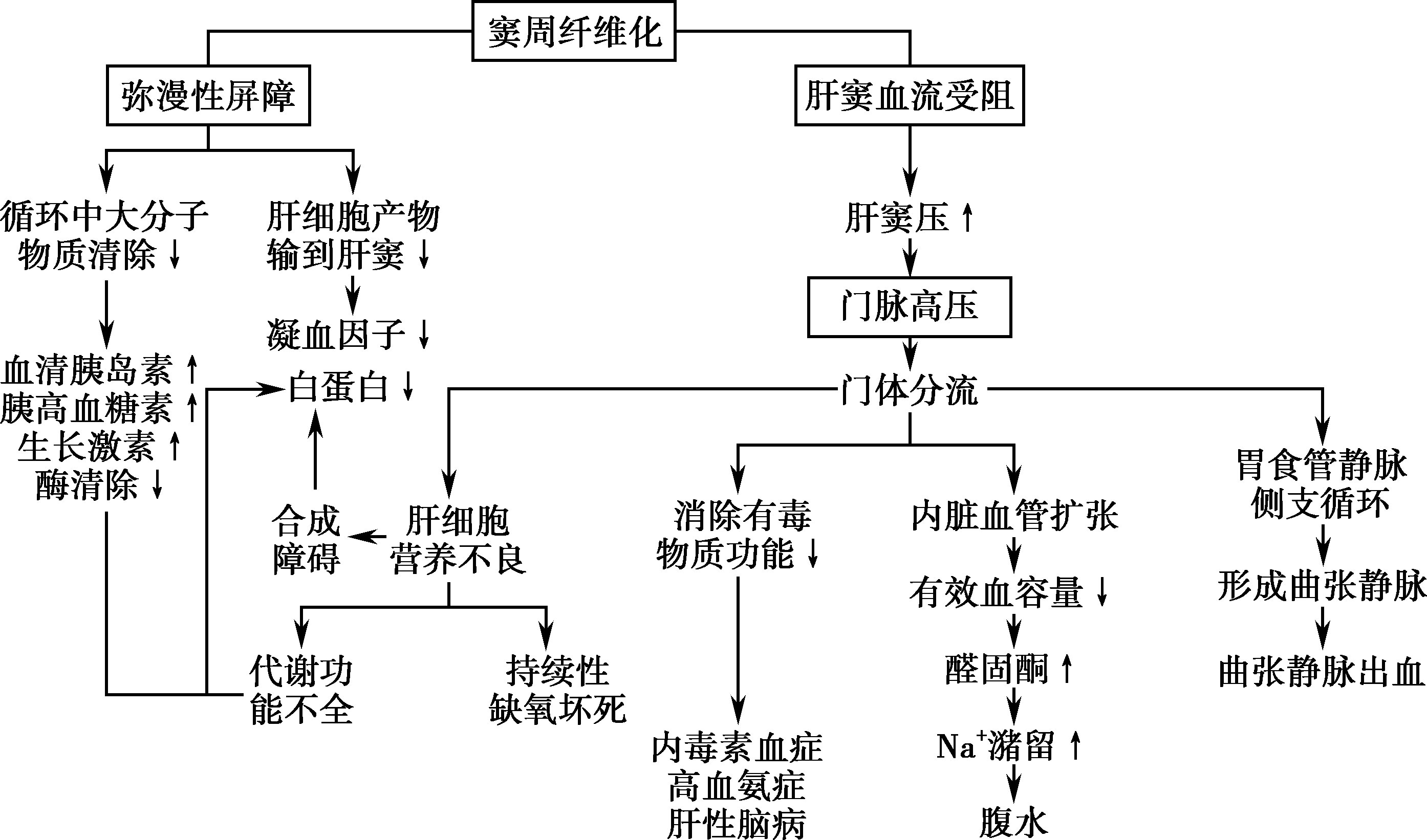
图15-8-1 结缔组织在窦周狄氏间隙沉积(窦周纤维化)的后果
【病理和病理生理】
(一)病理
病理特点是在肝细胞坏死基础上,小叶结构塌陷,弥漫性纤维化以及肝脏结构的破坏,代之以纤维包绕的异常的肝细胞结节(假小叶)和肝内血管解剖结构的破坏。
1.结节
1994年国际肝病信息小组,按结节形态将肝硬化分为三类:小结节性肝硬化(结节大小相等,直径<3mm,纤维间隔纤细)、大结节性肝硬化(结节大小不等,直径>3mm,也可达5cm或更大纤维间隔粗细不等,一般较宽)、大小结节混合性肝硬化(大结节与小结节比例相同)。
2.纤维化
用特殊染色可以观察到肝病理切片中的肝纤维化程度。用半定量方法及常用的分级系统(METAVIR或Ishak)可以将纤维化分为4级(前者)或6级(后者)来说明肝纤维化的严重程度。第4或第6级可以诊断为肝硬化。早期观察发生肝纤维化的位置对病因的判断有一定帮助。如从门管区和门脉周围开始的纤维化常提示慢性病毒性肝炎、自身免疫性肝炎,而如果开始时累及中央静脉,常见于酒精性和非酒精性脂肪性肝病或静脉流出道障碍。进展期和晚期肝硬化,肝脏正常结构消失,无法辨认。
3.血管的改变
除了纤维化进展,血管结构的改变在肝内循环中对于增加血管阻力和门脉高压病理生理在起重要作用。纤维间隔中有新生的血管,CD31染色可见血管密度增加。在肝硬化结节中可以显示CD34免疫组化染色阳性的肝窦内皮细胞,证明肝窦毛细血管化。
肝穿刺活检时,釆用18G穿刺活检针,标本长度应>1.5cm,包括11个门管区。
(二)病理生理
1.门静脉高压症(portal hypertension)
指门静脉压力持续升高引起的临床综合征。表现为侧支循环形成、腹水和脾大。临床上常用肝静脉楔入压与游离压之差即肝静脉压力梯度(hepatic venous pressure gradient,HVPG)来代表门静脉压力。正常人≤5mmHg,当 HVPG大于等于6mmHg时,定义为门静脉高压。当HVPG大于等于10mmHg时,出现临床表现,可发生胃食管静脉曲张。一旦HVPG大于等于12mmHg,可以发生腹水和曲张破裂出血。门静脉压力取决于门静脉血流量和门静脉阻力。肝硬化时门静脉阻力增加是门静脉高压发生的始动因子;而门静脉血流的增加是维持和加剧门静脉高压的重要因素,肝硬化引起的门脉高压是窦性和窦后性的。
(1)门静脉阻力增加:
主要由肝结构改变相关的机械因素引起(70%)。包括肝窦毛细血管化导致肝窦顺应性减少;胶原在Disse间隙沉着使肝窦变狭窄,以及再生结节压迫肝窦和肝静脉系统导致肝窦及其流出道受阻均引起门静脉血管阻力的增加。另有30%是可调控的因素,如肝窦内内皮素增加和一氧化氮(NO)减少引起星形细胞收缩、5-羟色胺(5-HT)等缩血管激素作用于门脉上受体导致的血管阻力增加和对α-肾上腺素能刺激反应性增强。
(2)门静脉血流量增加:
肝硬化时肝脏对去甲肾上腺素等物质清除能力降低以及交感神经兴奋,使心脏收缩增加,心输出量增加,又由于胰高糖素和NO增加,其扩血管作用以及对缩血管物质G蛋白依赖的传导途径损害,造成了血管对缩血管物质的低反应性,导致内脏小动脉扩张,形成肝硬化患者的内脏高动力循环。此时内脏血管充血,门静脉血流量增加,静脉压力持续升高,形成门静脉高压症。
晚近的研究结果提示新生血管的形成既增加了肝内阻力,又增加了内脏血流量,因此也是导致门静脉压力增高的因素。
(3)门静脉高压的后果
1)侧支循环形成:
门静脉高压时形成侧支循环来降低门脉压力,因此在门静脉与腔静脉之间形成许多交通支。这些交通支开放后,出现血流方向的改变,静脉扩张和迂曲。此时门静脉血可不经肝,通过侧支经腔静脉直接回右心。
主要的侧支循环有:①食管下段和胃底静脉曲张:门静脉血液通过胃左和胃短静脉、食管静脉回流到奇静脉。由于食管下段黏膜下静脉缺乏结缔组织支持,曲张静脉突出于食管腔内,该静脉距门静脉主干最近,最直接持续受门脉高压影响。食管静脉的局部因素决定了出血的危险性,包括曲张静脉的直径、静脉壁的厚度、曲张静脉内与食管腔之间的压力梯度。而出血的严重度则取决于肝脏失代偿程度、凝血功能障碍程度、门静脉压力和曲张静脉的粗细。门静脉高压导致的胃底静脉曲张及胃底黏膜血管扩张充血、黏膜水肿糜烂(门脉高压性胃病)也是引起上消化道出血的重要原因。②腹壁静脉显露和曲张:门静脉高压时脐静脉重新开放,通过腹壁上、下静脉回流,形成脐周和腹壁静脉曲张。脐静脉起源于肝内门静脉左支,因此肝外门静脉阻塞时无脐静脉开放,亦无腹壁静脉曲张。③直肠下端静脉丛:肠系膜下静脉分支痔上静脉与回流髂静脉的痔中、下静脉吻合,形成肛管直肠黏膜下静脉曲张,易破裂产生便血。此外,所有腹腔脏器与腹膜后或腹壁接触、黏着部位,均可能有侧支循环的建立。
侧支循环建立后不仅可因曲张静脉破裂引起消化道出血,还由于大量门静脉血不经肝脏而流入体循环,一方面使肝细胞营养进一步障碍,坏死增加,代谢障碍;另一方面对毒素清除减少,易产生内毒素血症和引起肝性脑病,内毒素血症可促使NO合成增加,进一步加重高动力循环。门静脉高压引起的胃肠道淤血、胃肠黏膜水肿可引起胃肠道分泌吸收功能紊乱,产生食欲减退、消化吸收不良、腹泻、营养不良等后果。
2)腹水形成:
参见下文“腹水”部分。
3)脾大:
参见第十六篇第五章第八节。
2.腹水
(1)腹水形成机制:
液体潴留在腹腔形成腹水(ascites),是多种因素综合作用的结果。门静脉高压导致内脏动脉扩张和有效动脉循环血容量下降是引起腹水的主要原因,血清白蛋白减少导致的体渗透压降低是引起腹水的重要因素。
1)门静脉压力增高:
正常时肝窦压力极低(0~2mmHg),门静脉高压时,肝窦静水压升高(门脉压力>10mmHg,是腹水形成的基本条件),大量液体流到Disse间隙,造成肝脏淋巴液生成过多。肝硬化患者常为正常人的20倍,当胸导管不能引流过多的淋巴液时,就从肝包膜直接漏入腹腔形成腹水。肝窦压升高还可引起肝内压力受体激活,通过肝肾反射,减少肾对钠的排泄,加重了水钠潴留。
2)内脏动脉扩张:
肝硬化引起的门静脉阻力增加导致扩血管物质如NO增加;门静脉高压增加了细菌移位,细菌的内毒素和炎症因子如TNF-α均可导致内脏血管扩张,进而通过侧支循环,引起全身血管扩张,导致有效动脉循环血容量下降,动脉压下降,进而激活交感神经系统、肾素-血管紧张素-醛固酮系统、增加抗利尿激素(ADH)释放来维持动脉压,造成肾血管收缩和钠水潴留。门脉高压与内脏血管扩张相互作用,改变了肠道的毛细血管压力和通透性,有利于液体在腹腔积聚。
3)血浆胶体渗透压降低:
肝硬化患者摄入减少,肝储备功能下降,合成白蛋白能力下降,导致血浆白蛋白降低,进而血浆胶体渗透压降低,大量的液体进入组织间隙,形成腹水。
4)其他因素:
肝硬化患者的内毒素血症和炎症还可导致毛细血管通透性增加。血浆中心钠素相对不足和机体对其敏感性降低、雌激素灭活减少、抗利尿激素分泌增加导致的排水功能障碍和前列腺素分泌减少,造成肾血管收缩,肾脏灌注量下降,肾血流量重新分布,均与腹水的形成和持续存在有关。
腹水可经壁层腹膜吸收,最大速率900ml/d,吸收的腹水经肠淋巴管引流或经内脏毛细血管重吸收。由于淋巴系统已超负荷,内脏毛细血管循环因Starling力的作用吸收有限,加上肝硬化患者常有腹膜增厚,吸收率下降。腹水生成增加而吸收下降,使腹水逐渐增多。
(2)自发性细菌性腹膜炎形成机制:
在腹腔内无感染源的情况下,腹水自发性感染导致自发性细菌性腹膜炎(spontaneous bacterial peritonitis,SBP)和内毒素血症。肝硬化患者肠道细菌过度生长和肠壁通透性增加,肠壁局部免疫防御功能下降,使肠腔内细菌发生易位经过肠系膜淋巴结进入循环系统产生菌血症。由于患者单核-吞噬细胞系统活性减弱,以及腹水中调理素、免疫球蛋白、补体及白蛋白下降导致腹水感染。
3.内分泌系统
(1)性激素紊乱:
由于肝细胞功能衰竭以及门体分流使主要在肝脏灭活的雌激素水平增高,在外周组织例如皮肤、脂肪组织、肌肉中雄激素转换为雌激素的转换率增高。患者出现肝掌、蜘蛛痣以及男性乳房发育。
(2)甲状腺激素:
肝硬化患者血清总T 3 、游离T 3 减低,游离T 4 正常或偏高,严重者T 4 也降低。上述改变与肝病严重程度之间具有相关性。由于肝病时5'-脱碘酶活性降低,T 4 转化为T 3 减少,反T 3 (rT 3 )形成增加,临床上可致生化性低T 3 综合征。此外,肝硬化血氨增高时,多巴胺类物质减少,可使TSH水平增高。
(3)肾上腺皮质功能:
肝硬化特别是有并发症的患者常伴有肾上腺功能不全,并随着疾病进展,严重度增加。
4.呼吸系统
(1)肝性胸腔积液:
腹水患者常伴胸腔积液,其性质与腹水相同,称为肝性胸腔积液(hepatic hydrothorax)。其发生机制可能由于腹压增高,膈肌腱索部变薄,形成胸腹间通道。由于胸腔负压,腹水由孔道进入胸腔。也可能与低蛋白血症引起胸膜毛细血管胶体渗透压降低,胸腔积液滤出增加,吸收降低以及奇静脉、半奇静脉压力增高、肝淋巴回流增加,导致胸膜淋巴管扩张、淤积、破坏,淋巴液外溢形成胸腔积液有关。胸腔积液以右侧多见。
(2)门脉性肺动脉高压:
门脉高压患者中2%~5%有继发性肺动脉高压,称为门脉性肺动脉高压(portopulmonary hypertension)。由于肺动脉收缩、肺动脉内膜纤维化和微小血栓形成所致。
(3)肝肺综合征:
肝肺综合征(hepatopulmonary syndrome,HPS)是进展性肝病、肺内血管扩张、低氧血症/肺泡-动脉氧梯度增加(>20mmHg)组成的三联征,肝脏对肺部扩血管活性物质灭活能力降低和肺部NO增多,引起肺血管阻力降低,出现肺内血管尤其是肺前毛细血管或毛细血管扩张、使氧分子难以弥散到毛细血管中去,难以与血红蛋白氧合,引起低氧血症/肺泡-动脉氧梯度增加。
5.泌尿系统
由于肾血管的极度收缩导致的肾皮质灌注不足导致肾衰竭称肝肾综合征(hepatorenal syndrome,HRS),是终末期肝硬化最常见而严重的并发症。肝硬化患者肝窦压升高,NO增加,造成内脏动脉扩张,有效血容量不足,反射性激活肾素-血管紧张素和交感系统产生肾动脉极度收缩,造成肾内血供过度不足,产生HRS。肝肾综合征时,患者虽然有肾功能不全,但是肾脏可无组织学上改变,是可逆的循环相关性肾衰竭。
6.血液系统
常表现为门静脉高压导致脾大和脾功能亢进(hypersplenism)。外周血全血细胞减少。由于肝脏合成障碍导致凝血因子合成减少,凝血酶原时间延长。血小板有质与量的降低,因此,患者常有贫血及出血倾向。
7.心血管系统
心输出量和心率增加、内脏血管扩张形成高动力循环。由于β-肾上腺能受体信号传导降低,跨膜电流和电机械耦合的改变,NO产生过多和大麻素-1受体刺激上调出现心肌收缩和舒张功能不全,导致肝硬化性心肌病(cirrhotic cardiomyopathy)。
8.神经系统
在肝硬化基础上出现的神经和精神异常,称为肝性脑病(hepatic encephalopathy,HE)。氨代谢紊乱引起的氨中毒是HE的重要发病机制。肝硬化失代偿时,肠道来源的氨生成和吸收增加,过多的氨由于肝脏实质的严重损害不能充分通过鸟氨酸循环合成尿素来清除,且因门脉高压引起门体分流,肠道的氨未经肝脏解毒而直接进入体循环,导致血氨增高,其通过血脑屏障进入脑组织,产生对中枢神经系统的毒性。
氨中毒引起HE的机制:①脑内星形胶质细胞(astrocyte)肿胀:脑内清除氨的主要途径依靠存在于星形胶质细胞中谷氨酰胺合成酶合成谷氨酰胺,后者是一种很强的有机渗透质,可导致该细胞肿胀、功能受损,进一步影响氨的代谢,并可影响神经元有效摄入或释放细胞外离子和神经递质的能力;②脑能量障碍:血氨过高可抑制丙酮酸脱氢酶活性,从而影响乙酰辅酶A生成,干扰大脑的三羧酸循环。谷氨酸被星形细胞摄取在合成谷氨酰胺过程中消耗线粒体上的α-酮戊二酸及ATP。其减少能使三羧酸循环运转降低,致大脑细胞能量供应不足,导致功能紊乱;③干扰神经细胞膜离子转运:氨可通过干扰神经细胞膜离子转运改变基因如水通道蛋白的表达,损害颅内血流自动调节机制,产生脑水肿;④氨促进活性氧的释放:启动氧化应激反应,导致线粒体功能障碍,损害细胞内信号通路,促进神经元中凋亡级联反应的发生。
其他毒性物质包括γ-氨基丁酸(gamma-aminobutyric acid,GABA)和假性神经递质等。前者进入血脑屏障通过与GABA/Bz复合受体结合促进氯离子由神经元胞膜的离子通道进入突触后神经元的细胞质,使膜超极化,引起神经传导抑制。后者因肝衰竭时,对食物中的芳香族氨基酸如酪氨酸、苯丙氨酸等经肠菌脱羧酶转变为酪胺和苯乙胺的清除发生障碍,通过血脑屏障进入脑组织,在脑内经β羟化酶的作用分别形成章胺(β-羟酪胺)和苯乙醇胺。后两者的化学结构式与正常兴奋性神经递质去甲肾上腺素相似,但不能传递神经冲动,故称为假神经递质。它们在脑内取代了突触中的正常递质,兴奋冲动不能正常地传到大脑皮质而产生异常抑制,故出现意识障碍与昏迷。
感染引起的全身炎症反应,促炎因子增加,NO和NOS氧化应激增加,TNF-α刺激星形胶质细胞分泌IL-1 IL-6等细胞因子,影响了血脑屏障的完整性。
总之,肝性脑病发病是由多种因素共同作用的结果,其中氨起了主要作用。星形胶质细胞功能的改变导致了神经细胞之间联系及功能破坏,低钠血症可以加重脑白质的轻度水肿。星形胶质细胞水肿还可刺激产生神经激素,促进GABA能神经递质的产生,进一步激活氧化应激和蛋白激酶。以上多种因素相互协同、依赖、互为因果共同促进了肝性脑病的发生和发展。
静息态功能MRI(fMRI)的研究显示,HE患者存在静息态脑网络的选择性损害,即背侧注意网络、脑默认网络、视觉网络及听觉网络异常,而感觉运动网络和自我参照网络未受损。利用全脑功能连接的fMRI研究发现,轻微肝性脑病患者存在广泛的脑功能连接异常,尤其是基底核-丘脑-皮质网络功能连接的改变在轻微肝性脑病的形成中起了关键作用。
大多数HE的发病通常都可以找到诱发因素,如:①消化道出血;②高蛋白饮食;③低钾性碱中毒;④低血容量与缺氧;⑤感染;⑥麻醉、镇痛、催眠、镇静等类药物;⑦便秘。这些诱发因素通过促进氨等毒素的生成,加重肝功能的损伤或增强毒素对神经系统的损伤,诱发肝性脑病的发生。
【临床表现】
起病常隐匿,早期可无特异性症状、体征,根据病程进展可分为代偿期和失代偿期。
(一)代偿期肝硬化
包括临床1期(无静脉曲张、无腹水)和临床2期(无腹水,内镜检查有食管静脉曲张,无出血)。10%~20%代偿期肝硬化患者无症状。其他患者可有食欲减退、乏力、消化不良、腹泻等非特异性症状。临床表现同慢性肝炎,鉴别常需依赖肝脏病理。
(二)失代偿期肝硬化
出现腹水是肝硬化患者进入失代偿期的标志。此期包括临床3期(有腹水,伴或不伴食管静脉曲张,无出血)、4期(食管静脉出血,伴或不伴腹水)和5期(出现脓毒血症或肝肾综合征等)。
1.症状
患者症状包括食欲减退、乏力、腹胀、腹痛、腹泻(较普遍,常与肠壁水肿,吸收不良和肠腔菌群失调有关)、体重减轻;出血倾向(凝血功能障碍可出现牙龈、鼻腔出血、皮肤黏膜紫斑或出血点,女性常有月经过多);内分泌系统失调(男性有性功能减退,男性乳房发育,女性常有闭经及不孕)。肝硬化患者的糖尿病发病率增加,表现为高血糖、糖耐量试验异常、高胰岛素血症和外周性胰岛素抵抗。进展性肝硬化伴严重肝细胞功能衰竭患者常发生低血糖及各种并发症的临床表现(见下文)。
2.体征
患者常呈慢性病容,面色黝黑,面部有毛细血管扩张、口角炎等。皮肤表现常见蜘蛛痣、肝掌,可出现男性乳房发育,胸、腹壁皮下静脉可显露或曲张,甚至在脐周静脉突起形成水母头状,曲张静脉上可听到静脉杂音。黄疸常提示病程已达到中期,随着病变进展而加重。1/3患者常有不规则发热,与病情活动及感染有关。腹部移动性浊音阳性。肝性胸腔积液常见于右侧(占85%),但也有双侧(2%)甚至仅为左侧(13%)。
肝脏在早期肿大,晚期坚硬缩小、肋下常不易触及。胆汁淤积和静脉回流障碍引起的肝硬化晚期仍有肝大。35%~50%患者有脾大,常为中度,少数重度。
3.并发症的临床表现
(1)食管胃静脉破裂出血:
急性出血患者出现呕血、黑便,严重者休克。死亡率平均32%,是肝硬化较为常见和严重的并发症。
(2)自发性细菌性腹膜炎:
住院的腹水患者中发生率为10%~30%。常表现为短期内腹水迅速增加,对利尿剂无反应,伴腹泻、腹痛、腹胀、发热,腹壁压痛和反跳痛。少数患者伴血压下降、肝功能恶化或门体分流性脑病加重。
(3)原发性肝癌:
进行性肝大,质地坚硬如石,表面结节状。
(4)肝肾综合征:
顽固性腹水基础上出现少尿、无尿以及恶心等氮质血症时的临床表现。常伴黄疸、低蛋白血症、肝性脑病;无蛋白尿。临床有二种类型:Ⅰ型,进展性肾功能损害,2周内肌酐成倍上升;Ⅱ型,肾功能缓慢进展性损害。
(5)肝肺综合征:
终末期肝病患者中发生率13%~47%。患者可出现杵状指、发绀、蜘蛛痣。
(6)肝性脑病:
常在诱因作用下,患者出现认知障碍,表现为计算能力下降,定位定时错误,轻度性格改变例如欣快激动或淡漠少言,行为失常如衣冠不整或随地便溺,昼夜倒错。严重时出现谵妄,进而昏迷。患者有肝臭,可引出扑翼样震颤(flapping tremor或asterixis)。分期见表15-8-1。
最近认为HE患者神经认知异常是一个渐进的过程。根据临床表现的严重度分为隐匿性肝性脑病(covert HE,CHE)和显性肝性脑病(overt HE,OHE)。CHE包括没有临床异常仅通过特殊检查才能发现的认知障碍的轻微肝性脑病(minimal HE,MHE)和 West Haven分类的1级。OHE为 West Haven分类的2、3、4级(表15-8-1)。
(7)门静脉血栓形成:
发生率10%~25%,大多B超检查时发现。43%稳定型,血栓缓慢形成,无明显临床症状;38%出现食管静脉或门脉高压性胃病出血;18%可出现剧烈腹痛,其中70%出现小肠梗死(intestinal infarction)。
(8)肝硬化性心肌病:
没有其他已知的心脏疾病的肝硬化患者,在应激情况下(行创伤性措施如外科手术/TIPS),心脏收缩反应损害和(或)舒张功能不全以及电生理异常(如Q-T间期延长),发生心功能不全甚至猝死。
综上所述,肝硬化早期表现隐匿,失代偿期的临床表现可以归结为:①门脉高压的表现,如侧支循环、脾大、脾功能亢进、腹水等;②肝储备功能损害所致的蛋白合成功能降低(包括白蛋白,凝血酶原)、黄疸、内分泌失调及皮肤表现等;并可出现并发症相关的临床表现。
表15-8-1 West Haven分级和临床说明
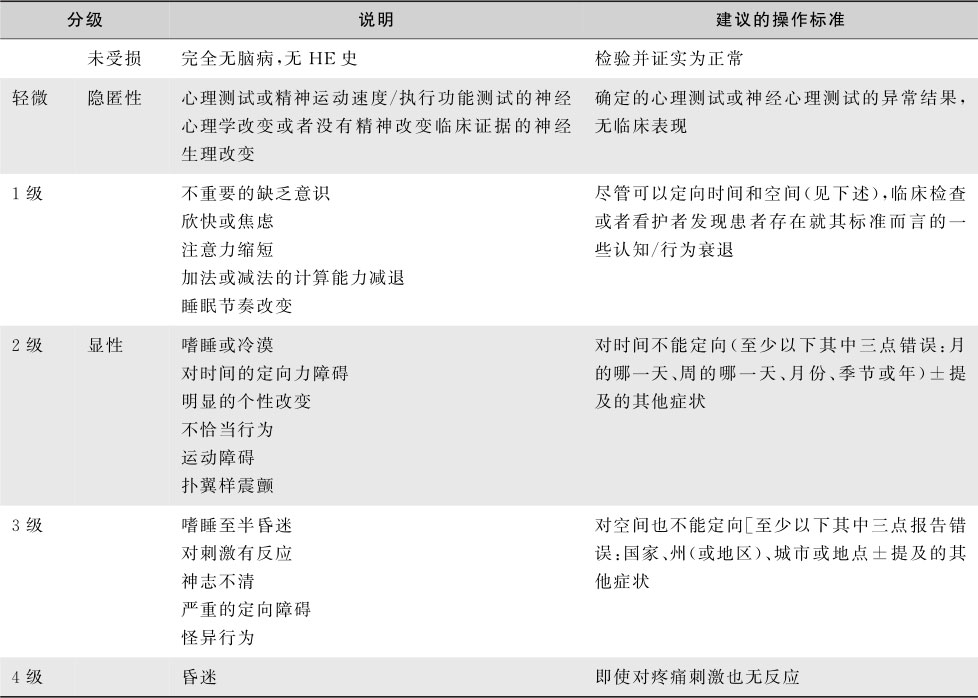
注:要求所有情况与肝功能不全和(或)门体分流有关
【实验室和辅助检查】
(一)实验室检查
1.血常规
代偿期多在正常范围。失代偿期由于出血、营养不良、脾功能亢进可发生轻重不等的贫血。有感染时白细胞可升高,脾功能亢进者白细胞和血小板均减少。
2.尿液检查
一般在正常范围,乙型肝炎肝硬化合并乙肝相关性肾炎时尿蛋白阳性。胆汁淤积引起的黄疸尿胆红素阳性,尿胆原阴性。肝细胞损伤引起的黄疸,尿胆原亦增加。腹水患者应常规测定24小时尿钠、尿钾。
3.便常规
消化道出血时出现肉眼可见的黑便和血便,门脉高压性胃病引起的慢性出血,便隐血试验阳性。
4.肝功能试验
(1)血清胆红素:
失代偿期可出现结合胆红素和总胆红素升高,胆红素的持续升高是预后不良的重要指标。
(2)蛋白质代谢:
肝脏是合成白蛋白的唯一场所,在没有蛋白丢失的情况(如蛋白尿)时,血清白蛋白量常能反映肝脏储备功能。在肝功能明显减退时,白蛋白合成减少。正常值为35~55g/L,白蛋白低于28g/L为严重下降。肝硬化时由于损伤的肝细胞不能清除从肠道来的抗原,或后者经过门体分流直接进入体循环,刺激脾脏B淋巴细胞产生抗体,形成高球蛋白血症。白蛋白与球蛋白比例降低或倒置。蛋白电泳可显示白蛋白降低,γ-球蛋白显著增高,β-球蛋白轻度升高。血清前白蛋白(pre-albumin)也由肝合成,当肝细胞受损伤尚未引起血清白蛋白下降时,血清前白蛋白则已明显下降。肝硬化患者可下降50%左右。
(3)凝血酶原时间:
是反映肝脏储备功能的重要预后指标,晚期肝硬化及肝细胞损害时明显延长,如用维生素K后不能纠正,更说明有功能的肝细胞减少。
(4)血清酶学检查:
①氨基转移酶:肝细胞受损时,ALT升高,肝细胞坏死时,AST升高。肝硬化患者这两种酶不一定升高,但肝硬化活动时可升高。酒精性肝硬化患者AST/ALT≥2。②γ-GT:90%肝硬化患者可升高,尤其以PBC和酒精性肝硬化升高更明显。合并肝癌时明显升高。③ALP:70%的肝硬化患者可升高,合并肝癌时常明显升高。④胆碱脂酶(ChE):肝硬化失代偿期Ch E活力明显下降,其降低程度与血清白蛋白大致平行,若ChE极度降低者提示预后不良。
(5)反映肝纤维化的血清学指标:
有Ⅲ型前胶原氨基末端肽(PⅢP);Ⅳ型胶原;透明质酸。肝纤维化时以上各项指标升高,由于受多种因素影响,尚不能作为确诊肝纤维化的指标,联合不同的血清学指标的数学模型有助于鉴别有无显著肝纤维化。
(6)脂肪代谢:
代偿期患者血中胆固醇正常或偏低,PBC和非酒精性脂肪性肝病患者升高。失代偿期总胆固醇特别是胆固醇酯明显降低。
(7)定量肝功能试验:
吲哚菁试验(ICG):检测肝细胞对染料清除情况以反映肝细胞储备功能,是临床初筛肝病患者较有价值和实用的试验。患者空腹静脉抽血后注射ICG 0.5mg/kg,注射后15分钟对侧手臂静脉血测滞留率。正常值10%以下,肝硬化患者ICG滞留率明显升高,甚至达50%以上。其他的定量肝功能试验包括利多卡因代谢产物生成试验、氨基比林呼气试验、半乳糖耐量试验、色氨酸耐量试验、咖啡因清除试验等。
(8)血氨:
动脉血氨的测定对肝性脑病有辅助诊断的价值。
5.血清电解质
对于判断患者有无电解质紊乱以及治疗有重要意义。
6.甲胎蛋白(AFP)
肝硬化活动时,AFP可升高。合并原发性肝癌时明显升高,如转氨酶正常AFP持续升高,需怀疑原发性肝癌。
7.病毒性肝炎标记测定
疑肝硬化者须测定乙、丙、丁肝炎标记以明确病因。肝硬化有活动时应作甲、乙、丙、丁、戊型标记及CMV、EB病毒抗体测定,以明确有无重叠感染。
8.血清免疫学检查
血清抗线粒体抗体阳性提示PBC(阳性率95%),自身免疫性肝病时常有抗平滑肌抗体、抗核抗体阳性。
9.血清铜蓝蛋白
肝豆状核变性时明显降低(<200mg/L),伴尿铜增加(>100μg/24h)。年龄<40岁的肝损伤患者应检查血清铜蓝蛋白排除此病。
(二)影像学检查
1.超声检查
肝硬化的声像图为肝表面不光滑或凹凸不平:肝叶比例失调,多呈右叶萎缩和左叶、尾叶增大:肝实质回声不均匀增强,肝静脉管腔狭窄、粗细不等。此外,还有脾大、门静脉扩张和门脉侧支开放等门脉高压症的声像图改变,部分患者还可探及腹水。多普勒超声可发现门脉侧支开放、门静脉血流速率降低和门静脉血逆流等改变。对门静脉血栓形成和肝癌等肝硬化的并发症也有较高的诊断价值。超声造影检查对鉴别肝硬化结节和肝癌有较高的诊断价值。
2.CT
肝硬化影像学与超声检查所见相似,表现为肝叶比例失调、肝裂增宽和肝门区扩大,肝脏密度高低不均。此外,还可见脾大、门静脉扩张和腹水等门脉高压症表现(图15-8-2)。对于肝硬化和原发性肝癌的鉴别十分有用。
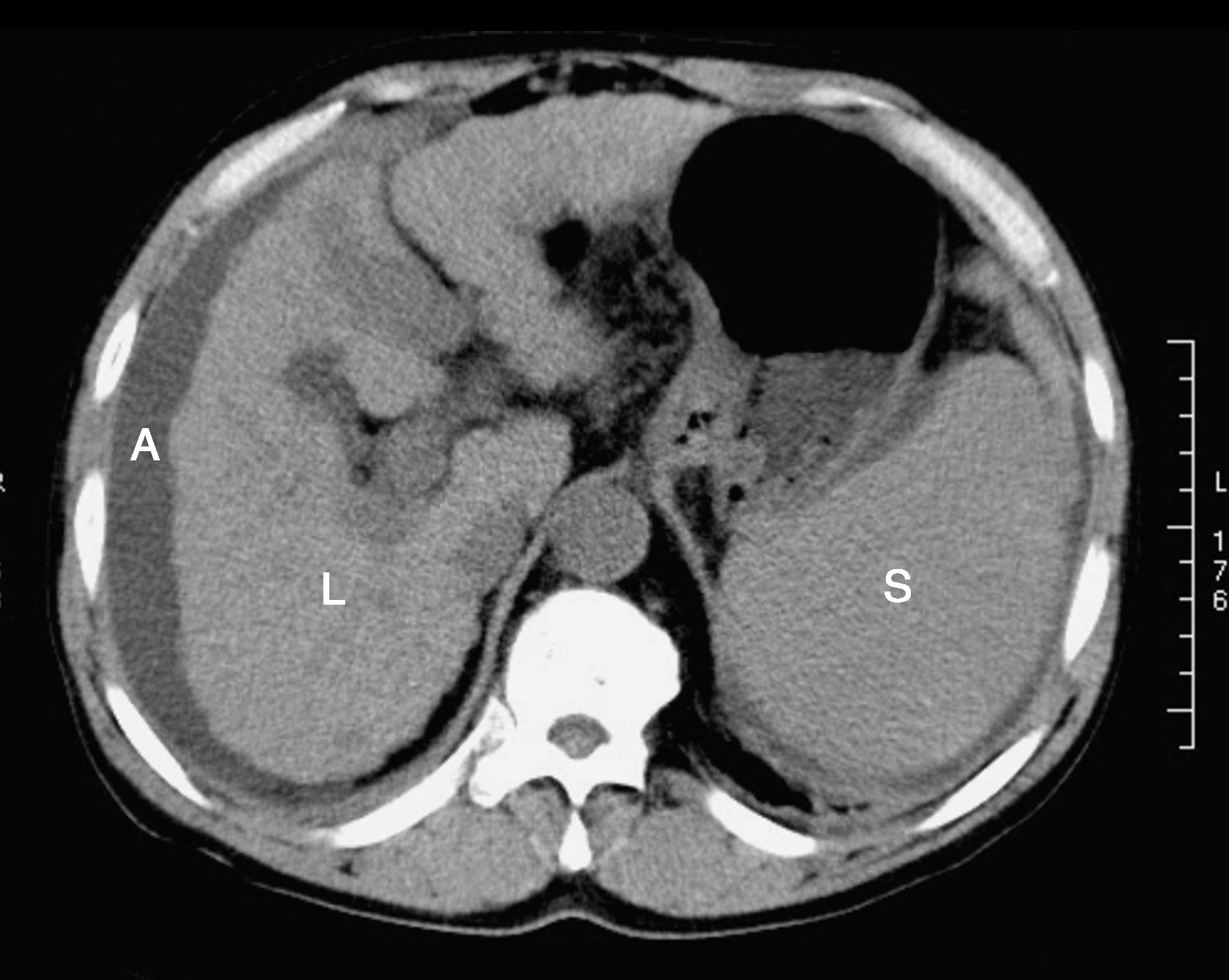
图15-8-2 肝硬化CT表现为肝叶比例失调、肝裂增宽和肝门区扩大,肝脏密度高低不均
3.磁共振成像(MRI)
磁共振成像除与CT相似外,对鉴别肝硬化结节、肝瘤结节更优于CT检查。磁共振血管成像(MRA)可代替血管造影显示门脉血管变化和门脉血栓。用于门静脉高压病因的鉴别以及肝移植前对门脉血管的评估。
4.放射性核素显像
经放射性核素 99 m Tc-扫描测定的心/肝比值能间接反映门静脉高压和门体分流程度,对诊断有一定意义,正常值0.26,肝硬化患者一般在0.6以上,伴门脉高压者常>1。
5.上消化道钡餐摄片
可发现食管及胃底静脉曲张征象,食管静脉曲张呈现虫蚀状或蚯蚓状充盈缺损,胃底静脉曲张呈菊花样缺损。但诊断敏感性不如胃镜。
(三)特殊检查
1.内镜
胃镜可直接观察并确定食管及胃底有无静脉曲张,了解其曲张程度和范围,并可确定有无门脉高压性胃病。存在食管及胃底静脉曲张是门静脉高压最可靠的指标,一旦出现曲张静脉即可诊断门静脉高压。结肠镜可在结肠发现异位静脉曲张;胶囊内镜和小肠镜可发现小肠异位静脉曲张,从而找出下消化道出血原因。
2.肝穿刺
1秒钟快速穿刺、超声指引下或腹腔镜直视下肝穿刺,取肝组织做病理检查,对肝硬化,特别是早期肝硬化确定诊断和明确病因有重要价值。凝血酶原时间延长及有腹水者可经颈静脉、肝静脉做活检,安全、并发症少。
3.肝硬度检测
瞬时弹性成像技术(transient elastography,TE)又称fibroscan,通过量化肝硬度值(kPa)诊断慢性肝病肝纤维化。无或Ⅰ级纤维化<7.3kPa;显著肝纤维化(3~4级)>12.4kPa;>17.5kPa时,诊断肝硬化的特异性>90%。>20kPa,提示合并临床显著门脉高压(clinical significant portal hypertension,CSPH)。
4.腹腔镜
可见肝脏表面高低不平,有大小不等的结节和纤维间隔,边缘锐利不规则,包膜增厚,脾大,圆韧带血管充血和腹膜血管曲张,腹水原因诊断不明确时,腹腔镜检查有重要价值。
5.门静脉测压
经颈静脉测定肝静脉楔入压和肝静脉游离压,两者差为HVPG,可代表门静脉压力。正常值0~5mmHg,食管静脉曲张出血者均>12mmHg。门静脉压力的测定是评价降门脉压力药物疗效的金标准。
6.腹水检查
所有新出现的腹水者、进展性肝硬化或上消化道出血伴腹水者以及腹水稳定的患者病情突然恶化,都应作诊断性穿刺。目的在于明确腹水是否由肝硬化引起,如果血清-腹水白蛋白梯度(SAAG)>11g/L提示腹水由肝硬化门静脉高压所致。此时则应寻找是否存在导致腹水增加的原因,如SBP等。检查内容包括:腹水的性质,如颜色、比重、蛋白含量、细胞分类以及腺苷脱氨酶(ADA)、血与腹水LDH比值、细菌培养和内毒素测定。腹水培养应在床旁进行,使用血培养瓶,包括需氧、厌氧两种。每个培养瓶接种的腹水至少10ml。
【诊断与鉴别诊断】
(一)肝硬化的诊断和鉴别诊断
1.肝硬化的诊断主要依据
①病史:以了解肝硬化病因。应详细询问肝炎史,饮酒史、药物史、输血史、社交史及家族遗传性疾病史。②症状体征:根据上述临床表现逐条对患者进行检查,确定是否存在门脉高压和肝功能障碍表现。③肝功能试验:血清白蛋白降低,胆红素升高,凝血酶原延长提示肝功能失代偿,定量肝功能试验也有助于诊断。④影像学检查:B超、CT有助于本病诊断。完整的诊断应包括病因、病理、功能和并发症四个部分。
(1)病因诊断:
明确肝硬化的病因对于估计患者预后及进行治疗密切相关。根据上述各种病因作相关检查以排除及确定病因诊断,如应做病毒性肝炎标志物排除由肝炎引起的肝硬化,怀疑Wilson病应由眼科检查K-F环,测定血清铜蓝蛋白、尿铜、血铜等。
(2)病理诊断:
肝活组织检查可明确诊断及病理分类,特别在有引起肝硬化的病因暴露史,又有肝脾大但无其他临床表现、肝功能试验正常的代偿期患者,肝活检常可明确诊断。
(3)肝脏储备功能诊断:
可用Child-Pugh分级(Child-Pugh Classification,CPC)来评定(表15-8-2)。
表15-8-2 肝硬化患者Child-Pugh分级标准
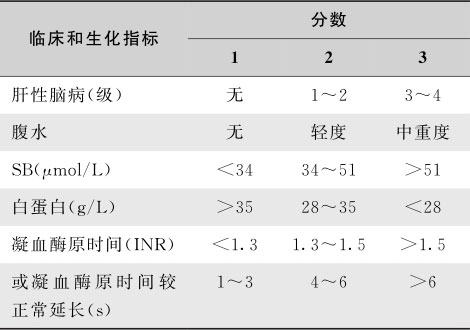
注: * PBC:SB(μmol/L)17~68:1分;68~170:2分;>170:3分
总分:A级≤6分;B级7~9;C级≥10分
2.鉴别诊断
(1)肝、脾大:
与血液病、代谢性疾病的肝脾大鉴别。必要时做肝活检。
(2)腹水的鉴别诊断:
应确定腹水的程度和性质,与其他原因引起的腹水鉴别。肝硬化腹水为漏出液,SAAG>11g/L;合并自发性腹膜炎为渗出液,以中性粒细胞增多为主,但SAAG仍大于11g/L。结核性和肿瘤性腹水SAAG<11g/L。结核性腹膜炎为渗出液伴ADA增高。肿瘤性腹水比重介于渗出液和漏出液之间,腹水LDH/血LDH>1,可找到肿瘤细胞。腹水检查不能明确诊断时,可做腹腔镜检查,常可明确诊断。
(二)并发症的诊断和鉴别诊断
1.食管胃静脉破裂出血
表现为呕血、黑便,常为上消化道大出血。在大出血暂停,血压稳定后,急症胃镜检查(一般在入院后12~48小时)可以明确出血部位和原因,鉴别是胃食管静脉出血(gastriceso phageal variceal bleeding)还是门静脉高压性胃病(portal hypertensive gastrophathy)或溃疡病引起。如由静脉曲张引起,需进一步检查明确静脉曲张由单纯肝硬化引起门静脉高压还是由门脉血栓或癌栓引起。
2.感染
发热的肝硬化患者需要确定有无感染以及感染的部位和病原。应摄胸片、作痰培养、中段尿培养、血培养,有腹水者进行腹水检查,以明确有无肺部、胆道、泌尿道及腹水感染。患者在短期内腹水迅速增加,伴腹痛、腹胀、发热、腹水检查白细胞>500×10 6 /L或中性粒细胞>250×10 6 /L,如能排除继发性感染者,即可诊断SBP。腹水和血鲎试验以及血细菌培养可阳性,常为革兰阴性菌。少数患者可无腹痛,患者可出现低血压或休克(革兰阴性菌败血症)。鉴别诊断应除外继发性腹膜炎、内脏破裂或脓肿。继发性腹膜炎的特点是腹水中性粒细胞>100 00×10 6 /L,糖<0.5g/L,蛋白>10g/L,抗生素治疗无效,腹水可分离出2种以上病原体,以及不常见病原体如厌氧菌及真菌。
3.肝肾综合征
顽固性腹水患者出现少尿、无尿、氮质血症、低血钠、低尿钠,考虑出现肝肾综合征。国际腹水协会诊断标准:①肝硬化腹水;②血清肌酐>133μmol/L(1.5mg/dl)。其中I型HRS:2周内血清肌酐成倍上升,>226μmol/L(2.5mg/dl);③停止使用利尿剂和使用白蛋白[1g/(kg·d),最多100g/d]扩容治疗后2天,血清肌酐水平无改善(降低到1.5mg/dl或以下);④未出现休克,或近期使用过肾毒性或血管扩张药物;⑤无肾实质病变(蛋白尿<500mg/d),无微小血尿(<50红细胞/HPF)和(或)无超声波肾脏异常发现。应与非甾体类消炎药、环孢素和氨基糖苷类药物的应用引起的医源性肾衰区分开来。
4.原发性肝癌
患者出现肝大、肝区疼痛、有或无血性腹水、无法解释的发热要考虑此病,血清甲胎蛋白持续升高而ALT正常或B超提示肝占位病变时应高度怀疑,CT或MRI可确诊。
5.肝性脑病
主要诊断依据为:①有严重肝病史和(或)广泛门体侧支循环分流;②出现精神紊乱、昏睡或昏迷;③有常见的诱因;④存在明显肝功能损害或血氨增高。以精神症状为唯一突出表现的HE易被误诊为精神病,因此凡遇精神错乱患者,应警惕HE的可能性。肝性昏迷还应与可引起昏迷的其他疾病,如代谢性疾病(糖尿病、低血糖、糖尿病酸中毒、Wilson病)、缺氧、高(低)钠血症、尿毒症、颅内损伤/创伤、脑血管意外(颅内出血、硬膜下和硬膜外血肿)、脑部肿瘤或感染、癫痫、中毒、酒精相关性、某些药物(镇静剂、催眠药、麻醉剂等)、特殊的营养缺乏(维生素B 1 )等相鉴别。诊断CHE前提是除外症状性 HE。对于“高危人群”,我国专家推荐采用数字连接试验(number connect test-A,NCT-A)、数字-符号试验(number-digit test,DST),两者均阳性可做出诊断。有条件者可进行试磁共振波谱(MRS)、fMRI和临界视觉闪烁频率(CFF)等检查。
6.肝肺综合征
有上述HPS临床表现,立位呼吸室内空气时动脉氧分压<70mmHg或肺泡-动脉氧梯度>20mmHg。下述试验提示肺血管扩张有助于作出诊断:①超声心动图气泡造影左心房有延迟出现的微气泡(心搏4~6次后);②肺扫描阳性。前者敏感性高,后者特异性高。HPS应与肺动脉高压相鉴别,后者有进行性呼吸困难,心前区疼痛而发绀少见,体检肺动脉瓣区第2音亢进,杂音向胸骨左缘传导,X线显示心脏扩大,心脏超声提示右室肥厚,心导管检查可确诊。
7.肝硬化性心肌病
诊断标准为患者有隐匿性收缩功能不全,表现在运动、血容量变化、药物刺激时,心输出量的增加受阻,休息时射血分数(ejection fraction,EF)<55%;舒张功能不全,表现为E/A比例<1.0、减速时间延长(>200毫秒)、等容舒张时间延长(>80毫秒);以及有Q-T间期延长、左心房扩大等。
【治疗】
(一)治疗原则
肝硬化疾病的发展是一个动态的过程,治疗主要是预防和治疗肝硬化的并发症。针对病因进行治疗常可以改善肝脏结构和功能,进而逆转或减慢肝硬化的进程。如酒精性肝硬化患者必须戒酒,乙型肝炎和丙型肝炎肝硬化者须行抗病毒治疗,忌用对肝脏有损害的药物。
(二)一般治疗
1.休息
代偿期患者可参加轻工作,失代偿期尤其出现并发症患者应卧床休息。由于直立体位激活RAAS及交感神经系统引起肾小球滤过减少和钠潴留。因此,卧床休息对于肝硬化腹水的住院患者有一定益处。
2.饮食
肝硬化是一种慢性消耗性疾病,目前已证实营养疗法对于肝硬化患者特别是营养不良者降低病残率及死亡率有作用。肝硬化患者的饮食热量为35~40kcal/(kg·d),其中碳水化合物占45%~65%,蛋白质1~1.5g/(kg·d)。应给予高维生素、易消化的食物,增加一次夜宵,严禁饮酒。可食瘦肉、河鱼、豆制品、牛奶、豆浆、蔬菜和水果。盐和水的摄入应根据患者水及电解质情况进行调整,食管静脉曲张者应禁食坚硬粗糙食物。
(三)病因治疗
1.抗病毒治疗
代偿期乙肝肝硬化患者HBV DNA>2000U/ml(ALT可正常)应抗病毒治疗。治疗目标是延缓和降低肝功能失代偿和HCC的发生。失代偿期乙肝肝硬化患者无论HBV DNA是否阳性、ALT是否升高,均需要长期甚至终生口服抗病毒效力强不易耐药的核苷类似物如恩替卡韦或替诺福韦抗病毒治疗。治疗目标是通过抑制病毒复制,改善肝功能,以延缓或减少肝移植的需求。服药期间须随访。代偿期患者肝功能好的在严密监测下也可选择干扰素,疗程1年。
新一代口服直接抗丙肝病毒药物(direct-acting antiviral drugs,DAAs)的问世,使HCV感染的治愈率达到90%以上。对进展性肝纤维化和失代偿期肝硬化应首先考虑该类药抗丙肝病毒治疗。后者服药后,如能达到持续性病毒反应(SVR),则可以改善 MELD和Child-Pugh评分,逆转失代偿症状,改善生存。但是其SVR明显低于代偿期肝硬化患者,特别是严重失代偿和门脉高压患者。
2.抗纤维化药物
针对病因的治疗例如抗病毒治疗能够逆转和减轻肝纤维化。中西医结合肝纤维化诊治指南推荐扶正化瘀胶囊和复方鳖甲软肝片等药物,有抗纤维化作用。
3.其他
酒精肝需戒酒、肝豆状核变性驱铜治疗、非酒精性脂肪性肝病针对代谢综合征的治疗等。
(四)腹水的治疗
腹水患者的治疗主要是减轻由于腹水或下肢水肿给患者带来的不适并防止腹水引起的并发症,如SBP、脐疝的破裂以及进一步发展为肝肾综合征。因此主要目的是减少腹水以及预防复发。应测定体重、血清电解质、肾功能及24小时尿钠、尿钾排出量,以指导治疗。
1.腹水的一般治疗
(1)控制水和钠盐的摄入:
对有轻度钠潴留者,钠的摄入量限制在88mmol/d(5.0g食盐)可达到钠的负平衡。应用利尿剂时,可适度放开钠摄入,以尿钠排出量为给药指导。轻中度腹水在限钠饮食和卧床休息后可自行消退。稀释性低钠血症(<130mmol/L),应限制水的摄入(800~1000ml/d)。
(2)利尿剂的应用:
经限钠饮食和卧床休息腹水仍不消退者须应用利尿剂,建议采用螺内酯与呋塞米的联合治疗,而不是序贯治疗(先使用螺内酯,随后加入呋塞米)。通常最初给予螺内酯100mg和呋塞米40mg,每日早晨给药1次。对于腹水量少的瘦小的患者,可采用更低剂量(例如,螺内酯50mg和呋塞米20mg)。若应用3~5日后临床效果不明显或体重减轻程度不理想,则药物剂量可分别增加100mg和40mg。若有需要,可以重复进行增量。推荐的最大剂量为螺内酯400mg/d和呋塞米160mg/d。服药后体重下降为有效(无水肿者每天减轻体重500g,有下肢水肿者体重减轻1000g/d)。体重下降过多时,利尿剂需要减量。对于肾实质疾病患者,应用低于100mg/40mg比例的螺内酯与呋塞米(例如,100mg/80mg或100mg/120mg)。需要反复尝试来确定剂量,以达到不伴高钾血症的尿钠排泄。在某些情况下,不能使用螺内酯,特别是在肾小球滤过率极低或患者出现高钾血症时。避免采用静脉给予呋塞米,因为静脉给予呋塞米可能导致急性肾功能减退并可以导致逐渐加重的氮质血症,随后可能造成肝肾综合征假象。如出现肝性脑病、低钠血症(血钠<120mmol/L)、肌酐>120mmol/L应停用利尿剂,可用胶体或盐水扩容或用V s 受体拮抗剂托伐普坦,但须避免24小时血钠上升>12mmol/L。最新指南不推荐托伐普坦用于肝硬化患者低钠血症的常规治疗。
(3)提高血浆胶体渗透压:
对于低蛋白血症患者,每周定期输注白蛋白、血浆可提高血浆胶体渗透压,促进腹水消退。
对于血压逐渐下降的进行性肝硬化患者,停用或避免开始使用血管紧张素转换酶抑制剂(ACEI)、血管紧张素Ⅱ受体拮抗剂(ARB)及β受体阻断药(β-RB),对于顽固性腹水患者不使用β受体阻断药。应避免使用前列腺素抑制剂,如非甾体类抗炎药(NSAIDs),因为这些药物可以降低尿钠排泄并诱发氮质血症。
2.顽固性腹水的治疗
对大剂量利尿剂(螺内酯400mg/d,呋塞米160mg/d)缺少反应(无体重下降)或在小剂量利尿剂时就发生肝性脑病、低钠、高钾等并发症,均属于顽固性或难治性腹水(refractory ascites),其在失代偿期肝硬化患者中的发生率为10%。治疗首先应针对导致顽固性腹水发生的一些可逆性原因,如:不适当的限钠、利尿;使用肾毒性药物;自发性细菌性腹膜炎;门静脉、肝静脉栓塞及未经治疗的活动性肝病。还可以用下列方法治疗。
(1)排放腹水、输注白蛋白:
对于顽固性大量腹水患者,如无其他并发症(肝性脑病、上消化道出血、感染)、肝储备功能为Child-Pugh A、B级,无出血倾向(INR<1.6,血小板计数>50×10 9 /L)可于1~2小时内抽排腹水4~6L,同时补充白蛋白6~8g/L腹水,以维持有效血容量,阻断RAAS系统激活。一次排放后仍有腹水者可重复进行,该方法腹水消除率达96.5%,排放腹水后应用螺内酯维持治疗。
(2)经颈静脉肝内门体分流术:
经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt,TIPS)是目前治疗顽固性腹水患者最有效的措施。术后门脉压力下降,阻断钠潴留,改善肾脏对利尿剂反应。可预防腹水复发;适应证是肝功能损害轻度而门脉高压显著者。终末期肝病模型(model of end-stage liver disease,MELD)积分≥15的患者不宜做TIPS,应该考虑肝移植(MELD积分=9.6log(肌酐 mg/dl)+3.8(胆红素 mg/dl)+11.2log(INR)+6.4)。
(五)并发症的治疗
1.胃底食管静脉破裂出血
胃底食管静脉破裂出血是肝硬化严重并发症和死亡主要原因,应予以积极抢救。
(1)重症监护:
卧床、禁食、保持气道通畅、补充凝血因子、迅速建立静脉通道以维持循环血容量稳定,密切监测生命体征及出血情况。必要时输血。短期应用抗生素,不仅可以预防出血后感染,特别如SBP,还可提高止血率、降低死亡率。可先予静脉用头孢曲松1g/d,能进食时口服环丙沙星0.4g,2次/天,共7天。
(2)控制急性出血
1)血管活性药物治疗:
一旦怀疑食管-胃静脉破裂出血,应立即静脉给予下列缩血管药物,收缩内脏血管,减少门静脉血流量,达到止血效果。诊断明确后继续用3~5天。常用药物有14肽生长抑素,首剂250μg静脉推注,继以250μg/h持续静脉点滴;8肽奥曲肽,首剂100μg静脉推注,继以25~50μg/h持续静脉滴注,必要时剂量加倍;三甘氨酰赖氨酸加压素(特利加压素)静脉注射,1~2mg,q6~8h;垂体后叶素(VP)0.4U/min静脉滴注。VP不良反应多,有腹痛、血压升高、心绞痛等,有心血管疾病者禁用。如要使用应合并硝酸甘油0.3~0.6mg(舌下含化或静脉滴),可减少VP不良反应,增强降门脉压力作用。
2)气囊压迫术:
使用三腔管对胃底和食管下段作气囊填塞。常用于药物止血失败者。压迫总时间不宜超过24小时,否则易导致黏膜糜烂。这项暂时止血措施,可为急救治疗赢得时间,也为进一步做内镜治疗创造条件。
3)内镜治疗:
经过抗休克和药物治疗血流动力学稳定者应立即送去做急症内镜检查,以明确上消化道出血原因及部位。如果是食管静脉曲张性出血,应予以内镜下硬化剂注射止血或者使用皮圈进行曲张静脉套扎术(endoscopic varix ligation,EVL);若胃静脉出血,宜注射组织胶。

(资源58) 内镜治疗(视频)
4)急症手术:
上述急症治疗后仍出血不止,患者肝脏储备功能为Child-Pugh A级者可行断流术。
5)介入治疗:
上述患者如无手术条件者可行TIPS作为救命的措施。术后门脉压力下降,止血效果好,但易发生肝性脑病和支架堵塞。覆膜支架不仅可以控制出血和预防再出血,还可以延长生存期。对胃静脉曲张活动性出血药物和内镜治疗无效时可紧急做经皮经肝曲张静脉栓塞术。
(3)预防再出血:
在第一次出血后,一年内再出血的发生率约70%,死亡率约30%~50%,因此在急性出血控制后,应采用以下措施预防再出血。
1)内镜治疗:
单纯食管静脉曲张,可用EVL与硬化剂治疗,胃静脉曲张注射组织胶。推荐与药物联合应用。
2)药物治疗:
非选择性β受体阻断药(普萘洛尔、纳多洛尔、替莫洛尔)通过其β受体阻滞作用,收缩内脏血管,降低门静脉血流量而降低门静脉压力(HVPG平均下降15%)。与对照组相比,预防出血效果确切。用法:普萘洛尔从10mg/d开始,每日增加10mg,直至静息时心率下降到基础心率的75%,作为维持剂量,长期服用,并根据心率调整剂量。15%患者有禁忌证(窦性心动过缓,支气管哮喘,慢性阻塞性肺部疾病、心力衰竭、低血压、房室传导阻滞、胰岛素依赖性糖尿病)。另外有15%患者不能耐受,出现SBP、顽固性腹水、肾损害、低钠血症(<130m Eq/L)或低血压(<90mmHg)而停用。卡维地洛(carvedilol)作为普萘洛尔的替代药物,通过非选择性β受体阻滞和α1肾上腺能阻滞作用,同时降低门脉血流量和肝血管张力,其降低门脉压力的作用大于普萘洛尔。起始剂量6.25mg/d,1周后增加到维持量12.5mg/d。不良反应有液体潴留、平均动脉压降低,影响长期应用。
3)外科减压或断流:
如果患者为代偿期或Child A级肝硬化,在药物或内镜治疗失败时也可考虑做远端脾肾吻合术或断流术。
4)TIPS:
一线治疗失败后,选择覆膜支架TIPS。食管静脉曲张、Ⅰ/Ⅱ型食管胃静脉曲张出血且药物和内镜治疗失败率高的患者(HVPG>20mmHg、CPC C级<14分或B级合并活动性出血者),应该早期(24小时内)行覆膜支架TIPS,可以延长生存期。
5)肝移植:
终末期肝病伴食管静脉反复出血者是肝移植的适应证。
(4)预防首次出血:
出血高危人群(CPC C级、曲张的食管静脉直径>5mm伴红色征)应选择EVL或药物治疗。药物包括普萘洛尔、卡维地洛等。
2.自发性细菌性腹膜炎
主要致病菌为革兰阴性菌(70%),如大肠埃希菌(47%)、克雷伯杆菌(13%)。由于SBP后果严重,如临床上怀疑SBP或腹水中性粒细胞>250/mm 3 ,应立即行经验性治疗,抗生素首选头孢噻肟2g每12小时1次,静脉滴注或头孢曲松2g每日1次,静脉滴注,在用药后48小时再行腹水检查,如中性粒细胞数减少一半,可认为抗生素治疗有效,疗程5~10天。腹水蛋白<10g/L、已发生过一次SBP以及食管静脉破裂出血者是复发性SBP的高危患者,应口服环丙沙星400mg/d进行预防。SBP最严重的并发症是肝肾综合征。一旦诊断SBP立即给予白蛋白输注1.5g/(kg·d),48小时后1g/(kg·d),可预防HRS,提高生存率。
3.肝肾综合征
治疗原则是增加动脉有效血容量和降低门静脉压力,在积极改善肝功能前提下,可采取以下措施:①早期预防和消除诱发肝肾衰竭的因素,诸如感染、出血、电解质紊乱、不适当的放腹水、利尿等;②避免使用损害肾功能的药物;③输注白蛋白1g/kg/24h,以后20~40g/24h,持续5~10天,使血 Cr<132.6μmol/L;④血管活性药物特利加压素0.5~2mg静脉注射(缓慢静脉推注1小时或用输液泵),12小时1次,通过收缩内脏血管,提高有效循环血容量,增加肾血流量,增加肾小球滤过率,阻断RAAS激活,降低肾血管阻力。也可用去甲肾上腺素(0.5~3mg/h)或米多君(2.5~3.75mg/d)加奥曲肽(300~600μg/d)代替特利加压素;⑤TIPS有一定帮助,应用对象:SB<51μmol/L、Child-Pugh<12分、无心肺疾患和肝性脑病者;⑥肝移植:对可能发生HRS的高危患者如稀释性低钠血症、低血压、低尿钠患者在发生HRS前行肝移植。
4.肝性脑病
(1)寻找并消除诱因:
及时控制感染和上消化道出血并清除积血,避免快速和大量的排钾利尿和放腹水。注意纠正水、电解质和酸碱平衡失调。缓解便秘,并控制使用麻醉、止痛、安眠、镇静等药物。当患者狂躁不安或有抽搐时,禁用吗啡及其衍生物、水合氯醛、哌替啶及速效巴比妥类。必要时可减量使用(常量的1/2或1/3)地西泮(安定)、东莨菪碱,并减少给药次数。异丙嗪、氯苯那敏(扑尔敏)等抗组胺药有时可作为安定替代药。
(2)乳果糖:
乳果糖在结肠内被乳酸菌、厌氧菌等分解为乳酸和醋酸,降低结肠pH,使肠腔呈酸性,从而减少氨的形成与吸收;其轻泻作用有助于肠内含氮毒性物质的排出;肠道酸化后,促进乳酸杆菌等有益菌大量繁殖,抑制产氨细菌生长,氨生成减少。剂量为每次15~30ml,每日3~4次口服。从小剂量开始,根据2~3次软便/天,调整剂量。严重肝性脑病时,可用乳果糖置入鼻胃管给药,一般为15~45ml每8~12小时1次;或乳果糖300ml置于1 L水中灌肠保留1小时,每2小时1次,直到症状改善。乳果糖还可以用于复发性HE的预防,其可以改善MHE患者的认知和生活质量,用于CHE的治疗。
(3)抑制肠道细菌生长:
利福昔明-α是一种口服后肠道吸收极少的广谱抗生素,其对肝性脑病有良好的疗效,具有耐受性好、起效快等优点。可作为Ⅰ~Ⅲ度肝性脑病的治疗和预防复发性HE发作,推荐剂量是800~1200mg/d,分次口服或与乳果糖合用。
含有双歧杆菌、乳酸杆菌等的微生态制剂可起到维护肠道正常菌群、抑制有害菌群、减少毒素吸收的作用。
(4)促进氨的转化和代谢:
L-鸟氨酸-L-天门冬氨酸(OA)中的鸟氨酸能增加氨基甲酰磷酸合成酶和鸟氨酸氨基甲酰转移酶活性,其本身也是鸟氨酸循环的重要物质,可促进尿素合成。天门冬氨酸可促进谷氨酰胺合成酶的活性,促进脑、肝、肾的利用和消耗氨以合成谷氨酸和谷氨酰胺而降低血氨,减轻脑水肿。每日静脉滴注20g,用于OHE,能显著降低 HE患者血氨,改善临床症状,安全性好。
5.肝肺综合征
内科治疗无效,TIPS可改善患者症状,为肝移植创造条件。
6.肝硬化性心肌病
治疗非特异性,主要针对左心室衰竭,肝移植是唯一可治疗的手段。
7.门静脉血栓形成
新近出现或进展性门静脉血栓(portal vein thrombosis)形成,早期可行低分子肝素抗凝治疗,抗凝前对有高危的静脉曲张者应给予β受体阻断药或EVL预防出血。用药2~3个月后影像学评估,如血栓形成继续进展,考虑TIPS;如有改善或稳定,继续抗凝直到肝移植。如果是稳定的陈旧性血栓或有门静脉海绵样变,在影响肠系膜上静脉的流量并且有易栓症情况下,进行抗凝;如不存在易栓症,影像学随访如血栓有进展,抗凝治疗。陈旧性血栓或有门静脉海绵样变的患者,肠系膜上静脉的流量未受影响的,则常规随访不必治疗。
8.原发性肝癌
见本章第八节“肝肿瘤”。
【预后】
肝硬化临床1到5期的年死亡率分别为1%,3.4%,20%,57%,>60%。Child-Pugh分级也与预后密切相关,1年和2年的估计生存率分别为Child-Pugh A级100%,85%;B级80%,60%;C级为45%,35%。呕血、黄疸、腹水是预后不良因素。肝移植的开展已明显地改变了肝硬化患者的预后。移植后患者1年生存率90%、5年生存率80%,生活质量大大提高。
【预防】
针对病因的防治,可以防止或者延迟肝硬化的形成和并发症的发生。在我国肝硬化的病因主要为慢性乙型病毒性肝炎,因此防治乙肝是预防本病的关键。新生儿和高危人群应注射乙肝疫苗,乙肝患者给予积极的抗病毒治疗;严格执行器械的消毒常规,严格选择献血员;节制饮酒;注意合理的营养;避免应用对肝脏有损害的药物;加强劳动保健;避免工农业生产中的各种慢性化学品中毒;定期体格检查,无疑也是预防本病的积极措施。
主要参考文献
1.中华医学会消化病学分会,中华医学会肝病学分会.中国肝性脑病诊治共识意见(2013年,重庆).中华消化杂志,2013,33(9):581-591.
2.Lee SS.Cirrhosis:A practical guide to management.Gastroenterology,2015,17(6):166-179.
3.Garcia-Tsao G:Ascites and its complications in Podolsky DK,Camilleri M,Fitz JG er al eds,Yamada's Textbook of Gastro-enterology 6th ed.Oxford:Wiley Blackwell,2016.2087-2106.
4.Tsochatzis EA,Bosch J,Burroughs AK.Liver cirrhosis.Lancet,2014,17;383(9930):1749-1761.
5.Tripathi D,Stanley AJ,Hayes PC,et al.UK guidelines on the management of variceal haemorrhage in cirrhotic patients.Gut,2015,64(11):1680-1704.
第二节
药物性肝病

郭津生 王吉耀
药物性肝病(drug induced liver disease,DILD)是指药物或(及)其代谢产物引起的不同程度和类型的肝损害,又称为药物性肝损伤(drug-induced liver injury,DILI),是引起肝损伤的常见病因。目前已发现有上千种药物有潜在肝毒性(见Liver Tox和Hepa Tox网站),包括了医学处方药物及人们因治疗、营养等目的使用的非处方药物、中草药、保健品、膳食补充剂。不同药物可导致相同类型肝损伤,同种药物也可导致不同类型的肝损伤。DILI约占所有药物不良反应的6%,急性肝炎的5%,非病毒性慢性肝炎的20%~50%,是引起暴发性肝衰竭的重要病因之一(50%以上)。
DILI中只有少部分由剂量依赖的毒性药物引起,而绝大多数是在推荐剂量下发生的个体对药物或其代谢产物的特异质性反应,难以预测,无特异性诊断标志物,发病与遗传易感因素、药物的理化和毒理性质、以及环境因素有关。
【发病机制】
肝是药物清除、生物转化和分泌的主要场所。肝常能通过多种机制适应低水平的肝毒性,然而当药物代谢过程中毒反应性产物的产生超过他们能安全排泄的速率时就会引起肝损伤。DILI的机制还包括药物本身的毒性、免疫过敏机制、代谢过程中由肝实质摄取、经胆盐及有机阴离子的转运和排出异常等方面。
(一)非免疫机制
某些药物(如对乙酰氨基酚)在肝内P450酶作用下可转化为毒性代谢产物,产生亲电子基和氧自由基,引起肝内谷胱甘肽耗竭,并与蛋白质、核酸和脂质等大分子物质共价结合,引起脂质过氧化,破坏线粒体、细胞骨架、微管、内质网及细胞核功能,结果导致肝细胞变性、坏死、凋亡和对炎症介质的敏感性增高。如果药物及其代谢产物引起肝窦底侧膜的摄取障碍、肝细胞分泌胆汁功能破坏和毛细胆管膜上的转运器的功能障碍,则可导致药物性胆汁淤积。
(二)免疫过敏机制
药物反应性代谢产物可通过改变肝细胞的蛋白质形成新抗原、以半抗原复合物形式获得抗原性、诱导自身抗体的产生等启动细胞免疫和(或)体液免疫反应,引起免疫介导的肝损伤。
(三)易感因素
许多获得和遗传性因素与药物性肝损伤的发生危险性有关:①年龄(老龄);②性别(女性);③慢性酒精摄入;④药物的化学性质、剂量、疗程以及药物间协同作用;⑤基础疾病(肝脏疾病和代谢紊乱)等。对于老年人、新生儿、营养不良者和已患有肝、肾疾病的患者应适当调整用药剂量;⑥宿主遗传因素:一些与药物生物转化、解毒以及免疫反应过程相关基因(如细胞色素P450、跨膜转运蛋白、溶质转运蛋白、解毒酶、免疫因子、HLA等)的单核苷酸多态性与特异质性药物性肝损伤相关。
【病理】
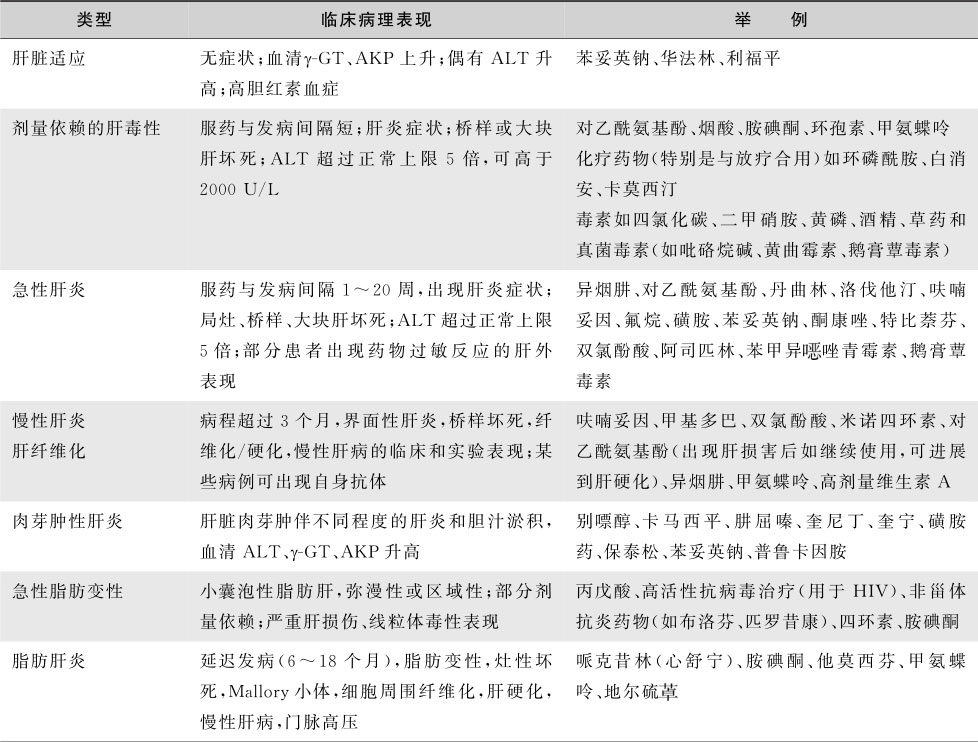
DILI可引起所有类型的肝损伤病理变化,包括坏死性肝炎、胆汁淤积、脂肪变、血管损伤和肝肿瘤(表15-8-3)。而肝内所有细胞均会受到药物的影响,有些药物甚至可能出现多种损伤表现。临床较多见的是类似急性黄疸性肝炎和胆汁淤积性肝病的症状和实验室检查异常。
表15-8-3 药物性肝病的临床病理表现
续表
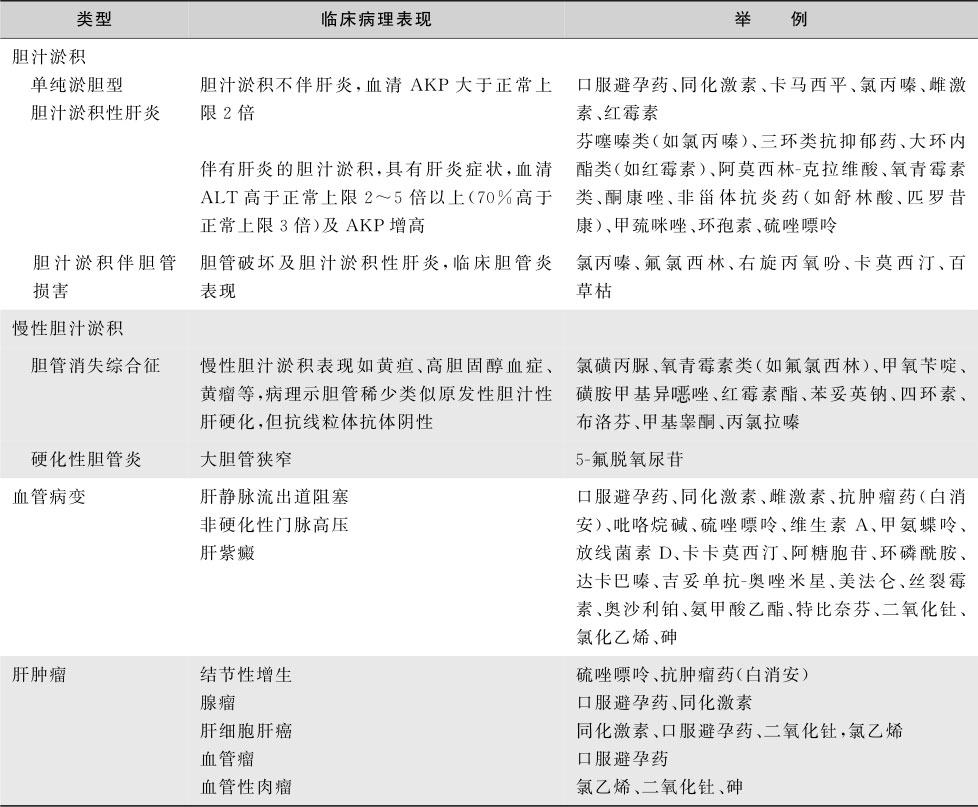
注:γ-GT:谷氨酰转肽酶;AKP:碱性磷酸酶;ALT:丙氨酸氨基转移酶
【临床表现和实验室检查】
(一)临床表现
DILI可因肝损伤药物的种类及机制不同而出现所有急、慢性肝胆疾病的类似表现(表15-8-3)。而最多见的是急性肝炎型和胆汁淤积型。
急性肝炎表现为主者常有全身症状如发热、乏力、食欲缺乏、黄疸和血清氨基转移酶增高达正常上限(ULN)2~30倍,ALT/AKP≥5,高胆红素血症和凝血酶原时间延长与肝损伤严重度相关。病情较轻者,停药后短期能恢复(数周至数月)。重者发生暴发性肝衰竭,出现进行性黄疸、凝血异常和肝性脑病,常发生死亡。药物性肝损伤是引起急性肝衰竭的最常见原因之一。
以胆汁淤积为主的DILI其临床与实验室表现主要为黄疸和瘙痒,可伴有发热、上腹痛、右上腹压痛及肝大,伴血清氨基转移酶轻度增高而AKP明显增高达正常上限2~10倍,ALT/AKP≤2,结合胆红素明显升高(34~500μmol/L),胆盐、脂蛋白X、γ-GT及胆固醇升高,而抗线粒体抗体阴性。一般于停药后3个月到3年恢复,少数可进展为胆汁淤积性肝硬化。混合型ALT≥3ULN,AKP≥2ULN,2<ALT/AKP<5。
以过敏反应为主的急性DILI,常有发热、皮疹、黄疸、淋巴结肿大,伴血清氨基转移酶、胆红素和AKP中度增高,药物接触史常较短(4周以内)。疾病严重程度与药物剂量之间无肯定联系;再次给药时,不仅疾病严重度增加,潜伏期也缩短,患者血清中存在自身抗体为其特点。
慢性DILI在临床上可表现为慢性肝炎、肝纤维化、代偿性和失代偿性肝硬化、AIH样DILI、慢性肝内胆汁淤积和胆管消失综合征等,还可出现肝窦阻塞综合征/肝小静脉闭塞病(SOS/VOD)及肝脏肿瘤。SOS/VOD也可呈急性,并有腹水、黄疸、肝大等表现。
(二)严重程度分级
可分为0~5级。
0级:无肝损伤,患者对暴露药物可耐受,无肝毒性反应。
1级:轻度肝损伤,血清ALT和(或)AKP呈可恢复性升高,总胆红素(TBil)<2.5倍正常值上限(ULN),且国际标准化比值(INR)<1.5。多数患者可适应。可有或无乏力、虚弱、恶心、厌食、右上腹痛、黄疸、瘙痒、皮疹或体重减轻等症状。
2级:中度肝损伤,血清ALT和(或)AKP升高,总胆红素(TBil)≥2.5×ULN,或虽无 TBil升高但INR≥1.5。上述症状可有加重。
3级:重度肝损伤,血清ALT和(或)AKP升高,TBil≥5×ULN,伴或不伴INR≥1.5。患者症状进一步加重,需要住院治疗,或住院时间延长。
4级:急性肝衰竭(ALF),血清ALT和(或)AKP水平升高,TBil≥10×ULN(171μmol/L)或每日上升≥17.1μmol/L,INR≥2.0或凝血酶原活动度<40%,可同时出现:①腹水或肝性脑病;或②与DILI相关的其他器官功能衰竭。
5级:致死性,因DILI死亡,或需接受肝移植才能存活。
(三)临床分型
1.发病机制分型
①固有型:可预测,与药物剂量密切相关,个体差异不显著;②特异质型:临床上较为常见和多样化,不可预测,个体差异显著。又分免疫特异质性和遗传特异质性。前者有免疫反应特征,通常起病较快。
2.病程分型
①急性:占绝大多数;②慢性:定义为发生6个月后血清ALT、AST、AKP及TBil仍持续异常,或存在门静脉高压或慢性肝损伤的影像学和组织学证据。
3.受损靶细胞类型分类
由国际医学组织理事会(CIOMS)初步建立后经修订,通过计算R值进行临床分型 和观测演变。R=(ALT实测值/ALT ULN)/(AKP实测值/AKP ULN)。可分为①肝细胞损伤型:ALT≥3×ULN,且R≥5;②胆汁淤积型:ALT≥2×ULN,且 R≤2;③混合型:ALT≥3×ULN,AKP≥2×ULN,且2<R<5;④肝血管损伤型:相对少见,靶细胞可为肝窦、肝小静脉和肝静脉主干及门静脉等的内皮细胞。表现为肝窦阻塞综合征/肝小静脉闭塞病(SOD/VOD),紫癜性肝病(PH)、巴德-吉(基)亚利综合征(Budd-Chiari综合征,BCS)、可引起特发性门静脉高压症(IPH)的肝汇管区硬化和门静脉栓塞、肝脏结节性再生性增生(NRH)等。
【诊断与鉴别诊断】
DILI的诊断主要根据服药史、发病过程与服药的时间有相关性的特点并排除其他肝损伤因素作出综合诊断。完整的诊断应包括诊断名、临床类型、病程、RUCAM评分结果、严重程度分级。
(一)用药史和危险因素
1.用药史
需了解发病前3个月内服过的药物,包括剂量、用药途径、持续时间及同时使用的其他药物。更应详细询问非处方药、中草药及保健品应用情况,此外还应了解患者的职业和工作环境。
中草药引起的肝损伤需引起警示。其毒理学基础包括:①药物及制剂的固有成分、污染物、掺杂物、微生物及重金属等均可能成为引起肝损伤的原因;②用药时间过长造成药物积累,或用量过大造成中毒;③中药材误用或炮制煎煮不当;④中药材滥用、劣药等人为因素;⑤中西药不合理的联合使用等。部分可引起药物性肝损伤的中草药及毒性成分见表15-8-4。对使用中草药对疾病的治疗和可能引起的肝毒性应按照中医药辨证论治的原则和考虑配伍问题。
美国国家糖尿病、消化系统疾病和肾病研究所(NIDDK)药物性肝损伤数据库LiveTox收录草药和膳食补充剂(HDS)项下的具有肝损伤报道品种(表15-8-5),主要是用来减肥、治疗关节炎和便秘的药物。毒性成分大多不明,并具有异质性,也有部分可能因掺杂物和错误标签所致。
表15-8-4 可引起药物性肝损伤的中草药和毒性成分

续表
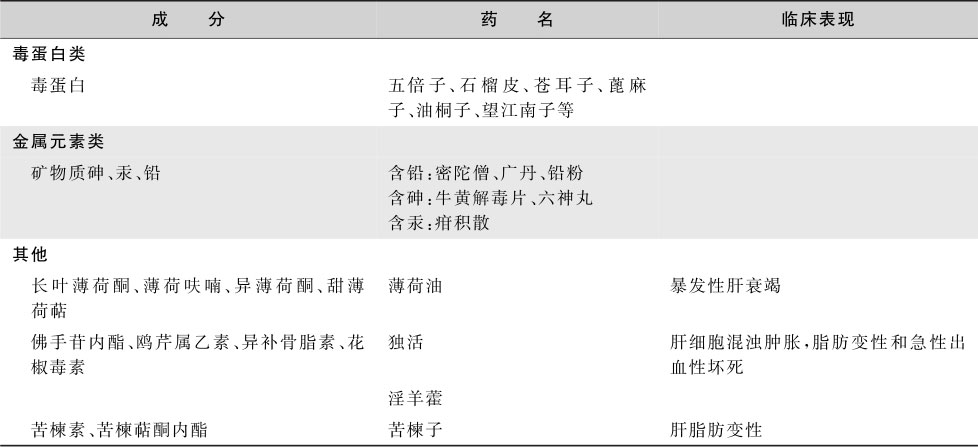
表15-8-5 LiverTox数据库中有肝毒性报道的草药和膳食补充剂
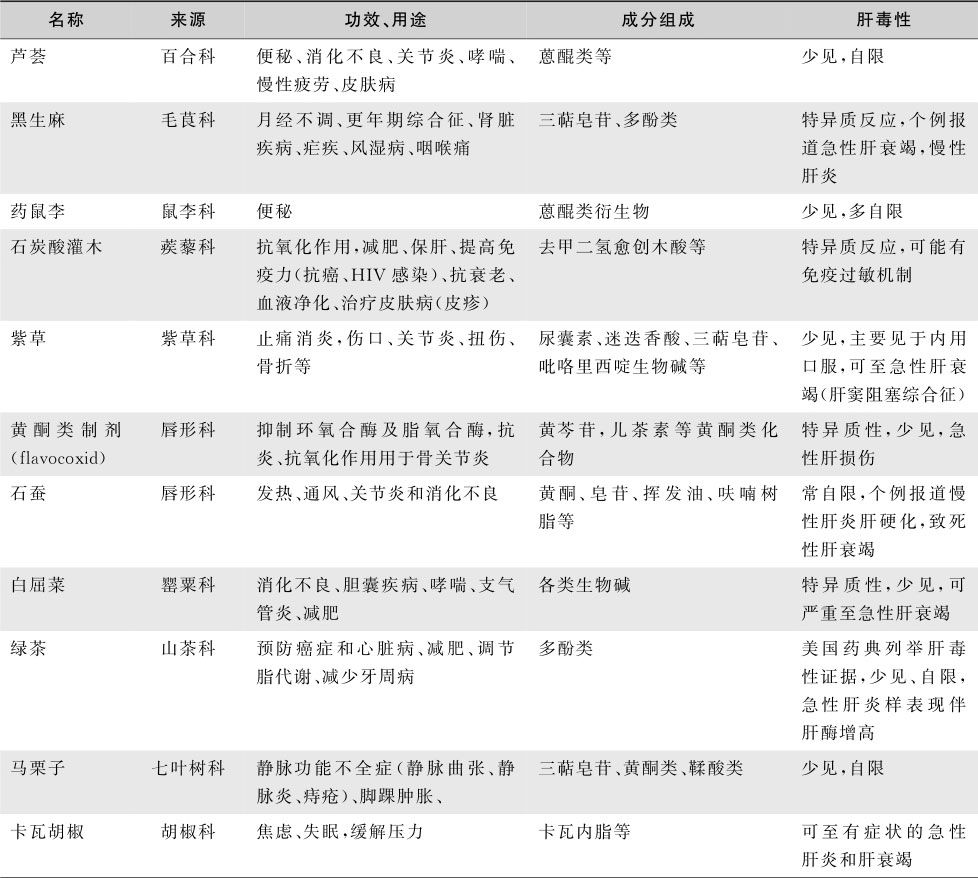
续表
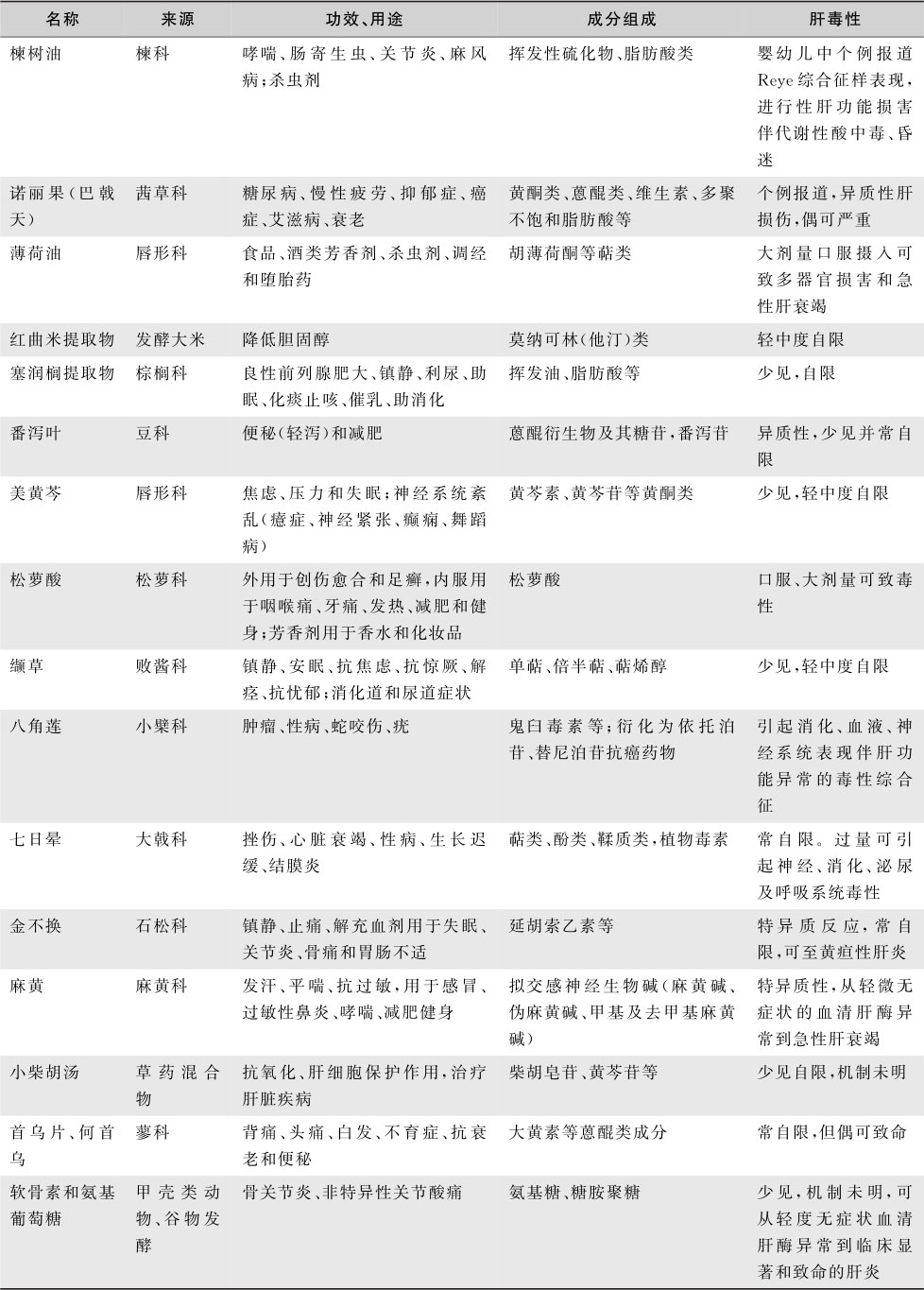
临床支持DILI的诊断依据有:使用已知有肝毒性的药物(如化疗、抗结核、某些抗生素类药物);血液药物分析阳性(如对乙酰氨基酚-蛋白加合物,吡咯-蛋白加合物、维生素A);肝活检有药物沉积(如维生素A自发荧光)及小囊泡性脂肪肝、嗜伊红细胞、小叶中央坏死、胆管损伤等肝损伤证据。
2.危险因素
包括:①肝病史:原来有无病毒性肝炎和其他肝病的证据;②原发病:是否有可能累及肝;③年龄大于50岁;④使用多种药物。
3.时序特点
包括以下几个方面:①可疑药物的给药到出现肝损伤的时间间隔多在1~12周。但既往已有对该种药物的暴露史或致敏史的患者可能在较短的时间内发病(1~2天)。1年以前服用的药物基本排除是急性肝炎的诱因。②停药后肝功能异常和肝损伤好转,常常数周内完全恢复。如果停药后临床表现在几天内消失而氨基转移酶在1周内下降超过50%以上,则对诊断非常有意义。③偶然再次给予损伤药物引起肝功能再次异常。但不可故意重新给予可疑损伤药物,以免引起严重肝损伤的危险,特别是免疫致敏性肝炎,重新给药有时会引起暴发性肝炎。
(二)药物过敏或过敏性疾病表现
任何相关的过敏反应如皮疹和嗜酸性粒细胞增多对诊断DILI十分重要。药物过敏反应具以下特点:①服药开始后5~90天及距最后一次用药15天之内出现肝功能障碍。②首发症状主要为发热、皮疹、皮肤瘙痒和黄疸等。③发病初期外周血嗜酸性粒细胞上升(达6%以上)或白细胞增加。④药物敏感试验(淋巴细胞培养试验、皮肤试验)为阳性,血清中有自身抗体。⑤偶然再次用药时可再引起肝病。对于药物过敏反应所致的肝病具①④或①⑤者可以确诊;具①②或①③者可以拟诊。
(三)排除其他能够解释肝损伤的病因
排除标准根据肝损伤的类型而有差别:①急性肝炎患者要询问有无肝胆疾病史、酒精滥用史和流行病学上与病毒感染相符合的情况(吸毒、输血、最近外科手术、流行病地区旅行);②对主要的肝炎病毒应进行血清学分析(A、B、C、D、E型肝炎病毒;某些情况下还包括巨细胞病毒、EB病毒和疱疹病毒);③需排除与心功能不全有关的潜在的肝缺血,特别是老年患者;④需通过超声或其他适当的检查手段排除胆道阻塞;⑤还应排除自身免疫性肝炎或胆管炎、一些酷似急性肝炎过程的细菌感染(如弯曲菌属、沙门菌属、李斯特菌属);⑥HIV和AIDS的并发症。年轻患者应排除Wilson病。
诊断DILI的难点在于某些临床表现不典型的病例,如:①药物用于治疗的疾病本身会导致肝异常(如细菌感染);②既往已有慢性肝病;③同时摄入几种肝毒性药物(如联合抗结核治疗);④药物处方难以分析的病例:如自服被认为是安全的药物(中草药)、隐瞒信息(非法药物)、遗忘信息(老年),暴发性或亚暴发性肝炎。
多数情况下诊断DILI不需要肝活检,然而在需要排除其他肝损伤病因和定义至今未知肝毒性药物的损伤等情况下可进行肝活检检查。在疾病早期进行肝活检有助于鉴别病变类型和了解肝损伤程度。
CIOMS或RUCAM量表(表15-8-6)是第一个也是目前所使用的最主要的评估DILI的相对标准化的评分系统,此外还有Maria&Victorino/CDS、Naranjo量表等。
表15-8-6 RUCAM量表
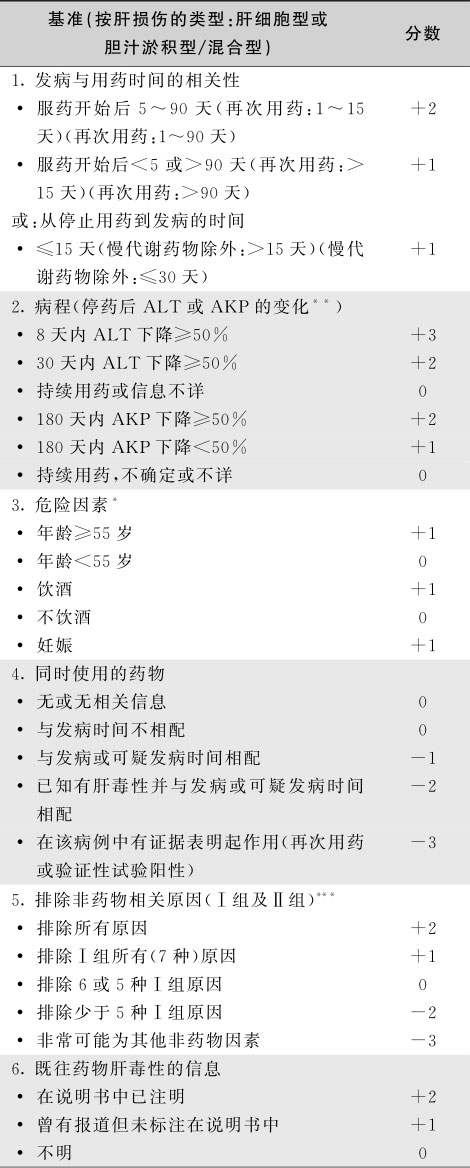
续表

注:CIOMS:国际医学组织理事会;RUCAM:Roussel Uclaf因果关系评估方法
* 有:1分,无:0分
** ALT或AKP的变化:指峰值与正常上限值之差
*** 非药物相关原因:Ⅰ组:7种,包括甲型(HAV)、乙型(HBV)、丙型(HCV)、戊型(HEV)肝炎病毒感染;胆道梗阻;酒精性肝病;低血压或心功能不全;Ⅱ组:5种,包括潜在其他疾病(如败血症、转移性恶性肿瘤、自身免疫性肝炎、慢性乙型或丙型病毒性肝炎、原发性胆汁性胆管炎或原发性硬化性胆管炎、肝脏遗传性疾病);巨细胞病毒(CMV)、EB病毒(EBV)、单纯疱疹病毒(HSV)、水痘-带状疱疹病毒(VZV)感染
【治疗】
(一)预防
药物性肝损害重在预防,应严格掌握药物的适应证,不可滥用。应避免同时使用多种药物,特别是应谨慎使用那些在代谢中有相互作用的药物;尽可能了解将服用的药物与肝损伤的可能关系,避免不必要的服药;避免服药时饮酒(酒精与多种药物合用)。
(二)停用和防止重新给予引起肝损伤的药物
包括属于同一生化家族的药物(以防止有相关化学结构的药物之间的交叉毒性反应)。
(三)早期清除和排泄体内药物
服药6小时内可通过洗胃、导泻(硫酸镁)、吸附(活性炭)等清除胃肠残留的药物。还可采用血液透析(血浆药物浓度高,分布容积低的情况下)、血液超滤(摄取过量在14~24小时以内的患者)、渗透性利尿(血浆药物浓度低,分布容积高,采用血液超滤无效的情况下)促进药物的排泄。
(四)药物治疗
包括抗氧化剂(促进反应性代谢产物的清除)、保护性物质的前体、阻止损伤发生的干预剂或膜损伤的修复剂。常用药物有:①N-乙酰半胱氨酸:对于对乙酰氨基酚过量的患者有特殊疗效,可作为谷胱甘肽的前体或通过增加硫酸盐结合解毒已形成的反应性代谢物,此外还有促进肝内微循环的作用。治疗应尽早,10小时内给药可获最大保护效果。用法:初次口服(或灌胃)140mg/kg,以后每4小时口服70mg/kg,共72小时;或首次静脉滴注150mg/kg(加入5%葡萄糖液200ml内静脉滴注15分钟),以后静脉滴注50mg/kg(500ml/4小时),最后100mg/kg(1000ml/16小时);②还原型谷胱甘肽:补充肝内SH基团,有利于药物的生物转化;③S-腺苷-L-蛋氨酸:通过转甲基作用,增加膜磷脂的生物合成,增加膜流动性并增加Na + -K + -ATP酶活性,加快胆酸的转运。通过转硫基作用,增加生成细胞内主要解毒剂谷胱甘肽和半胱氨酸,生成的牛磺酸可与胆酸结合,增加其可溶性,对肝内胆汁淤积有一定的防治作用。用药方法为每日1~2g静脉滴注;④多烯磷脂酰胆碱:具有保护和修复肝细胞膜作用;⑤熊去氧胆酸(UDCA):有稳定细胞膜、免疫调节及线粒体保护作用,能促进胆酸运输和结合胆红素的分泌,可用于药物性肝损伤特别是药物性淤胆的治疗。用法:0.25g每日3次,口服;⑥甘草酸制剂;⑦皮质激素:可诱导MRP2,从而加速胆红素排泄,可用于胆汁淤积和有免疫高敏感性证据的患者,可采用甲基泼尼松龙30~40mg/d,有效后减量。
对发生DILI的患者应加强支持治疗。卧床休息,密切检测肝功能等指标,特别是监测急性肝衰竭和进展为慢性肝衰竭的征象。酌情补充血浆、白蛋白、支链氨基酸,给予口服新霉素和乳糖,给予预防应激性溃疡的药物。无肝性脑病时给予高热量高蛋白饮食,补充维生素,注意维持水、电解质和酸碱平衡。
胆汁淤积引起的瘙痒、骨病、脂溶性维生素缺乏等的治疗类似于其他胆汁淤积性肝病。
药物引起急性肝衰竭的治疗原则基本同急性重型肝炎。
(五)支持治疗
重症DILI可选择人工肝支持治疗。
(六)肝移植
重症DILI导致肝衰竭、重度胆汁淤积和慢性肝损伤进展到肝硬化时,可考虑肝移植治疗。
主要参考文献
1.中华医学会肝病学分会药物性肝病学组.药物性肝损伤诊治指南.中华肝脏病杂志,2015,23(11):810-820.
2.Danan G,Teschke R.RUCAM in drug and herb induced liver injury:the update.Int J Mol Sci,2015,17(1):14.
第三节
自身免疫性肝病

郭津生 王吉耀
自身免疫性肝病(autoimmune liver diseases,AILD)是一类病因尚不明确,具有自身免疫基础的非化脓性炎症性肝病。自身免疫性肝病的各种疾病在自身免疫的攻击对象、免疫应答类型和临床表现等方面均有各自的特点。根据主要受累的肝细胞类型不同可分为两大类:肝细胞受累的自身免疫性肝炎,胆管细胞受累的自身免疫性胆管病。后者有胆汁淤积的表现,包括原发性胆汁性肝硬化、原发性硬化性胆管炎、IgG4相关硬化性胆管炎。对自身肝脏组织失去耐受性,肝脏出现病理性炎症性损伤的同时,血清中可发现与肝有关的循环自身抗体。
一、自身免疫性肝炎
自身免疫性肝炎(autoimmune hepatitis,AIH),以血清中出现自身抗体(非器官和肝特异)、血清转氨酶和IgG增高(高γ-球蛋白血症)、组织学以界面肝炎、门脉大量浆细胞浸润为特点,常共存有肝外自身免疫性疾病,治疗上对激素等免疫抑制剂等有反应。该病见于所有人种和所有年龄,女性∶男性4∶1,大部分患者年龄>40岁。亚太地区的患病率(40~245)/百万人,年发病率(6.7~20)/百万人。
AIH可根据自身抗体进一步分型。Ⅰ型是最常见的类型,血清抗核抗体(ANA,靶抗原为着丝粒,52k Da SSA/Ro,组蛋白,核糖核蛋白)和抗平滑肌抗体(ASMA,靶抗原为肌动蛋白、微管蛋白、中间丝),或抗可溶性肝抗原/肝胰抗原抗体(抗SLA/LP)阳性;而Ⅱ型主要发生于儿童,肝肾微粒体抗体(LKM,靶抗原为细胞色素单氧化酶P450IID6)和(或)抗肝细胞溶质抗原-1型(抗LC-1)阳性。
【发病机制】
机体对自身组织蛋白失去耐受产生自身抗体及(或)自身致敏淋巴细胞,攻击自身靶抗原细胞和组织,发生病理改变和功能障碍。最为接受的假说是外源性抗原和自身抗原之间的分子模拟,导致自身耐受的破坏和多种AILD出现在同一个体。
1.遗传易感性
主要与人类白细胞抗原(HLA)Ⅰ类分子及Ⅱ类分子有关。其中 HLA DR3(DRB1*0301)及DR4(DQB1*0401)是Ⅰ型AIH的危险因子,而Ⅱ型AIH可能与DR7有关。
2.环境促发因素及抗原交叉反应
一些因素如感染(麻疹病毒、肝炎病毒和EB病毒感染等)、药物和毒素、交叉抗原等可能诱导自身抗体的产生和打破自身耐受,发生针对肝的自身免疫反应。
3.免疫功能异常
从体液免疫角度,AIH患者可能具有抑制性T细胞功能缺陷,不能正常抑制对自身抗原有反应性的B细胞,后者产生针对自身抗原的自身抗体,进一步可通过抗体依赖的细胞介导的细胞毒(ADCC)作用破坏自身细胞。从细胞免疫角度,AIH发生时HLA分子、细胞黏附分子及淋巴细胞功能相关抗原异常表达,细胞因子失衡,T细胞打破耐受而识别自身抗原,导致效应T细胞与靶细胞结合复合体的形成和细胞溶解,引起肝损伤和坏死。
【病理】
肝组织学检查对AIH的诊断和治疗非常重要,可帮助明确诊断、评价肝病分期和分级。
AIH特征性肝组织学表现包括:①界面性肝炎:汇管区和小叶间隔周围肝细胞呈碎片样坏死,伴淋巴细胞、浆细胞为主的炎性细胞浸润,也可出现汇管区-汇管区、小叶中央-汇管区的桥样坏死;②淋巴-浆细胞浸润:主要见于门管区和界面处,也可出现在小叶内;③肝细胞玫瑰花瓣样改变:指数个水样变性的肝细胞形成的假腺样结构,中心有时可见扩张的毛细胆管,形似玫瑰花环,一般见于界面炎周围;④淋巴细胞穿入现象和小叶中央坏死等。
肝细胞的持续坏死刺激胶原结缔组织的增生及肝细胞再生结节的形成,可表现为进展性纤维化、肝硬化。
在肝损害的各个阶段,肝内胆管及毛细胆管损伤、扭曲、受压都可造成胆汁排泄障碍,继而出现胆汁淤积的病理学特征。
以上形态学表现都非自身免疫性肝炎所特有,慢性病毒性肝炎、药物性肝炎都可出现这些征象。当患者出现胆汁淤积、胆管上皮细胞损伤及增生时,病理学不易与PBC、PSC相鉴别。
【临床表现】
(一)发病特点
发病常隐匿性,患者可无症状,或诉说某些症状体征波动长达数月或2年以上。本病也可急性、亚急性甚至暴发性发作,临床上很难与急性病毒性肝炎相区别。急性发病的患者大多先前已有慢性肝损伤过程。
女性患者占多数(80%)。发病的年龄分布呈双峰型,即青春期(15~24岁)和女性绝经期前后(45~64岁)。
年轻患者病情多较严重,糖皮质激素难以控制病情。而年长患者病程趋于缓和,易用免疫抑制剂控制。
(二)症状
最常见的主诉是极度疲乏、嗜睡,其他症状可有厌食、体重减轻、右上腹不适或疼痛、皮肤瘙痒、关节肌肉疼痛、发热等。10%的患者无任何症状。本病常伴有肝外免疫性疾病,一些患者以关节炎的关节疼痛、白癜风、自身免疫性甲状腺疾病、胰岛素依赖性糖尿病就诊,在治疗其他疾病时出现肝病的症状或体征,或发现肝功能异常。
(三)体征
常有显性黄疸,可有肝大、脾大、蜘蛛痣、腹水、周围水肿、呕血及黑便。8%患者以呕血或(和)黑便就诊。30%患者就诊时已有肝硬化。
【实验室检查】
常规肝功能检查结果差异大,可表现为急慢性肝损伤、胆汁淤积。转氨酶和胆红素的水平可以刚刚超过正常上限,也可以高于正常的30~50倍。实验室检查的异常程度与肝活检组织学严重程度可以不一致。伴有胆汁淤积者可有碱性磷酸酶(AKP)和谷氨酸转肽酶(γ-GT)的轻中度升高。
【诊断与鉴别诊断】
应结合临床症状、体征、血清生化、免疫学异常、血清自身抗体以及肝脏组织学等进行综合诊断,并需排除其他引起肝损伤的疾病。
原因不明的肝功能异常和(或)肝硬化患者均应考虑AIH的可能。自身抗体是诊断AIH的重要依据,ANA、ASMA、抗SLA/LP、抗LKM-1、和(或)抗LC-1阳性是诊断AIH的关键部分,对疑似患者应首先进行监测。但自身抗体非AIH特异性,不是本病的病因,抗体滴度也不随治疗而改变,不必连续监测。ANA的特异性最差,也可在PBC、PSC、病毒性肝炎、药物相关性肝炎、酒精和非酒精性脂肪肝患者中检出。拟诊AIH时应常规检测血清IgG和(或)γ-球蛋白水平,对诊断和观察治疗应答有重要价值。AIH特征性肝组织表现包括界面性肝炎、淋巴-浆细胞浸润、肝细胞玫瑰花环样改变等,应尽可能对拟诊AIH的患者进行肝组织学检查以明确诊断。
(一)诊断标准
AIH的明确和疑似诊断标准见表15-8-7。诊断不明的患者也可根据临床表现和影响因素经过积分系统进行诊断(表15-8-8),并通过累积分数反映激素治疗前后诊断的准确性。2008年提出简化积分系统(表15-8-9),具有较低的敏感性和较高的特异性。
表15-8-7 AIH诊断标准(Czaja & Freese,2002)
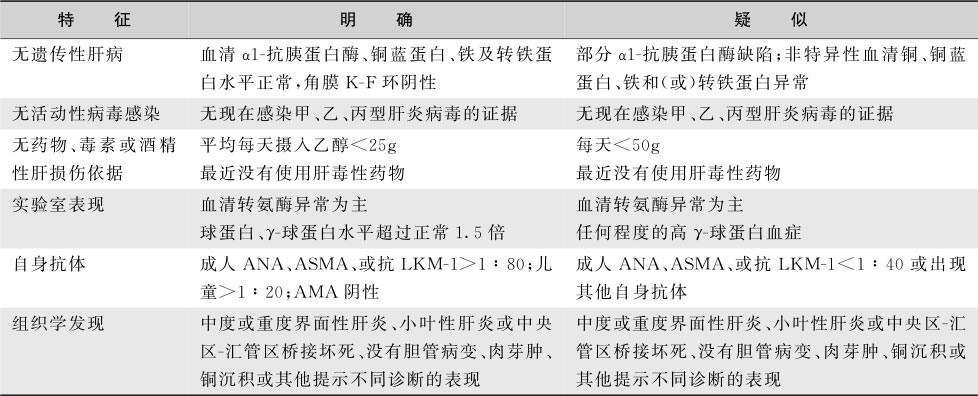
表15-8-8 成人不典型AIH的诊断积分系统(Czaja&Freese,2002)
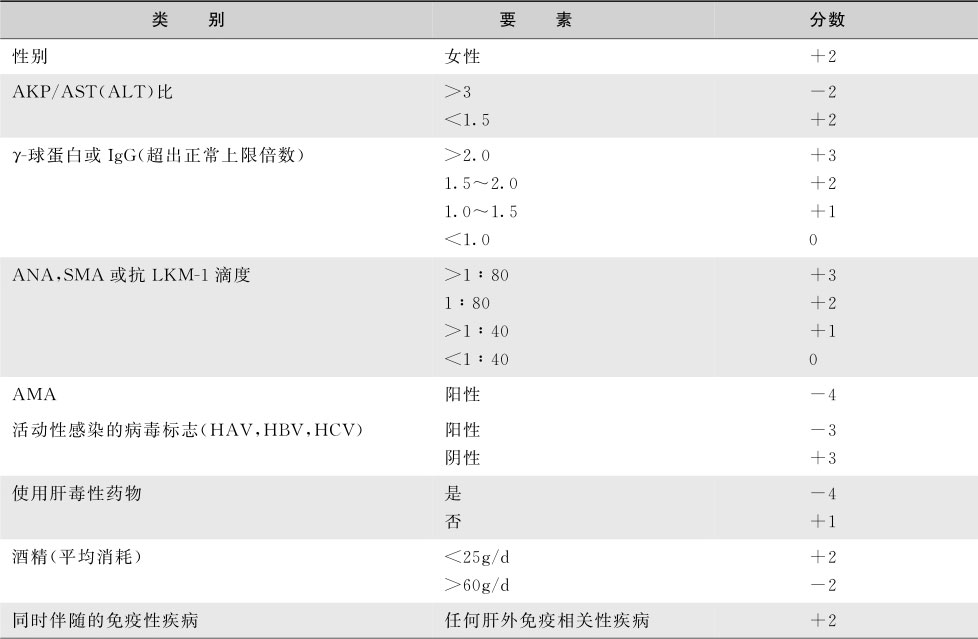
续表
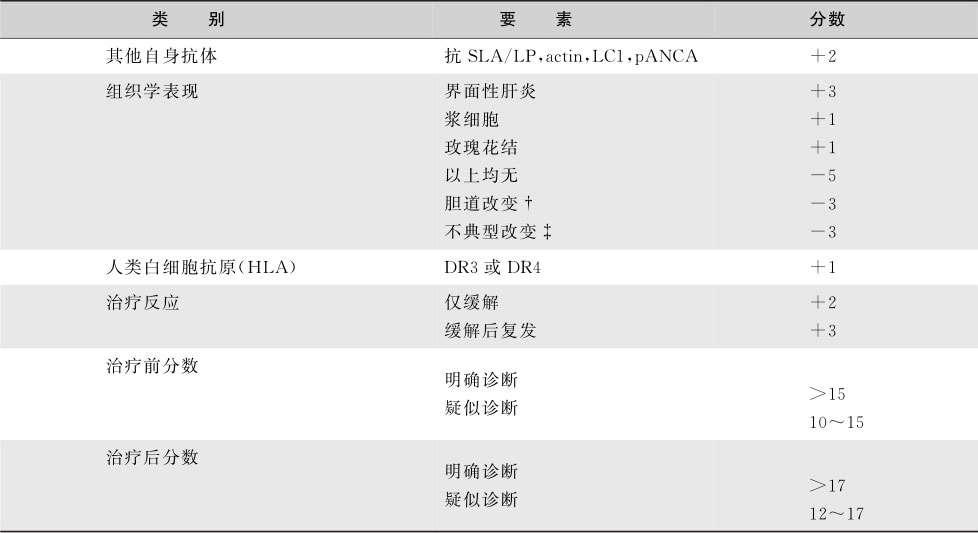
注:†包括破坏性和非破坏性胆管炎或胆管稀少
‡包括脂肪肝,支持遗传性血色病的铁负荷,酒精诱导的肝炎,病毒感染表现(毛玻璃样肝细胞),或包涵体(巨细胞病毒,单纯疱疹病毒)
表15-8-9 AIH的简化诊断积分系统(Hennes EM,et al,2008)

注:AIH:自身免疫性肝炎;ANA:抗核抗体;ASMA:抗平滑肌抗体;抗LKM-1:抗肝肾微粒体抗体-1型;抗-SLA:抗肝可溶性抗原抗体
(二)临床分期和特殊类型的AIH
临床上AIH可分为:①无症状AIH;②有症状AIH;③缓解期AIH;④治疗中复发;⑤代偿期无活动性肝硬化;⑥失代偿期活动性肝硬化;⑦肝衰竭。还有一些情况需特殊治疗:①儿童;②妊娠;③多次复发或对皮质类固醇耐受;④合并丙型病毒性肝炎;⑤特殊类型的AIH:如AIH-PBC重叠综合征、自身免疫性胆管炎;⑥AIH-PSC重叠。
(三)鉴别诊断
临床上AIH与其他肝病在治疗上有着明确的区别,需仔细鉴别。主要包括:①肝遗传性疾病,如Wilson病、血色病、α 1 -抗胰蛋白酶缺陷;②药物诱导的肝病;③慢性病毒(如 HCV、HBV)感染;④酒精性肝病;⑤其他自身免疫性肝病或重叠。
【治疗】
AIH对激素等免疫抑制药物治疗敏感,但一般仅对严重、快速进展的AIH才使用免疫抑制药物治疗,对于尚不满足绝对指征的患者的治疗应基于临床判断并个体化。对失代偿的患者也应考虑激素治疗。治疗的总体目标是获得肝组织学缓解、防止肝纤维化进展、发生肝衰竭,延长患者生存期、提高患者的生存质量。治疗目标是获得完全生化指标缓解,即ALT/AST和IgG水平均恢复正常。非活动性AIH患者还应每3~6个月密切观察肝功能和免疫球蛋白,病情加重可考虑重复肝组织检查。
(一)免疫抑制药物治疗
1.治疗指征
(1)绝对指征:
①血清氨基转移酶至少10倍于正常上限甚至重症(伴出凝血异常,INR>1.5);②血清氨基转移酶至少3倍于正常而γ-球蛋白至少1.5倍于正常;③病理组织学检查示桥样坏死,或多小叶坏死,界面性肝炎(重度、融合)。
(2)相对指征:
乏力、关节痛、黄疸症状明显;血清氨基转移酶和(或)γ-球蛋白增高水平低于绝对指征;界面肝炎(轻中度)。
(3)无指征:
无活动性肝硬化,既往对泼尼松和(或)硫唑嘌呤不耐受,已有共存疾病。
2.治疗方案
推荐使用泼尼松或泼尼松联合硫唑嘌呤的成人治疗方案见表15-8-10。治疗应持续进行直到疾病缓解,或确定治疗失败、出现严重药物不良反应。联合治疗可显著减少泼尼松(龙)剂量及其不良反应。也可在使用泼尼松(龙)2周出现显著生物化学应答后再加用硫唑嘌呤。
约65%的患者治疗后症状缓解,肝功能恢复正常(血清转氨酶水平正常或小于正常2倍),组织学上没有活动性肝炎证据(肝组织正常,或少量炎症及没有界面性肝炎)。应经肝活检证实有组织学改善再逐渐停药(停药间期应不短于6周),而过早中断治疗是复发的常见原因。停药期内应每3周进行血清AST、胆红素、γ-球蛋白的检查,治疗结束后也应经常(至少每3个月进行1次)复查以监测复发。
表15-8-10 成人AIH治疗方案(Czaja AJ & Freese DK,2002)
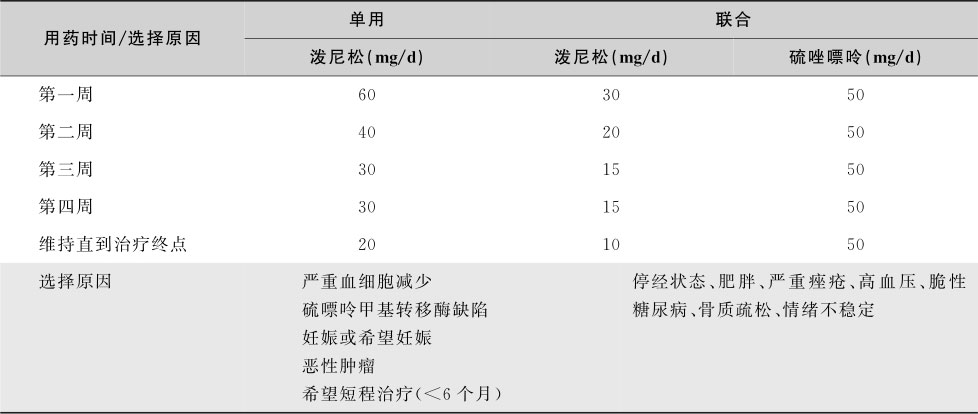
3.复发、治疗失败及应答不完全的处理
(1)复发:
指在停药过程中或之后症状重新出现,血清谷草转氨酶水平上升到正常上限的3倍以上,或组织学检查再出现至少是门静脉周围炎改变。停药后复发是AIH的临床特点之一。3年内复发率高达70%。复发后再治疗可诱导再一次缓解,但药物撤退后常常出现再一次复发。复发患者比那些停药后持续缓解的患者预后差,更易发生药物有关的不良反应。复发多于一次的患者应联合泼尼松和硫唑嘌呤治疗,或低剂量泼尼松或单用硫唑嘌呤维持治疗。
(2)治疗失败:
一部分患者在治疗中出现临床、生化或组织学表现的恶化称治疗失败。对这些患者应重新考虑自身免疫性肝炎的诊断,需进一步排除其他因素如病毒、药物、毒素、酒精的影响及患者对治疗方案的依从性。除外上述因素后可采用大剂量泼尼松(60mg/d)或泼尼松(30mg/d)联合硫唑嘌呤(150mg/d)治疗至少1个月,如果病情持续改善则每月剂量减少泼尼松10mg和硫唑嘌呤50mg直到一般的维持剂量。治疗失败的患者大部分具有活动性组织学变化和皮质激素依赖性,因此常常发生严重药物相关的不良反应和出现肝衰竭。
(3)应答不完全:
约13%的患者在治疗2~3年后中临床、实验室和组织学表现仅部分改善,未完全恢复正常,建议调整药物到防止病情加重的最低适合剂量长期维持治疗,使患者处于无症状、实验室指标稳定的状态。
(4)药物不良反应:
发生容貌变化(Cushing体征),有症状的骨质疏松,情绪不稳定,难以控制的高血压,脆性糖尿病或进行性血细胞减少。减少剂量或根据不良反应的程度停药,调整并维持能够耐受的药物剂量。
(二)其他替代药物
第二代皮质激素布地奈德可替代泼尼松(龙)作为AIH的一线治疗方案,可减轻糖皮质激素相关不良反应,但不推荐用于传统激素无应答的病例,也不宜应用于肝硬化患者,因可通过侧支循环直接进入体循环而失去肝脏首过效应的优势,同时还可能有增加门静脉血栓形成的风险。可试用于AIH治疗的二线药物有环孢素A[5~6mg/(kg·d)]、6-巯基嘌呤、酶酚酸酯(MMF)、甲氨蝶呤、FK506(4mg,2次/日),细胞保护性药物多烯磷脂酰胆碱、熊去氧胆酸等,其中MMF是标准治疗效果不佳患者中应用最多的替代免疫抑制剂。
(三)肝移植治疗
对皮质激素治疗中或治疗后失代偿的AIH患者可考虑肝移植。对没有治疗过的失代偿患者应使用皮质激素或其他免疫抑制药物作为防止和延迟移植手术的补救治疗措施。移植后5年存活率超过80%。在同种肝移植后至少17%的受体AIH可能复发,主要发生于免疫抑制不充分或HLADR3与供体不匹配的患者,移植后复发患者可通过调整免疫抑制药物的方案来控制。
二、原发性胆汁性肝硬化
原发性胆汁性肝硬化(primary biliary cirrhosis,PBC)是一种成年人慢性进行性胆汁淤积性肝疾病。以肝内进行性非化脓性小胆管破坏伴门静脉炎症和肝纤维化为特点,绝大多数PBC患者抗线粒体抗体(antimitochondrial antibodies,AMA)阳性,特别是AMA-M2亚型阳性对本病诊断敏感性和特异性较高。最终可进展为肝硬化和肝衰竭,是肝移植的主要适应证之一。由于越来越多地认识到该病的自然发展史和早期类型,国内外专家建议将该病更名为“原发性胆汁性胆管炎”。
PBC主要发生在40~60岁的中年女性,女性∶男性约为9∶1。发病年龄可在20~90岁,平均年龄50岁。PBC发病不受地区和人种的限制。估计每年的发病率和患病率为2~24/100万和19~240/100万。PBC有家族因素,在患者的一级亲属中患病率远远高于普通人群。
【发病机制】
PBC至今病因不明,以选择性破坏肝内胆管上皮细胞和肉芽肿形成为特点,几乎所有患者均有针对非器官、非种属特异的存在于线粒体内膜的自身抗原的特异性自身抗体和自身反应性T细胞反应,此外常常合并其他器官特异性自身免疫性疾病如硬皮病和自身免疫性甲状腺疾病,并常有唾液腺上皮细胞受损,因此被认为是一种器官特异性的自身免疫性疾病。PBC与抗线粒体抗体,特别是线粒体内膜丙酮酸脱氢酶的E2成分有密切关系。AMA为PBC的重要血清标志。除AMA外,一部分(约50%)的PBC患者可同时或单独出现抗核抗体(antinuclear antibody,ANA)阳性,如抗核孔膜蛋白gp-210及抗核小体蛋白sp100抗体。胆管上皮细胞异常表达线粒体抗原、T细胞介导的异常免疫反应、细菌和异生物素有关的分子模拟(molecular mimicry)和宿主自身抗原发生变化等机制可能参与PBC的发生。
【临床表现】
(一)无症状类型
又分为无症状肝功能正常及无症状肝功能异常二种。这些患者中相当一部分(60%)在诊断时已经形成肝纤维化,80%患者在随访的第1个5年产生PBC的症状和体征。
(二)有症状类型
有症状PBC患者表现为慢性进行性胆汁淤积,主要表现为伴或不伴黄疸的瘙痒(25%~70%)、非特异的症状如乏力(65%~85%)、右上腹痛以及肝硬化失代偿表现如腹水、静脉曲张出血等。体检可发现有皮肤色素沉着、搔痕、黄斑瘤和黄瘤(皮下大量胆固醇沉积)。肝脾大在早期就常见,而门脉高压的体征可能在发展成肝硬化之前就出现。患者常常没有其他慢性肝病的皮肤表现,如蜘蛛痣。
(三)并发症及表现
1.骨质疏松
因维生素D缺乏、激素应用、缺少日照等因素引起。
2.脂溶性维生素缺乏
维生素A缺乏引起的夜盲;维生素E缺乏引起的反射异常、本体感觉减退、共济失调等神经系统异常。
3.高胆固醇血症
胆固醇沉积出现黄瘤、黄斑瘤。
4.脂肪泻
胆酸向小肠排泌异常、胰腺外分泌功能不全、细菌过度生长等。
5.晚期进展性肝病的表现
如静脉曲张出血、腹水和肝性脑病等。
6.其他自身免疫性疾病及结缔组织病
发生于80%的PBC患者。特别是干燥综合征(75%)、硬皮病或CREST综合征(钙质沉着、雷诺现象、食管动力异常、硬皮病和毛细血管扩张)中的任一项(10%以上)、类风湿关节炎、皮肌炎、混合结缔组织病、近端或远端肾小管酸中毒等。部分患者可检测到抗甲状腺抗体(抗微粒体、抗促甲状腺激素抗体)并出现淋巴细胞性甲状腺炎,Graves病及甲状腺功能亢进少见。少于5%的患者可出现不明原因的肺纤维化和炎症性肠病。约1/3的PBC患者可发现具有胆石症。此外有研究认为PBC患者发生肝细胞性肝癌及总的发生其他肿瘤(如乳腺恶性肿瘤)的危险度增加。
【实验室及辅助检查】
(一)血清生化指标
典型的肝功能检查表现为碱性磷酸酶(AKP)、5-核苷酸酶、γ-谷氨酰转肽酶(γ-GT)显著升高。血清氨基转移酶常常仅轻度增高,一般不会增高到正常值上限的5倍。血清胆红素水平早期可正常而晚期随疾病进展上升。高胆固醇血症(多与脂蛋白-X有关)常见,脂蛋白(a)浓度下降。肝合成功能一般保持尚好直至晚期。凝血酶原时间延长提示可能有维生素K的缺乏。PBC患者血清免疫球蛋白增加,特别是IgM。还可发现许多血清自身抗体,包括抗核抗体、抗血小板抗体、抗甲状腺抗体、抗着丝粒抗体、Ro、La、抗-烯醇化酶、淋巴细胞毒抗体)等,但AMA及抗核孔复合物成分的抗体与PBC最密切相关。
临床上还有一小部分患者虽有典型的PBC的临床、生化和组织学表现,但血清AMA检测阴性,被称为自身免疫性胆管炎或抗线粒体阴性的PBC,这些患者大多数具有ANA或SMA,并常有血氨基转移酶活性及IgG增高。
(二)影像学检查
超声检查常用于排除肝外胆管阻塞引起的黄疸。其他横断面图像技术如CT或磁共振能提供其他信息,如门脉高压表现(脾大、腹腔内静脉曲张及门静脉逆向血流)和可能的隐性进展性疾病。PBC患者中15%可出现门静脉周围淋巴腺病,需与恶性肿瘤鉴别。
(三)组织学特点
肝活检有助于对疾病的分期和诊断线粒体阴性的PBC。PBC的诊断性病理特征是非化脓性损伤性胆管炎或肉芽肿性胆管炎。病理组织学(Scheuer's分期系统)将PBC分为以下四期:①Ⅰ期:胆管炎期,以胆管损伤和坏死为特点,胆管上皮细胞皱缩和空泡样变,周围伴有含淋巴细胞、浆细胞、组织细胞、嗜酸性粒细胞和巨噬细胞的肉芽肿性损伤,局灶胆管阻塞伴肉芽肿形成(又称旺炽性胆管损伤),是PBC最特殊的病理特征。②Ⅱ期:汇管区周围炎期:炎症从门静脉三角区延伸出去并伴有胆管碎片状坏死,可见显著的胆管炎、肉芽肿及胆管增生。门静脉周围肝细胞的空泡变性,围绕以泡沫样变性的巨噬细胞。③Ⅲ期:进行性纤维化期:表现为进展性纤维化和瘢痕,邻近的门静脉之间以纤维间隔连接起来,小管稀少(定义为小叶间胆管丢失50%)更为常见,引起胆汁淤积和肝铜在门静脉及间隔周围肝细胞内的沉积。④Ⅳ期:肝硬化期,以具有纤维间隔和再生结节的胆汁性肝硬化形成为特点。由于肝活检时的取样误差,因此组织学受累程度应取所观察到的最高分期。
【诊断及鉴别诊断】
PBC的诊断主要建立在:①生化指标支持胆汁淤积的存在(血清碱性磷酸酶AKP的水平上升);②血清抗线粒体抗体间接免疫荧光或免疫印记法检测阳性;和(或)③肝组织学活检符合PBC表现。诊断时须考虑到无症状型PBC及AMA阴性的PBC。
PBC需与其他胆汁淤积性肝病进行鉴别,其中主要包括肝外胆管阻塞、原发性硬化性胆管炎、肝炎肝硬化、药物性肝病、结节病、重叠自身免疫性肝炎综合征、原因不明的成年人胆管稀少等。

(资源59) 胆汁淤积性肝病(幻灯)
【治疗】
(一)药物治疗
1.熊去氧胆酸(ursodeoxycholic acid,UDCA)
其作用机制包括促进内源性胆酸分泌、提高膜稳定性、减少肝细胞HLA Ⅰ类抗原的异常表达、降低细胞因子的产生、抑制疏水胆酸引起的凋亡和线粒体失功能等。部分患者对UDCA治疗有反应,服药10~20mg/(kg·d)能延长生存期,减少食管静脉曲张及肝硬化的发生。
2008年Corpechot等提出UDCA生物学应答的巴黎Ⅰ标准:UDCA治疗一年后,AKP≤3×ULN,AST≤2×ULN,总胆红素≤1mg/dl。2011年Corpechot等又提出针对早期PBC(病理学分期为I~II期)的UDCA生物学应答的巴黎Ⅱ标准:UDCA治疗一年后,AKP及AST≤1.5×ULN,总胆红素正常。约66%的患者对长期UDCA单一药物治疗表现为“不完全反应”。“不完全反应”定义为血清碱性磷酸酶浓度不能降至正常和(或)发展为肝硬化。治疗初始血清碱性磷酸酶浓度较高及组织学进展程度较严重的患者不完全反应者较多。对药物治疗反应不佳的患者必须排除几种潜在的肝外原因,包括剂量不恰当或未能坚持用药等。如果重叠AIH治疗反应也可能不完全。对UDCA单一药物治疗表现为不完全反应者联合布地奈德、硫唑嘌呤、贝特类降脂药及奥贝胆酸(法尼酯X受体激动剂)等治疗可能有效,但有待进一步验证。
2.免疫抑制剂
如皮质激素、硫唑嘌呤、吗替麦考酚酯、环孢素A、甲氨蝶呤、苯丁酸氮芥等往往不良反应大,而且疗效不确定。
3.贝特类药物
荟萃分析报道贝特类药物如非诺贝特(或苯扎贝特)联合UDCA较UDCA单药治疗对患者AKP、γ-GT、ALT、IgM及甘油三酯水平改善效果好。但治疗过程中需密切检测不良反应。
4.瘙痒的治疗
一线药物是离子交换树脂考来烯胺(考来烯胺),早餐前后4g/d口服。二线药物为利福平,口服150~600mg/d可能缓解症状,但偶可引起肝毒性和骨髓抑制。静脉使用阿片类拮抗剂丙烯基二氢羟吗啡酮(naloxone)或口服纳美芬(nalmefene)也可能缓解症状,主要不良反应为严重的脱瘾症状。瘙痒常因日照加重,因此患者应避光。其他治疗方法包括血浆透析和血浆置换、分子吸附再循环(MARS)透析等。非常严重并难以控制的瘙痒和乏力可考虑进行肝移植。
5.高脂血症的治疗
80%PBC患者可出现,血清胆固醇和甘油三酯浓度均增高。还可出现脂蛋白异常。PBC中黄瘤的形成与血清胆固醇的浓度没有明显关系。经验性使用考来烯胺和他汀类药物(3-羟-3-甲基-戊二酰辅酶A还原酶抑制剂)可能有效。
6.代谢性骨病的防治
推荐每天口服补充钙(1000~1200mg/d)。如果有脂溶性维生素吸收不良引起的维生素D缺乏,建议在检测血清浓度低于正常时给予口服替代(25 000~50 000U,每周2~3次)治疗。降钙素、氟化钠及羟乙二磷酸钠也能增加骨密度。
7.脂肪泻的治疗
对胆酸浓度下降的患者口服补充中链甘油三酯(代替长链混合物)辅以低脂饮食常有益。胰酶替代治疗及经验性抗生素使用可能分别对胰腺功能不足及细菌过度生长有效。
8.脂溶性维生素吸收不良的治疗
维生素A缺乏见于20%的患者,常无临床症状。推荐口服25 000~50 000U每周2~3次替代治疗。6~12个月后检测血清浓度以避免补充过量。第二常见的是维生素D缺乏,所有慢性胆汁淤积的患者均建议补充钙及维生素D。对有慢性淤胆的绝经后妇女推荐雌激素替代治疗(经皮途径)。有症状的维生素E缺乏较少见,可表现为脊髓后索异常的共济失调,推荐对无症状的患者每天口服补充维生素E 400U。维生素K缺乏者可予5~10mg/d剂量补充。
(二)肝移植
肝移植是终末期PBC患者唯一有效的治疗方法,PBC是成年人进行肝移植的主要病因之一。PBC患者移植后瘙痒和乏力可迅速改善,代谢性骨病可在第1个6~12个月的一过性加重后改善。移植后长期随访发现有部分患者出现组织学上PBC复发的证据。
【预后】
PBC患者的预后差异很大。无症状患者总的中位生存时间显著长于有症状患者。总胆红素水平高于136.6~171.0μmol/L的患者中位生存期约2年。影响预后的因素包括老年、血清总胆红素浓度增高、肝合成功能降低及组织学分期的程度。门脉高压并发症可出现在有症状的PBC患者,3年以后食管静脉曲张及出血的危险性增加。硬化前PBC患者出现食管静脉曲张的病因包括因肉芽肿性胆管炎症及窦周肝纤维化。
三、原发性硬化性胆管炎
原发性硬化性胆管炎(primary sclerosing cholangitis,PSC)是一种特发性肝内外胆管炎症和纤维化导致多灶性胆管狭窄、慢性胆汁淤积综合征、门脉高压和最终肝衰竭的慢性胆汁淤积性肝病,10%~30%的患者还会发生胆管癌。主要累及年轻人,平均诊断年龄是40岁,并且70%的患者是男性。国外报道PSC常常伴有炎症性肠病,特别是慢性溃疡性结肠炎。
与PBC相似,一系列胆汁淤积的并发症如瘙痒、骨质疏松、脂溶性维生素缺乏及高胆固醇血症以及进展性肝病的表现在PSC中也可发生,此外PSC还具有一些特殊的并发症如胆管炎、胆管狭窄、胆石症、胆管癌及因慢性溃疡性结肠炎进行结肠直肠切除和回肠造口术后发生的造口处静脉曲张。胆管癌约在10%的患者发生。
【临床表现】
临床表现可为无症状但肝功能异常,或以慢性胆汁淤积、复发性胆管炎、慢性肝病的并发症就诊,也有剖腹手术时偶然发现。症状和体征常见有乏力、瘙痒、黄疸症状,还可有重量减轻、发热等不适。体征可有肝大、黄疸、脾大、色素过度沉着、黄瘤等。部分患者并发炎症性肠病(特别是慢性溃疡性结肠炎)而有相应肠道表现。
【实验室及辅助检查】
(一)生化检查
主要表现为胆汁淤积,AKP、γ-GT活性增高,且持续超过6个月,但无明确的诊断标准临界值;血清转氨酶通常正常,或可升高约2~3倍正常值上限,显著升高的转氨酶水平需考虑存在急性胆道梗阻或重叠有AIH可能。血清胆红素和白蛋白可初始正常而随疾病进展出现异常,晚期可出现低白蛋白血症及凝血功能障碍。
(二)免疫学检查
1.血清免疫球蛋白
约有30%的患者可出现高γ-球蛋白血症,约50%的患者可伴有IgG或IgM水平的轻至中度增高,但免疫球蛋白异常与其治疗过程中的转归对预后无明确的提示意义。部分PSC患者可见IgG4轻度增高(9%~36%),需与IgG4相关胆管炎鉴别。
2.自身抗体
约超过50%PSC患者血清中可检测出多种自身抗体,包括抗核抗体(ANA)、抗中性粒细胞胞质抗体(pANCA)、抗平滑肌抗体(SMA)、抗内皮细胞抗体、抗磷脂抗体等,其中pANCA分别在33%~85%的PSC和40%~87%的溃疡性结肠炎患者中阳性,但均为非特异性抗体,对PSC无诊断价值。疑似PSC患者可通过检测AMA除外PBC。
(三)影像学检查
1.磁共振胰胆管成像(MRCP)
表现为局限或弥漫性胆管狭窄,“串珠”样改变,显著狭窄的胆管在MRCP上显影不佳,表现为胆管多处不连续或呈“虚线”状,病变较重时可出现狭窄段融合,小但管闭塞导致肝内胆管分支减少,其余较大胆管狭窄、僵硬似“枯树枝”状,称“剪枝征”。胆道成像对于PSC诊断的确立至关重要。
2.经内镜逆行性胰胆管造影(ERCP)
典型表现为肝内和(或)肝外胆管弥散性、多灶性环状狭窄;短带状狭窄;憩室状突出;胆管壁僵硬似铅管样、狭窄上端的胆管可扩张呈串珠样表现,进展期患者可显示长段狭窄和胆管囊状或憩室样扩张,但肝内胆管广泛受累时可表现为枯枝样改变。相较于MRCP,ERCP更有助于判断肝外胆管梗阻及严重程度。
3.经腹超声检查
可作为PSC的初始筛查,显示肝内散在片状强回声及胆总管管壁增厚、胆管局部不规则狭窄等变化,并可显示胆囊壁增厚程度与胆系胆汁淤积情况及肝内三级胆管的扩张情况等。常规超声结合病史可以协助肝内外胆管结石、胆管癌、继发性胆管炎及术后胆道狭窄等与PSC有相似临床症状疾病的鉴别。
(四)肝脏病理学表现
PSC患者肝活检病理表现早期不特异,只提示胆道损伤,晚期表现为胆道系统的纤维化改变,累及整个肝内外胆道系统,胆管纤维化呈节段性分布,狭窄与扩张交替出现,肝内小胆管典型改变为胆管周围纤维组织增生,呈同心圆性“洋葱皮样”纤维化。病理组织学可沿用Ludwig分期系统将PSC分为4期:①Ⅰ期:门脉期,表现为门脉肝炎(局限于界板)炎症改变仅仅局限于肝门区,淋巴细胞、中性粒细胞向胆管浸润,胆管上皮变性坏死等;②Ⅱ期:门脉周围期,表现为门脉周围实质的纤维化/炎症(超出界板),出现肝细胞坏死、胆管稀疏和门静脉周围纤维化;③Ⅲ期:纤维间隔形成期,表现为纤维化及纤维间隔形成及(或)桥接状坏死,肝实质还表现为胆汁淤积和碎屑样坏死,伴有铜沉积,胆管严重受损或消失;④Ⅳ期:硬化期。
【诊断】
PSC的诊断需结合临床表现、生化检查、影像学检查结果,一些病例还需行病理检查。对于具有胆汁淤积生化表现的患者,若胆道成像具备PSC典型表现,且除外其他原因所致者可诊断PSC。对于疑诊PSC患者,应进行胆道成像检查,且首选MRCP。除非对于诊断胆道影像学检查无异常的小胆管型PSC患者,肝组织活检对于诊断PSC不是必需的,但活检病理可以评估疾病的活动度和分期,还可以用于协助判断是否重叠其他疾病如AIH等。
本病除病因、疾病严重程度诊断外,还需对胆汁淤积的并发症及PSC特殊的并发症如胆管炎、胆管狭窄、胆石症、胆管癌、慢性溃疡性结肠炎进行诊断。胆管成像结果显示明显狭窄者通过ERCP细胞学及活组织检查有助于排除胆管癌。
【鉴别诊断】
(一)继发性硬化性胆管炎
临床特征与PSC相似,但病因明确。如胆总管结石、胆道手术创伤、反复发作的化脓性胆管炎、肿瘤性疾病(胆总管癌、肝细胞癌侵及胆管、壶腹部癌、胆总管旁淋巴结转移压迫)、胰腺疾病(胰腺癌、胰腺囊肿和慢性胰腺炎)、肝胆管寄生虫、IgG4相关性胆管炎、缺血性胆管病(如遗传性出血性毛细血管扩张症、结节性多动脉炎和其他类型的脉管炎、肝移植相关缺血性胆管炎)、肝动脉插管化学治疗(主要为5-氟尿嘧啶)、腹部外伤等。少见原因有自身免疫性胰腺炎、胆总管囊肿、肝脏炎性假瘤、组织细胞增生症X、与艾滋病和其他类型的免疫抑制相关的感染性胆管炎、先天性胆管异常或胆道闭锁、囊性纤维化等。特别是既往有胆道手术或同时患有胆道结石或肝胆管肿瘤时,两者的鉴别诊断困难,需仔细询问病史、了解病程中是否伴有IBD、了解手术病理表现,对鉴别诊断具有重要作用。
(二)其他胆汁淤积性疾病
如PBC、AIH、药物性肝损伤、慢性活动性肝炎、酒精性肝病等。特别是有些不典型的PSC,血清AKP仅轻度升高,而转氨酶却明显升高,易误诊为AIH。
【治疗】
PSC的治疗目前也同样没有特异或有效的方法。治疗可采用机械性(内镜下ERCP进行球囊扩张治疗胆道狭窄、短期胆管支架植入进行胆汁引流;鼻胆管引流)、外科性(胆道重建、胆肠内引流术、正位肝移植)、内科性(免疫抑制剂、抗纤维化、利胆药、抗生素)方法。肝移植是唯一能挽救终末期PSC患者生命的治疗措施,一般来说PSC应早期在发生胆管癌和晚期肝衰竭之前就考虑肝移植,然而术后有20%的复发率。
四、重叠综合征
一些患者可同时或顺序出现自身免疫性肝炎和自身免疫性胆管病变,如这些疾病中任意两者同时出现则称为“重叠综合征”,其中以PBC-AIH重叠综合征最为常见。
PBC-AIH重叠综合征
患者或先后,或同时在临床、生化、血清学、伴或不伴组织学特征出现PBC和AIH这两种疾病的表现。其病理生理机制可能同属一种自身免疫性疾病,但不同的遗传背景导致了不同的临床、生化和组织学表现,或为两种自身免疫性疾病的中间状态。
【诊断】
PBC和AIH的诊断需联合血清、生化和组织学特征。至少同时具备两种疾病的2~3个诊断指标才能诊断PBCAIH重叠综合征(表15-8-11),其中组织学表现中重度淋巴细胞碎屑样坏死(界面性肝炎)是诊断所必需的。
除了最常见的PBC和AIH同时出现这一类型,还有从PBC发展到AIH或相反的类型,称之为“序贯综合征”。PBC的基线情况和对UDCA的初步反应不能预测重叠AIH的发生。另外,AMA阴性的PBC和AIH重叠也有报道,较单纯PBC患者病情更严重,预后更差。
表15-8-11 PBC-AIH重叠综合征的诊断标准

注:至少需同时具备两种疾病的2~3个诊断指标,其中包括组织学重度界面性肝炎表现
【治疗】
联合疗法(UDCA和糖皮质激素)是PBC-AIH重叠综合征的最佳治疗选择。另一种治疗方法是:开始时单用UDCA,如果一定时间段内(如3个月)没有达到充分的生化应答,应加用糖皮质激素。开始阶段泼尼松使用量是0.5mg/(kg·d),一旦ALT水平出现应答就要逐步减量。波尼松(龙)联合UDCA治疗不能缓解或泼尼松(龙)不良反应明显者,可加用免疫抑制剂如硫唑嘌呤,或其他二线免疫抑制剂如环孢素A、他克莫司和MMF。
UDCA治疗的PBC患者,如进展为AIH(序贯综合征),需用免疫抑制治疗。
PSC-AIH重叠综合征
少见并主要发生于儿童、青少年和年轻人。约占诊断为PSC患者的7%~14%,患者AMA阴性,常伴随炎症性肠病。
【诊断】
PSC-AIH重叠综合征的诊断标准是相加性的,即在明确PSC诊断的基础上(具有典型的PSC胆道造影或组织学表现),同时存在AIH的特征性临床和病理表现,包括:①修订的AIH评分>15;②ANA或ASMA抗体滴度至少1∶40;③肝组织学示存在界面肝炎。
【治疗】
UDCA联合免疫抑制治疗作为PSC-AIH重叠综合征的药物治疗,如 UDCA[15~20mg/(kg·d)]、泼尼松龙(10~15mg/d)和硫唑嘌呤(50~75mg)。肝移植是终末期PSC可选的治疗手段。
五、IgG4相关性胆管炎
IgG4相关性胆管炎(IgG4 related cholangiopathy,IAC)是一种新近发现的病因不明的胆道疾病,其生化和胆道造影表现与PSC相似。常累及肝外胆管。患者有梗阻性黄疸的临床表现,如乏力、黄疸、瘙痒、体重减轻等。糖皮质激素治疗对IAC有效,常伴发自身免疫性胰腺炎(AIP)以及其他纤维化性疾病,血清IgG4水平升高和胆管内及肝组织IgG4阳性浆细胞浸润是其特征性表现。IAC与IBD无关。多数男性患者诊断时中位年龄是60岁左右。免疫抑制治疗有效者的长期预后良好。
【诊断】
如果患者伴有肝内胆管、近端肝外胆管和(或)胰腺内胆管的狭窄,硬化性胆管炎的典型胆道影像学改变者需考虑IAC诊断,但还需基于以下发现:①近期胰腺癌/胆道外科手术史或胰腺针芯活检有AIP/IAC特征性组织学表现;或②典型的AIP影像学改变伴IgG4升高;或③符合以下标准中的两项:a.IgG4升高:血清IgG4≥135mg/dl;b.同时合并AIP,或其他脏器改变如硬化性涎腺炎、腹膜后纤维化、伴IgG4阳性浆细胞浸润的胃肠道或腹部淋巴结肿大;c.胆管活组织检查示每高倍镜视野下的IgG4阳性浆细胞>10个;d.对糖皮质激素显效且治疗4周拆除支架后,阻塞性胆汁淤积不复发,血清肝指标<2×ULN,IgG4和CA19-9下降。
【治疗】
免疫抑制治疗可明显改善IAC的炎性活动度,有报道治疗3个月后可获得完全长期缓解。病变的累及范围可能会影响药物的长期疗效,因此本病的初始治疗建议选择糖皮质激素,泼尼松40mg/d,口服2周,然后逐渐减量(每周减5mg),共约11周。对近端和肝内胆管狭窄、糖皮质激素治疗期间和治疗后复发的患者,可考虑加用硫唑嘌呤[2mg/(kg·d)]。对一些患者来说,3个月的治疗可能已足够,但当疾病活动度尚未停止或疾病复发时,则需长期低剂量维持治疗。
主要参考文献
1.Hennes EM,Zeniya M,Czaja AJ,et al.International Auto-immune Hepatitis Group.Simplified criteria for the diagnosis of autoimmune hepatitis.Hepatology,2008,48(1):169-176.
2.Lindor KD,Gershwin ME,Poupon R,et al.Primary biliary cirrhosis.Hepatology,2009,50(1):291-307.
3.Chapman R,Fevery J,Kalloo A,et al.Diagnosis and man-agement of sclerosing cholangitis.Hepatology,2010,51(2);660-677.
4.European Association for the study of the liver.EASL clini-cal practice guidelines:autoimmune hepatitis.J Hepatol,2015,63(4):971-1004.
第四节
酒精性肝病

董玲 沈锡中
酒精性肝病(alcoholic liver disease,ALD)是由于长期大量饮酒导致的中毒性肝损伤,初期表现为肝细胞脂肪变性,进而发展为酒精性肝炎、最终导致肝纤维化、酒精性肝硬化。短期严重酗酒时也可诱发广泛肝细胞损害甚或肝衰竭。本病在欧美国家多见,近年来我国发病率也在上升。目前居肝硬化病因的第二位。
【病因和发病机制】
饮酒后乙醇主要在小肠上段吸收,90%以上在肝内代谢。乙醇进入肝细胞后,80%~85%经过乙醇脱氢酶(ADH)代谢为乙醛,再通过乙醛脱氢酶(ALDH)代谢为乙酸,后者在外周组织中降解为水和CO 2 。多余的乙醇可通过肝微粒体乙醇氧化酶(MEOS)、过氧化氢酶(H 2 O 2 酶)降解。MEOS中细胞色素P450CYP2E1是代谢限速酶,可由酒精诱导而加速乙醇降解。乙醇代谢为乙醛、乙酸过程中,氧化型辅酶Ⅰ(NAD)转变为还原型辅酶Ⅰ(NADH)明显增加,肝内氧化还原状态异常。
乙醇导致肝脏脂肪变可能与以下原因有关:①外周脂肪组织动员、肠道乳糜微粒吸收增多,脂肪酸转运入肝脏增多;②肝脏合成内源性脂肪酸增多。肝内氧化还原状态异常。脂肪酸β氧化减少,转化为甘油三酯增多;③极低密度脂蛋白合成或分泌减少,甘油三酯转运出肝细胞减少;④乙醇诱导单磷酸腺苷活化蛋白激酶(AMPK)活性,抑制PPAR-α,诱导激素调节元件结合蛋白1c促进脂肪合成增加,降解减少。最终导致肝脏内甘油三酯积聚,加剧细胞氧化应激反应。
酒精性脂肪肝肝炎与以下机制有关:①乙醇的中间代谢物乙醛是高度反应活性分子,结合细胞内蛋白质和DNA形成复合物,作为新抗原诱发机体自身免疫损伤;并造成线粒体损伤、谷胱甘肽功能抑制,促进氧化应激反应。②长期摄入酒精诱导MEOS通路的P450CYP2E1,加剧细胞氧化应激和脂质过氧化反应。③内毒素和细胞因子:ALD患者肠菌易位,肠道通透性增加,单核-吞噬细胞系统清除减弱,产生内毒素血症;肝脏的库普弗细胞通过 TLR(toll-like receptor)诱发CD14的表达,促使其与内毒素成分脂多糖(LPS)结合活化,诱导炎症信号通路活化,激活肝星状细胞(HSC),促进肝纤维化发生。
【病理特点】
ALD病理学改变主要为大泡性或大泡性为主伴小泡性混合性肝细胞脂肪变性。中华医学会肝病学分会脂肪肝和酒精性肝病学组于2010年修订酒精性肝病诊疗指南,依据病变肝组织是否伴有炎症反应和纤维化.可分为单纯性脂肪肝、酒精性肝炎肝纤维化和肝硬化。
各型酒精性肝病病理特点(表15-8-12):
(1)单纯性脂肪肝:依据肝细胞脂肪变性占组织标本量的范围分4度:F0~4。F0:<5%的肝细胞脂肪变性。
(2)酒精性肝炎肝纤维化:酒精性肝炎的脂肪肝程度与单纯性脂肪肝一致,分为4度(F0~4)。依据炎症程度,分为4级(G0~4);依据纤维化范围和形态,肝纤维化分为4期(S0~4)。G0:无炎症;S0:无纤维化。
(3)酒精性肝硬化:肝小叶结构完全损毁,代之以假小叶和广泛纤维化,典型的是小结节性肝硬化。根据纤维间隔是否有界面性肝炎,分为活动性和静止性。
表15-8-12 酒精性肝病病理分级
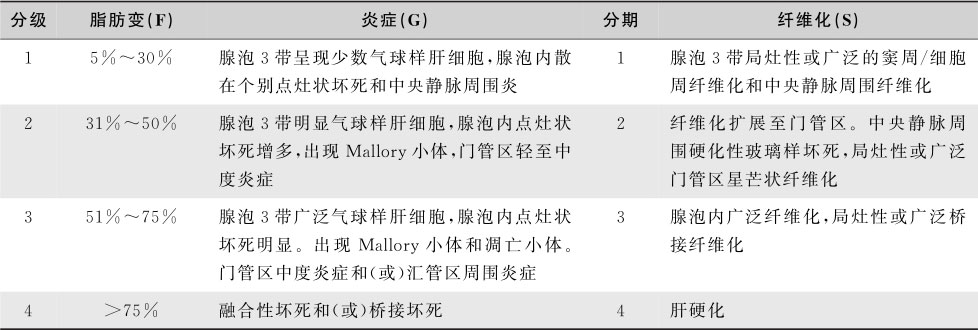
【诊断和鉴别诊断】
酒精性肝病的诊断包括:病因诊断、病理诊断、鉴别诊断。
(一)病因诊断
1.病史
(1)饮酒史:
长期大量饮酒是诊断酒精性肝病的必备条件。包括酒的种类、每天的摄入量和持续时间等。目前酒精摄入的安全量尚有争议,我国标准是:长期饮酒史,一般超过5年,折合乙醇量男性≥40g/d,女性≥20g/d,或2周内有大量饮酒史(>80g/d)。但应注意性别、遗传易感性等因素的影响。
乙醇量换算公式:乙醇量(g)=饮酒量(ml)×酒精含量(%)×0.8(酒精比重)
(2)饮酒方式:
不同酒精饮料所致肝损伤亦有差异。狂饮模式,空腹饮酒造成的肝损伤更严重。
(3)慢性肝炎病毒感染史:
酒精性肝病和慢性病毒性肝炎有明显协同作用。酒精性肝损害可增加患者对HBV、HCV的易感性;反之,慢性肝炎患者对酒精敏感性增高,容易促进肝硬化和肝癌的发生发展。
(4)其他:
女性对酒精介导肝毒性的敏感性是男性2倍,酒精性肝硬化发生于非白色人种者较多。存在蛋白质热量营养不良和严重程度对决定ALD患者的预后,死亡率与营养不良程度成正比。遗传因素、基因多态性也影响酒精代谢、此外尚需排除代谢异常和药物因素引起的肝脏损伤。
2.症状和体征
(1)轻症酒精性肝病:
肝脏生化、影像学和组织病理学,检查基本正常或轻微异常。
(2)酒精性脂肪肝:
一般情况良好,常仅有肝脏肿大,影像学诊断符合脂肪肝标准,血清ALT、AST或γ-GT可轻微异常。
(3)酒精性肝炎:
临床表现差异大,与组织学损害程度相关。常发生在近期大量饮酒后,出现全身不适、食欲减退、恶心呕吐、乏力、腹泻、肝区疼痛等症状。可有低热、黄疸、肝大并有触痛。严重者可并发急性肝衰竭。
(4)酒精性肝硬化:
常有明显酒精性容貌,肝掌、蜘蛛痣、面部毛细血管扩张。可以门脉高压为主要表现,但脾大不如肝炎肝硬化常见。此外还可出现肝外器官酒精中毒损害,如酒精性心肌病、胰腺炎,巨幼红细胞贫血,骨骼肌萎缩、生育障碍。可伴神经系统表现:谵妄、Wernicke脑病、周围神经病等。
(5)评价酒精性肝病严重程度的指标:
有几种方法可用于评估酒精性肝炎的严重程度和近期存活率。Maddrey判别函数(discriminant function,DF),即4.6×(凝血酶原时间-对照值)+血清总胆红素(mg/dl),当DF>32,提示患者近期死亡率高。终末期肝病模型(MELD评分)>18,Glasgow评分>8,提示预后不良。其他如Lille评分也有预测价值。
3.实验室检查
(1)血常规:
多有白细胞升高、营养不良性贫血。脾功能亢进时可有白细胞、血小板减少。
(2)生化检查:
①血清 AST、ALT轻中度升高,以AST为著,AST/ALT比值可超过2倍。线粒体AST/总AST明显增高。禁酒后4周血清AST、ALT基本恢复正常(低于2倍正常上限值),但酒精性肝炎AST>500U/L,ALT>200U/L较少,需考虑其他病因;②血清γ-谷氨酰转肽酶(γ-GT)升高2倍以上,禁酒4周后明显下降(降到正常值的1/3或比戒酒前下降40%以上);③糖缺陷转铁蛋白(CDT)增高:过量乙醇抑制糖蛋白糖基转移酶活性,影响转铁蛋白糖基化过程,是反映慢性乙醇中毒的指标,但敏感性特异性有限;④其他:平均红细胞容积(MCV)增高。
4.影像学检查
(1)B型超声:
可见肝脏体积增大,近场回声弥漫性增强,远场回声逐渐衰退;肝内管道结构显示不清,但肝内血管走向正常,对诊断脂肪肝帮助较大。肝硬化为小结节性肝硬化,肝表面波纹状,可有门脉高压征。
(2)CT:
可见弥漫性肝脏密度降低,肝/脾CT比值≤1。0.7<肝/脾CT比值≤1.0为轻度;0.5<肝/脾CT比值≤0.7为中度;肝/脾CT比值≤0.5者为重度。
(3)磁共振扫描:
对鉴别脂肪肝或肝炎和肝硬化及肝癌等可能更好。
(二)病理学检查
肝活组织检查是确定酒精性肝病及分期分级的可靠方法,是判断其严重程度和预后的重要依据。但很难与其他病因引起的肝脏损害鉴别。
(三)鉴别诊断
首先应排除其他原因所引起的脂肪肝。排除非酒精性脂肪肝、嗜肝病毒感染、药物、中毒性肝损伤和自身免疫性肝病等。对于酒精性肝病与病毒性肝炎所致的肝硬化应审慎鉴别。肝性脑病要和酒精性谵妄、Wernicke脑病等相鉴别。
【治疗】
酒精性肝病的治疗原则:戒酒、营养支持、清除肝脂肪浸润、治疗酒精性肝炎、防治肝硬化及并发症。
(一)戒酒
戒酒是治疗酒精性肝病的关键。戒酒4周可使酒精性脂肪肝恢复正常,也可使酒精性肝炎的临床症状、肝功能、病理学改变逐渐减轻,在彻底戒酒后甚至可完全恢复。虽然戒酒难以逆转肝硬化的病理改变,但可以提高肝硬化患者的存活率。可以用心理疗法或用纳曲酮、阿坎酸(acamprosate)等药物辅助戒酒。若出现酒精戒断症状时可减量应用安定类等药物。
(二)营养支持
长期酗酒者,酒精代替了食物提供身体所需热量,故而蛋白质营养不良和维生素缺乏症常见。在戒酒的基础上,对酒精性肝病患者应给予高热量(35~40kcal/kg)、高蛋白(1.5g/kg)、低脂饮食,如有肝性脑病的表现或先兆,应限制蛋白质饮食。此外,乙醇代谢过程中对维生素的利用、转化、贮存均发生障碍,尤其是B族维生素缺乏普遍,应注意及时补充维生素A、B、E、叶酸和微量元素。对严重酒精性肝病患者,积极给予肠内营养支持。
(三)药物治疗
单纯戒酒可使酒精性脂肪肝恢复正常,戒酒配合积极的药物治疗也可使酒精性肝炎恢复,肝纤维化得到改善,并降低肝衰竭的死亡率。
1.糖皮质激素
虽然多年来对其疗效尚存在争议,但到目前为止多数临床研究表明糖皮质激素对重型酒精性肝炎有效,可降低其死亡率。主要机制是通过抑制NF-κB转录活性进而抑制以TNF α为主的多种炎症因子的转录,抑制肝细胞的炎症反应。泼尼松龙每天40mg,7天后如果Lille评分<0.45,可继续激素治疗3周,2周内逐步撤药;如果7天后Lille评分>0.45,提示预后不良,合适的患者应尽早考虑肝移植。感染和消化道出血是激素应用的禁忌证。
2.己酮可可碱(pentoxifylline,PTX)
可抑制TNF - α基因的转录,相应降低TNF-α下游效应分子水平。主要用于酒精性肝炎,尤其适宜合并感染或肝肾综合征的严重酒精性肝炎患者,用法:400mg每天3次,连续28天。
3.抗氧化剂
补充外源性谷胱甘肽及其前体药物N-乙酰半胱氨酸、S-腺苷蛋氨酸可增加肝细胞内谷胱甘肽含量,改善肝细胞的抗氧化能力,促进肝细胞修复。N-乙酰半胱氨酸与糖皮质激素有协同作用。
4.抗TNFα抗体(infliximab)
可阻断TNFα活性,减轻TNFα介导的病理损伤。但疗效和安全性尚存争议。
(四)肝移植
Child-Pugh C级和MELD>15的酒精性肝硬化患者在经过仔细的医疗和心理评估后可考虑肝移植,但要求患者肝移植前戒酒3~6个月,并且无其他脏器的严重酒精性损害。移植后主要问题是患者再次酗酒,则会很快进展为包括肝纤维化在内的肝脏损害。
【预后】
酒精性脂肪肝一般预后良好,戒酒后可完全恢复。酒精性肝炎如能及时戒酒和治疗,大多可恢复,主要死亡原因为肝衰竭。若不戒酒,酒精性脂肪肝可进展为酒精性肝硬化,部分酒精性肝硬化可并发肝癌。
主要参考文献
1.酒精性肝病诊疗指南(2010年1月修订).中华医学会肝病学分会脂肪肝和酒精性肝病学组.胃肠病学,2010,15(10):617-621.
2.EASL Clinical Practical Guidelines:Management of Alco-holic Liver Disease.J Hepatol,2012,57:399-420.
3.Jose A,Eric SO,Ramon B.Chapter 103.Alcoholliver dis-ease In Podolsky DK,Camilleri M,Fitz JG,et al.Yamadas Text-book of Gastroenterology.6th ed.New York:John Wiley&Sons Ltd,2016,2043-2055.
第五节
非酒精性脂肪肝病

沈锡中 董玲
非酒精性脂肪肝病(nonalcoholic fatty liver disease,NAFLD)是一种无过量饮酒和其他明确的肝损害因素所致,以肝实质细胞脂肪变性为特征的临床病理综合征。组织学上,NAFLD分为非酒精性脂肪肝(NAFL)和非酒精性脂肪性肝炎(NASH)两种类型。NAFL指存在大泡为主脂肪变,无肝细胞损伤,多为良性、非进展性。NASH指肝脏脂肪变性,合并炎症和肝细胞损伤,伴或不伴纤维化,可进展为肝硬化、肝衰竭和肝癌。
【流行病学】
不同种族、不同年龄组男女均可发病。欧美等发达国家普通成人中NAFLD患病率高达20%~40%,亚洲国家为12%~30%。肥胖症患者NAFLD患病率为60%~90%,NASH为20%~25%。2型糖尿病和高脂血症患者NAFLD患病率分别为28%~55%和27%~92%。近年来中国患病率不断上升,呈低龄化趋势,发达城区成人NAFLD患病率在15%左右。绝大多数NAFLD患者与代谢危险因素有关。西方国家,NAFLD/NASH相关HCC占所有HCC的10%~24%。
【病因与发病机制】
NAFLD主要分为原发性和继发性两大类,通常所指的NAFLD是原发性的,与胰岛素抵抗和遗传易感性相关;而继发性NAFLD包括了由药物(胺碘酮、他莫西芬等的使用)、广泛小肠切除、内分泌疾病等病因所致的脂肪肝。此外,NAFLD与一些少见的脂质代谢病(如无β-脂蛋白血症)和存在严重胰岛素抵抗的罕见综合征(如脂肪萎缩性糖尿病和Mauriac综合征等)有关。
本病病因复杂。发病机制中,“二次打击(two hits)”或“多重打击”学说已被广泛接受。初次打击主要指胰岛素抵抗(insulin resistance,IR)引起的肝细胞内脂质,特别是甘油三酯异常沉积,引起线粒体形态异常和功能障碍。第二次打击主要为反应性氧化代谢产物增多,形成脂质过氧化产物(lipid peroxidation,LPO),导致损伤肝细胞内磷脂膜氧化,溶酶体自噬异常,凋亡信号通路活化;内质网应激,炎症因子通路活化,促进脂肪变性。“多重打击”学说即遗传因素(家族聚集、种族、adiponutrin酶突变)、环境因素(胰岛素抵抗、肠道菌群紊乱、脂肪细胞因子失调、氧化应激等)共同导致NAFLD的发生和进展。
【病理】
推荐NAFLD的病理学诊断和临床疗效评估参照美国国立卫生研究院NASH临床研究网病理工作组指南,常规进行NAFLD活动度积分(NAFLD activity score,NAS)和肝纤维化分期。NAS积分(0~8分):①肝细胞脂肪变:0分(<5%);1分(5%~33%);2分(34%~66%);3分(>66%)。②小叶内炎症(20倍镜计数坏死灶):0分,无;1分(<2个);2分(2~4个);3分(>4个)。③肝细胞气球样变:0分,无;1分,少见;2分,多见。
NAS为半定量评分系统,NAS<3分可排除NASH,NAS>4分则可诊断NASH,介于两者之间者为NASH可能。规定不伴有小叶内炎症、气球样变和纤维化,但肝脂肪变>33%者为NAFL,脂肪变达不到此程度者仅称为肝细胞脂肪变。
肝纤维化分期(0~4):0期:无纤维化;l期:肝腺泡3区轻~中度窦周纤维化或仅有门脉周围纤维化;2期:腺泡3区窦周纤维化合并门脉周围纤维化;3期:桥接纤维化;4期:高度可疑或确诊肝硬化,包括NASH合并肝硬化、脂肪性肝硬化以及隐源性肝硬化(因为肝脂肪变和炎症随着肝纤维化进展而减轻)。
【临床表现】
非酒精性脂肪性肝病起病隐匿,发病缓慢,常无症状。少数患者可有乏力、肝区隐痛或上腹胀痛等非特异症状。严重脂肪性肝炎可出现黄疸、食欲减退、恶心、呕吐等症状。部分患者可有肝脏肿大。失代偿期的肝硬化患者临床表现与其他原因所致的肝硬化相似。
查体:约30%~100%的患者存在肥胖,50%患者有肝大,表面光滑,边缘圆钝,质地正常,无明显压痛。进展至肝硬化时,患者可出现黄疸、水肿、肝掌、蜘蛛痣等慢性肝病体征及门脉高压体征。
【实验室检查】
血清转氨酶(ALT/AST)上升2~5倍常见于NASH患者,但不是反映NAFLD严重程度。30%NAFLD患者碱性磷酸酶(ALP)、γ-谷氨酰转肽酶(GGT)可升高2~3倍。肝硬化和肝衰竭时,可出现血清白蛋白和凝血酶原时间异常,常早于血清胆红素的升高。约30%~50%的NASH患者存在血糖增高或糖耐量异常。20%~80%的患者存在高脂血症。近来,细胞角蛋白(CK 18)片段作为诊断NASH的新型标志物被广泛研究。
【辅助检查】
(一)超声检查
当肝脂肪沉积超过30%时,可检出脂肪肝,肝脂肪含量达50%以上时,超声诊断敏感性可达90%。弥漫性脂肪肝表现为肝脏近场回声弥漫性增强,强于肾脏回声,远场回声逐渐衰减,肝内管道结构显示不清。
(二)CT
弥漫性脂肪肝表现为肝的密度(CT值)普遍降低,严重脂肪肝CT值可变为负值。增强后肝内血管显示非常清楚,其形态走向均无异常。0.7<肝/脾CT比值≤1.0为轻度;肝/脾比值0.5<CT比值≤0.7为中度;肝/脾CT比值≤0.5者为重度脂肪肝。CT诊断脂肪肝的特异性优于B超。
(三)MRI
主要用于鉴别超声与CT上难以区分的局灶性脂肪肝、弥漫性脂肪肝伴正常肝岛与肝脏肿瘤。MRI波谱分析、二维磁共振成像是目前无创性诊断研究的热点。
(四)肝活组织检查
指征:①经常规检查和诊断性治疗仍未能确诊的患者;②存在脂肪性肝炎和进展期肝纤维化风险,但临床或影像学缺乏肝硬化证据者;③鉴别局灶性脂肪性肝病与肝肿瘤、某些少见疾病如血色病、胆固醇酯贮积病和糖原贮积病;④血清铁蛋白和铁饱和度持续增高者推荐进行肝活检,尤其是存在血色沉着病 C 282 Y 基因纯合子或杂合子突变的患者。
【诊断】
明确NAFLD的诊断必需符合以下3项条件:①无饮酒史或饮酒折合乙醇量每周<140g(女性<70g/周);②除外病毒性肝炎、药物性肝病、Wilson病、全胃肠外营养、自身免疫性肝病等可导致脂肪肝的特定疾病;③肝脏组织学表现符合脂肪性肝病的病理学诊断标准。
鉴于肝组织学诊断有时难以获得,NAFLD工作组定义为:①肝脏影像学表现符合弥漫性脂肪肝的诊断标准并无其他原因可供解释;和(或)②有代谢综合征相关组分如肥胖、2型糖尿病、高脂血症的患者出现不明原因ALT/AST/GGT持续增高半年以上,减肥或改善胰岛素抵抗后,异常酶谱和影像学脂肪肝改善甚至恢复正常者可明确NAFLD的诊断。
推荐代谢综合征组分的诊断采用改良的2005年国际糖尿病联盟的标准。
【鉴别诊断】
1.酒精性肝病 酒精性肝病和NAFLD在组织学特征、临床特点和实验室检查存在一定的重叠。故而应重视病史、体检信息的采集。NAFLD常为肥胖和(或)糖尿病,高血脂患者,AST/ALT比值<1,而酒精性肝病则一般病情较重,血清胆红素水平较高,AST/ALT比值>2;酒精性肝病常见组织学表现如 Mallory小体、胆管增生、巨大线粒体等在NAFLD中常不明显;酒精性肝病一般发生于每日摄入乙醇量超过40g(女性20g)的长期酗酒者,无饮酒史或每周摄入乙醇量小于140g基本可以排除酒精性肝病。但是每周摄入乙醇介于少量(男性<140g/周,女性<70g/周)和过量(男性>280g/周,女性>140g/周)之间的患者,其血清酶学异常和脂肪肝原因常难以界定,需考虑酒精滥用和代谢因素共存可能。
2.NASH需与慢性病毒性肝炎(特别是丙型肝炎)、自身免疫性肝炎、早期Wilson病等可导致脂肪肝的肝病相鉴别。NASH肝细胞损害、炎症和纤维化主要位于肝小叶内,且病变以肝腺泡3区为重;其他疾病的肝组织学改变主要位于门脉周围等特征,病史资料、肝炎病毒标志、自身抗体和铜蓝蛋白等检测有助于相关疾病的明确诊断。NASH如存在血清铁及铁饱和持续性增高,需与血色病相鉴别。
3.其他原因导致的脂肪肝 还需除外药物、全胃肠外营养、炎症性肠病、甲状腺功能减退、库欣综合征、β脂蛋白缺乏血症以及一些与胰岛素抵抗有关的综合征导致脂肪肝的特殊情况。
【治疗】
首要目标:改善胰岛素抵抗,防治代谢综合征和终末期靶器官病变;次要目标:减少肝脏脂肪沉积,避免“多重打击”导致NASH和肝功能失代偿。包括病因治疗、饮食控制、运动疗法和药物治疗。
1.病因治疗 针对原发病和危险因素予以治疗,如减肥、合理控制血糖和血脂、纠正营养失衡等。
2.控制饮食和适量运动是治疗关键。建议低热量低脂平衡饮食,肥胖成人每日热量摄入需减少500~1000kcal。中等量有氧运动(每周至少150分钟)。体重至少下降3%~5%才能改善肝脂肪变,达到10%可改善肝脏炎症坏死程度。
3.药物治疗
(1)改善胰岛素抵抗,纠正糖脂代谢紊乱:噻唑烷二酮类,可改善胰岛素抵抗,可用来治疗肝活检证实NASH的脂肪性肝炎。二甲双胍并不能改善NAFLD患者肝组织学损害,不推荐用于NASH的治疗。
如无明显肝功能异常、失代偿期肝硬化,NAFLD患者可安全使用血管紧张素Ⅱ受体阻断药降血压,他汀类、依折麦布调脂治疗。Omega-3可作为NAFLD患者高甘油三酯一线治疗药物。
(2)抗氧化剂:维生素E 800U/d可作为无糖尿病的NASH成人的一线治疗药物。但尚未推荐用于合并糖尿病和肝硬化的HASH患者。
(3)护肝抗炎药:无足够证据推荐NAFLD/NASH患者常规使用护肝药物。可以根据疾病的活动度、病期、药物的效能选择以下药物:如必需磷脂、还原型谷胱甘肽、水飞蓟素。
(4)中医药治疗:常用中药有丹参、泻泽、草决明、山楂、柴胡等。
4.外科手术
(1)减肥手术:BMI>40kg/m 2 ,或>35kg/m 2 伴有并发症如难以控制的2型糖尿病可以考虑减肥手术。
(2)肝移植:推荐肝衰竭晚期NASH患者进行肝移植。然而部分患者肝移植后容易复发,并迅速进展至NASH和肝硬化,可能与遗传以及术后持续性高脂血症、糖尿病和皮质激素治疗等有关。BMI>40kg/m 2 不宜做肝移植。
【随访】
大多数非酒精性脂肪性肝病呈良性经过。少数非酒精性脂肪性肝炎患者可进展为肝硬化、肝衰竭或肝癌。NASH合并肝硬化的患者应进行胃食管静脉曲张和肝细胞肝癌筛查。
主要参考文献
1.华医学会肝脏病学分会脂肪肝和酒精性肝病学组.非酒精性脂肪性肝病诊疗指南.中华肝脏杂志,2010,18:163-166.
2.Shadeb MS,Arun JS.Chapter 104,Nonalcoholic fatty liver disease//Podolsy DK,Camilleri M,Fitz JG,et al.Yamadas Text-book of Gastroenterology.6th ed.New York:John Wiley&Sons Ltd.,2016:2056-2069.
第六节
肝脏血管性疾病

郭津生
肝脏血管性疾病包括:①门静脉血栓形成/肝外门静脉阻塞;②肝动脉疾病(动脉瘤,血栓形成,肝动脉门脉瘘);③血窦阻塞性疾病;④放射诱导的肝病;⑤肝紫癜症和血窦扩张;⑥先天性血管畸形。以上大部分疾病的共同特点是可引起非硬化性门脉高压及相应的病理生理改变。本节主要介绍门静脉血栓形成/肝外门静脉阻塞、巴德-吉(基)亚利综合征(Budd-Chiari综合征,布-加综合征)及肝窦阻塞综合征。
一、门静脉血栓/肝外门静脉阻塞
门静脉血栓形成(portal vein thrombosis,PVT)定义为肝外门静脉系统内血栓形成,可向肝内门静脉分支或向远端肠系膜上静脉、脾静脉延伸;肝外门静脉阻塞(extrahepatic portal vein occlusive,EHPVO)还包括血栓以外的其他病因如恶性肿瘤浸润或压迫导致门静脉血向肝内回流受阻。PVT可分为急性和慢性,其分类无明显时间限定,区分急慢性血栓的简单方法为急性血栓无侧支血管和门静脉海绵样变。PVT可发生于儿童、肝硬化患者和肝移植受体,其表现和治疗也因病因不同有所区别。PVT是引起肝前性门脉高压的主要原因。

(资源60) 慢性肝病门脉血栓形成的诊断与治疗(幻灯)
【病因和发病机制】
与多种局部和全身危险因素有关,这些因素引起血管壁损伤、血流减慢、高凝状态和易栓症(thrombophilia)。在急性PVT比慢性PVT更容易识别病因。
(一)局部因素
1.肝硬化
是PVT发生的首要因素,大部分是部分PVT。PVT是肝硬化的重要并发症,发生率随硬化的严重程度而增加。许多患者PVT发生隐匿。代偿期肝硬化患者PVT发生率约0.6%~5%,失代偿期患者可达25%,与门静脉血流改变、终末期肝病凝血状态异常有关。
门脉血流下降,肝内血管阻力增加,是促凝因素。慢性肝病时促凝和抗凝内在平衡能力下降;肝硬化时血小板数目和功能缺陷导致出血倾向,但Ⅷa/vWF水平增加,血小板黏附增加;血浆促凝(Ⅷ因子)和抗凝(蛋白C)平衡的结果是Ⅷ因子作用更强和高凝潜能。肝硬化患者发生PVT/EHVPO的危险与肝病严重程度、内毒素血症、硬化剂及氰基丙烯酸胶注射、是否脾切除、外科门体分流手术、TIPS失功能,是否并发肝癌,有否先天性血栓形成性疾病和携带易形成血栓的基因多态性有关。门静脉所属脏器恶性肿瘤(伴或不伴门静脉浸润和压迫);如原发性肝胆管癌、转移性癌。
2.腹腔内感染或炎症性疾病
如急慢性胰腺炎、憩室炎、阑尾炎、炎症性肠病和肝脓肿、新生儿脐炎、先天性胆总管囊肿、十二指肠溃疡、胆囊炎、结核性淋巴结炎、巨细胞病毒性肝炎。
3.门静脉系统损伤
如腹部外科手术(脾、结肠、胃、胆囊、胆管、肝移植等),腹部外伤。
(二)全身因素
主要包括潜在的遗传或获得性易栓症(见第十六篇第七章第十四节有关“血栓栓塞性疾病”部分),对其识别和筛选有助于制定治疗方案和评估预后。
1.恶性肿瘤以及全身炎症反应 引起或共同引起PVT/EHVPO的常见原因。
2.髓增生性疾病(Myeloproliferative disorders,MDS)没有癌症或硬化的年轻成年人,PVT常是髓系增生性疾病(典型或不典型,V617F JAK2阳性及阴性)的发病表现。
3.凝血抑制因子缺陷 抗磷脂综合征,阵发性睡眠性血红蛋白尿症,Behcet病,凝血因子Ⅴleiden、因子Ⅱ变异,蛋白C、蛋白S缺陷,抗凝血酶缺陷,凝血酶原缺陷等。G20210A凝血酶原杂合子、高同型半胱氨酸血症(与MTHFR多态性有关)。急性PVT时全身性炎症反应可改变这些抑制因子的基线水平;慢性PVT患者,即使肝功能失代偿不明显凝血因子和抑制因子的合成也可有非特异性改变。
4.口服避孕药或雌激素替代治疗。
【临床表现】
(一)急性PVT
1.腹痛或腰痛 突然发生或逐渐进展。如血栓不延展到肠系膜静脉弓,症状可随血管再通或海绵样变的形成而完全好转。门静脉或肠系膜静脉快速和完全阻塞而不累及肠系膜静脉弓可引起肠道淤血,表现为严重持续性腹部绞痛有时伴非血性腹泻。
2.中度腹胀但无肠梗阻表现。
3.腹水、静脉曲张出血、血性腹泻 肝硬化PVT可导致门脉压力增高,肝脏血流下降,诱发胃肠道出血,肝功能异常和腹水。
4.全身炎症反应 持续性的、无高峰的发热和腹痛。
5.透壁肠缺血、肠坏死的表现 持续性严重腹痛超过5~7天,绞痛并放射到背部,血性腹泻和腹水。酸中毒、肾或呼吸道失功能也提示肠梗死。病情进展可出现肠穿孔、腹膜炎、休克和多器官衰竭而死亡。肠坏死的出现与完全性静脉流出阻塞有关(血栓延展累及远端肠系膜静脉,此时肠系膜弓不再能成为侧支途径)并反映动脉受压和阻塞。
6.急性脓毒性PVT(常称急性门静脉炎)以出现感染性单发或多发血栓为特点,临床表现包括高热伴寒战、肝痛,有时出现休克,还可能出现脓毒症有关的胆汁瘀积。血培养类杆菌属阳性伴或不伴其他肠菌生长。此时常见多灶性的小的肝脓肿。急性化脓性PVT总伴有腹腔内感染灶,原发灶在临床上容易被忽视,需仔细通过CT或 MR检查发现。
(二)慢性PVT/EHVPO
门静脉主干或两条主要分支完全阻塞伴随门脉高压和门体侧支循环的形成。替代阻塞门静脉的侧支的数目、大小和部位在不同的患者有很大差别。典型变化为门脉海绵样变(cavernous transformation of the portal vein,CTPV)。
最常见的表现是门脉高压伴反复静脉曲张出血,脾亢。阻塞部位门静脉、胃窦、十二指肠、胆道静脉、胰静脉可显著扩张,压迫大胆管引起变形。出现胆汁淤积提示海绵状血管瘤等因素引起的胆树受压(又称门脉性胆管病,portal cholangiopathy)。
【实验室检查】
血浆急性时相反应物常显著增高。肝功能可能因肝动脉血流增加补偿了下降的门静脉血流而维持正常,或表现为血清转氨酶水平瞬时的、中等度的增加。红细胞压积或血小板计数增高提示潜在的髓系增生性疾病。
【影像学检查】
超声检查可显示管腔内高回声并向门静脉及其分支延伸。多普勒图像显示部分或所有管腔血流缺失。CT和MRI可显示门脉栓子,并帮助判断血栓是新发(缺少侧支循环)还是慢性的(出现海绵样变改变)(图15-8-3)。长期门静脉血栓形成可能会引起肝脏轮廓不规则(可能是由于血流不匀称所致),导致肝硬化的影像学表现。CT和MRI血管造影比多普勒超声更为敏感,能清晰显示肠系膜静脉。
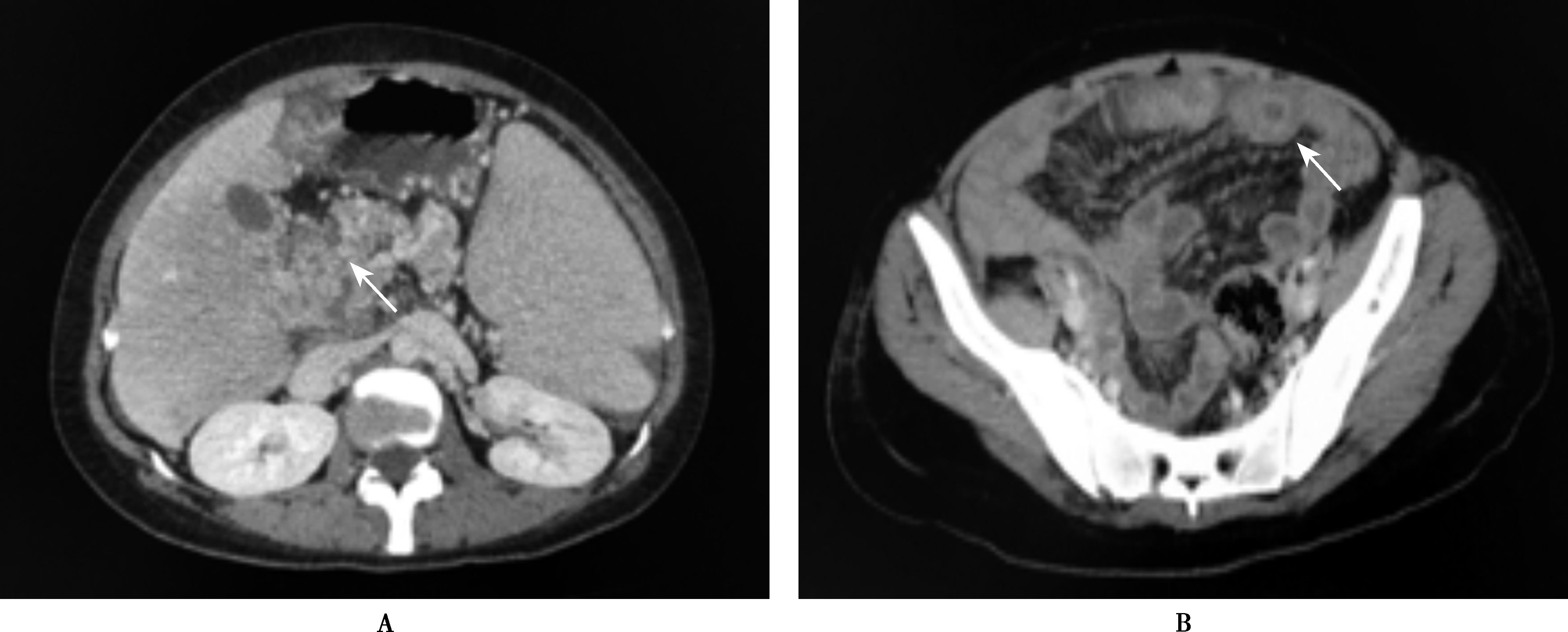
图15-8-3 门静脉血栓形成的CTA表现
A.肝硬化,脾大伴局部梗死,肝门区结构紊乱;肠系膜上静脉及分支、门脉主干广泛血栓,门脉海绵样变(箭头);B.中下腹小肠管壁水肿增厚(箭头)
【诊断及鉴别诊断】
(一)诊断
1.急性PVT
腹痛超过24小时伴或不伴发热或腹泻的患者均要考虑PVT的可能,如怀疑急性PVT则可行超声或CT(平扫或增强)检查。有高热和寒战的急性PVT患者要考虑化脓性门静脉炎并行血培养细菌学检查。持续腹痛、出现腹水、肠壁变薄或增厚的肠壁缺少增强显影、出现多脏器衰竭应考虑肠坏死的可能性,需考虑外科探查。门静脉血流紊乱、血栓证据或出现门脉海绵样变是诊断PVT的要素。多普勒超声检查常足以建立诊断,对比增强计算机断层显像(CT)或腹部磁共振图像(MRI)有助于判断PVT向肠系膜静脉的延伸,以及出现肠梗阻或门脉胆管病。
2.慢性PVT/EHPVO
新诊断门脉高压患者需考虑。门静脉血流紊乱、血栓证据或出现门脉海绵样变是其诊断要素。多普勒超声或CT、MRI有助诊断。针对病因应全面筛查易栓症。
(二)鉴别诊断
需对症状、急慢性及严重程度、并发症及潜在疾病进行鉴别。
1.肠梗阻具有腹胀伴停止排便、排气等其他肠梗阻表现。
2.腹膜炎腹痛伴腹部压痛、反跳痛的腹膜炎体征。
【治疗】
(一)急性PVT的治疗
治疗目的是再通阻塞的静脉、防止血栓延伸、防止肠坏死和门脉高压。高热和血白细胞增高者应使用抗生素。
1.抗凝治疗
急性期抗凝治疗应使用低分子量肝素(LMWH),然后口服华法林维持INR 2~3。抗凝治疗患者应在超声下在第1、3个月和以后每6个月监测。目前推荐不管门静脉再通与否均需长期抗凝治疗。
发生EHPVO和开始抗凝治疗时间间隔长、治疗前已出现腹水、伴有脾静脉血栓形成的患者抗凝再通效果差。肝硬化合并门静脉血栓的治疗请见肝硬化章节。
2.介入治疗
对于肝外门脉狭窄所致门脉血栓,采用球囊血管成形术或和支架植入术,解除梗阻因素即可恢复门脉血流;门脉主干完全闭塞合并肝内门脉分支广泛血栓,建议TIPS途径取栓、溶栓治疗。充分的抗凝伴随于整个介入治疗过程。
3.其他治疗
如血栓切除,外科血栓切除后复发常见,因此一般只在怀疑肠坏死而需外科手术患者进行。溶栓治疗应考虑到出血的危险,因此应局限于严重或进展性疾病、对抗凝治疗无反应者,并权衡有效性和风险-受益比。
(二)慢性PVT/EHPVO的处理
主要是预防和治疗胃肠道出血、防止血栓再次形成和治疗门脉胆管病。慢性PVT使用抗凝治疗存在争议,主要是因为有门脉高压相关出血的危险,应在有效的预防出血措施下[如使用β受体阻断药和(或)内镜下套扎]进行,特别是在具有血栓发生发展危险的潜在疾病患者。超选择性、阶段性抗凝药物输入治疗可能减少并发症。
1.门脉高压并发症的处理与肝硬化患者相似。
2.经颈静脉肝内门体分流(TIPS)可恢复血管血流并允许在有高危曲张静脉出血的患者进行抗凝治疗。TIPS应在伴或不伴肠缺血、已进行抗凝治疗或为禁忌的进展性PVT患者考虑使用。TIPS也可运用于控制曲张静脉出血和内镜治疗症状性门脉胆管病失败的慢性EHVPO患者、以及出现门静脉海绵样变而肝内PV分支开放患者。
3.解压外科手术 主要包括远端脾肾分流或H移植肠腔分流。可在内镜治疗出血失败或胆道并发症、特别是不能进行TIPS的患者考虑。
(三)伴PVT的肝硬化患者的肝移植外科治疗
伴PVT的肝硬化患者肝移植技术难度高,近期存活和死亡率均高。门静脉再栓塞机会高(9%~42%),并与PVT分期、Child-Pugh分级、以及是否因酒精性肝病进行移植等有关。
【预后】
急性PVT的死亡率可很高,早期抗凝治疗可影响血栓再次发生和(或)海绵样变相关的长期生存率。PVT引起肠梗死可导致20%~50%的致死率。因潜在的血栓形成疾病新的血栓发生事件每年约为5%。5%的病例发生胆管并发症,可能严重到危及生命。慢性骨髓增生性疾病的患者特别是骨髓纤维化真性红细胞增多症,其预后多与潜在的血液系统紊乱有关。
二、巴德-吉(基)亚利综合征
巴德-吉(基)亚利综合征(Budd-Chiari syndrome,BCS)是在无右心衰和缩窄性心包炎的情况下,由肝小静脉至回流入右心房的下腔静脉连接处之间的任意段病变导致肝静脉流出道堵塞所引起,是引起肝后性门脉高压的主要原因。堵塞主要是由于血管内血栓形成所致,血栓的形成可能是突发的,也可能长期反复发生并伴有血管再生和不同程度的肝实质损伤和一系列临床表现。根据静脉堵塞的位置和解剖,BCS可分为三种类型:①肝静脉型(隔膜型和广泛肝静脉闭塞型);②下腔静脉型(隔膜型和节段型);③混合型(肝静脉+下腔静脉型)。门静脉血栓形成(PVT)可同时发生在约15%的BCS患者。
BCS治疗初始必须考虑阻塞程度、阻塞原因、肝脏结构和功能损害的严重程度等问题。对具有暴发性过程或已发生伴有肝衰竭的肝硬化患者应考虑肝移植。治疗的选择需根据每个患者的临床情况和胃肠病学、介入放射科、移植外科医生的密切协作。
【病因、发病机制】
可分为原发性(原发于静脉有关疾病如血栓形成、静脉炎)和继发性(静脉外来源的良、恶性肿瘤压迫)。
常见病因有:①肝上下腔静脉膜样蹼;②遗传或获得性疾病引起高凝状态和血栓形成倾向是BCS的潜在危险因素,可导致肝静脉和(或)肝上下腔静脉的血栓形成;③肿瘤压迫和浸润肝静脉和(或)下腔静脉,如肾或肾上腺肿瘤、后腹壁肉瘤、肝细胞癌、下腔静脉肿瘤;④其他可引起肝静脉和(或)下腔静脉阻塞的疾患,如肝棘球蚴病及肝脓肿;⑤使用避孕药是BCS的一个偶发因素,尤其是高雌激素含量药片,它与血栓形成倾向缺陷的杂合子或纯和子状态有关;⑥妊娠妇女(通常是产后)BCS:与雌激素改变、下腔静脉受压和生理性高纤维蛋白原血症有关。
【病理】
肝静脉总的流出道受阻,肝脏发生进行性的广泛小叶中央性淤血、肝实质细胞缺血、坏死、肝纤维化等病理变化,最终出现窦后性门脉高压症的肝大、腹水、出血性食管胃静脉曲张。
【临床表现】
临床表现的严重性取决于肝静脉阻塞的速度和程度。传统上将BCS分为暴发性(5%)、急性(20%)、亚急性或慢性BCS(60%)三种类型。无症状性BCS(无腹水或腹痛)约占病例的15%,通常在检测意外发现肝功能轻微异常后被诊断。BCS也可表现为暴发性肝衰竭。在一些急性BCS患者有慢性疾病(如新形成的血栓联合之前形成的亚临床血栓)的组织学证据。肝细胞癌可使BCS更加复杂,其发病率和其他慢性肝病相似。
典型的临床表现一般仅在大部分肝静脉流出道被阻塞(至少两支肝静脉或肝上腔静脉发生阻塞)的情况下才会出现,表现为:
1.腹水
最常见,伴轻或中度腹部不适、肝大、右上腹不适、黄疸、静脉扩张、踝部水肿。
2.腹痛
急性发作,伴肝脏增大和腹水。
3.下肢水肿和静脉侧支、甚至下肢溃疡
提示下腔静脉的受压或血栓形成。
【诊断与鉴别诊断】
诊断主要基于肝静脉流出道堵塞的临床表现,有腹水和肝淤血证据的患者均应考虑BCS的可能。对出现急性腹痛,肝脏增大尤其是伴已知的血栓形成倾向性疾病,或当暴发性肝衰竭伴腹水的患者,应考虑BCS这一诊断。难治性腹水,尤其是肝功能检查相对正常时,应排除慢性BCS。腹水SAAG较高。
实验室检查发现潜在基础疾病是探寻肝静脉流出受阻解剖异常病因的重要方法。多普勒超声诊断是推荐使用的一线检查方法。此外,CT扫描或MRI可显示肝实质地图样强化的典型诊断特征。肝静脉阻塞的发现可借助多普勒超声显影、三维计算机体层摄影术、三维对比加强磁共振血管成像、肝静脉造影和延迟门静脉显象的肠系膜动脉造影、磁共振血管造影等。
肝活检可根据特征性小叶中心性充血表现进行诊断并可除外同时存在的肝硬化。需注意不一定所有三条主要的肝静脉都同样程度地受累于血栓形成过程。
介入肝静脉血管成像有助于确定血栓的位置和测定腔静脉的压力,还可进行经颈静脉肝活检、扩张术和(或)肝静脉和下腔静脉支架植入术。如果计划行TIPS而不能进行肝静脉插管时,可通过经腔静脉穿刺到达门静脉(DIPS)。
重要的鉴别诊断是右心衰竭、缩窄性心包炎和其他阻塞性心源性因素。
【治疗】
目的在于纠正阻塞、预防再阻塞、纠治门脉高压及其并发症、以及以最小的不良反应纠正肝功能损害。为实现这些目的所选择的特异的治疗应基于肝静脉回流受阻的解剖水平、病因和生理性影响。预后和治疗结果也很大程度上与肝静脉阻塞部位和程度有关。
(一)药物治疗和并发症的治疗
1.抗凝治疗
除非有禁忌证,所有患者均应进行。先使用静脉肝素,后用华法林或低剂量阿司匹林长期治疗。急性BCS患者,诊断后的72小时之内行早期溶栓治疗。
2.对症治疗
如针对腹水等症状选用抗利尿剂等对症治疗。
(二)介入治疗
1.介入血管成形术、支架植入术或者介入腔内第二肝门重建术
用于阻塞部位局限的局部狭窄或堵塞的患者,如下腔静脉膜性或段性闭塞、局限性肝静脉狭窄或闭塞。
2.经颈静脉肝内门体分流(TIPS)
旨在通过在肝静脉和门静脉肝内部分建立低阻通道以使高压的门静脉内的血流回到心脏,起到建立旁路和减压肝血窦的作用。适用于肝静脉广泛闭塞型BCS。
3.介入溶栓
导管定向的溶栓(尿激酶、链激酶、组织纤溶酶原复合物局部注射)对急性发生的下腔静脉或肝静脉栓塞、没有严重的进行性肝坏死、时间上允许尝试的经选择的某些BCS病例也有效果。溶栓治疗越早进行越好。导管定向的溶栓优于全身给予溶栓药物。血栓溶栓治疗最严重的并发症是肺栓塞。
(三)外科治疗
1.外科分流
急性型和亚急性型BCS可选择解除门静脉压力的手术。早期门静脉减压是提高生存和生活质量的关键,以阻止不可逆的肝细胞损伤的发生,减少肝衰竭和死亡的危险。
2.外科血管置换
先天性异常或外伤损伤引起的下腔静脉阻塞可通过外科血管置换解除阻塞。
3.肝移植
适应证包括:①暴发性BCS;②先天性代谢性疾病(如抗凝血酶III缺陷),可通过肝移植纠正遗传缺陷;③终末期肝病的BCS患者;④解压性分流(TIPS或外科分流手术)失败或分流后失代偿患者;⑤伴广泛门静脉系统血栓形成(少见)的不能分流的门脉高压患者。
对OLT后不能解除高凝状态的患者需接受长期抗凝治疗。
【预后】
病因、发病速度、肝脏失代偿的严重性、血栓形成的解剖学位置决定了BCS的预后。
三、肝窦阻塞综合征/静脉闭塞性疾病
肝窦阻塞综合征/肝小静脉闭塞病(hepatic sinusoidal obstruction syndrome/veno-occlusive disease,HSOS/VOD)是一种以肝大、腹水、体重增加和黄疸为特点的临床综合征。临床过程严重程度不等,可分为①轻型:症状可消失,血清胆红素水平降至低于2mg/dl;②中型:临床症状和体征进行性加重,出现腹水和(或)胸膜渗出,但没有多器官衰竭(MOF);③重型:发生 MOF,呼吸衰竭和(或)肾衰竭和(或)肝性脑病。
【病因】
(一)毒素和药物
主要见于食用了含有吡咯双烷生物碱(pyrrolizidine alkaloids,PAs)的植物或食物,我国主要见于土三七中毒。HSOS还与其他毒物如酒精、口服避孕药、毒油、特比萘芬或放射性损伤有关。
(二)造血干细胞移植(SCT)及器官移植
国外报道造血干细胞移植(SCT)相关及其他实质性器官移植尤其是肾移植后发生HSOS的报道,主要与硫唑嘌呤、环磷酰胺毒性有关。
(三)实体肿瘤化疗
使用过量化疗方案的患者中HSOS的发生率很高。新的化疗药物尤其是吉妥单抗-奥唑米星和奥沙利铂,有较多报道引起肝窦毒性。
【病理生理学和组织学】
由于较轻的VOD患者肝小静脉损伤不显著,而且实验研究发现该病血流的阻塞最早发生在肝窦,已提出用肝窦阻塞综合征(HSOS)来代替肝静脉闭塞性疾病(VOD)这一术语。
早期的组织学异常包括:伴小叶中央坏死的肝窦充血和之后的肝小静脉纤维性闭塞性病变,伴位于腺泡3区的组织学损伤。肝窦和肝脏小静脉内皮的广泛损伤导致了凝血级联反应的激活和血栓形成。纤维蛋白性栓子、细胞碎片等进行性地阻塞肝窦,导致肝内窦后性门脉高压,从而出现液体潴留、肝大、腹水和黄疸等临床表现。通常在发病几周后会发生纤维化。
【临床表现和辅助检查】
典型临床表现是液体潴留导致的体重快速增加、疼痛性肝脏肿大和不明原因的高胆红素血症。
在临床表现和实验室指标异常(发现PAI-1、Ⅲ型前胶原及其前体肽P-Ⅲ-P等的血清水平升高)出现之前,就可怀疑有内皮性损伤。血清透明质酸、vWF-裂解蛋白酶ADAMTS13和CA125已被评价作为HSOS的早期标志。其他内皮损伤标志如血栓调节蛋白和P选择素也增高。
腹部多普勒超声检查是一线的影像学检查方法。可发现腹水、肝大、肝静脉变细和(或)胆道扩张等表现。然而,这些特征都不具有诊断特异性,必须结合临床情况综合考虑。
脉冲多普勒超声观察到门静脉血流减少或逆向可提示HSOS。二维超声图中肝动脉阻力指数显著升高可能是HSOS相关性肝损伤的一个敏感指标。
CT可见肝脏斑片状增强;CTA或MRA可除外肝静脉流出道阻塞,以与BCS鉴别。
肝静脉导管术可测定肝静脉压力梯度(HVPG)和行肝活检。肝静脉和下腔静脉间缺乏显著压力差(<6mmHg)可排除流出道堵塞的解剖学因素。HVPG还有助于判断预后,HVPG大于20mmHg与不良预后相关。
【诊断】
诊断主要基于症状和体征,病史(尤其是服用土三七、含有或污染PAS的食物,以及SCT史),还可通过超高效液相色谱-串联质谱法(UPLC-MS)检测血中吡咯-蛋白质加合物浓度诊断PAs相关HSOS和评估预后。
常用HSOS临床诊断标准有:
1.Baltimore标准
血清总胆红素水平上升(≥2mg/dl),并有以下三条标准中至少2条:①有触痛的肝大;②体重上升超过基线>5%;③腹水。
2.Seattle标准
在SCT后20天内发生以下事件中的2项:①高胆红素血症(≥2mg/dl);②肝大或肝脏源性右上腹痛;③因液体积聚所致不能解释的体重增加(超过基线>2%)。
患者有用药史,符合上述临床标准,加上彩超多普勒逆向血流以及CT肝脏斑片状增强表现,除外BCS,基本上可以作出诊断。肝活检和HVPG测定为金标准。
【鉴别诊断】
如病毒感染肝炎、自身免疫性肝病、酒精性肝病、Budd-Chiari综合征、肝脏遗传性疾病、移植物抗宿主病、继发性胆汁淤积性败血症、心力衰竭和肝脏肿瘤浸润。
【治疗】
1.支持治疗
通过限制钠的摄入、利尿剂和腹腔穿刺术来治疗腹水。在严重的患者常需纠正凝血紊乱、脏器衰竭和预防感染,并通过清除肠道感染来避免细菌的异位。
2.特异性治疗
早期应给予抗纤维蛋白溶解剂以促进纤维蛋白的降解,伴或不伴抗凝治疗,但发生严重出血时应避免使用。
去纤维蛋白多核苷酸[10~60mg/(kg·d),每6小时1次]是一种具有抗纤维蛋白溶解和抗栓活性的多聚脱氧核苷酸,可减少白细胞滚动和与内皮的黏附,降低凝血因子的产生和循环中PAI-Ⅰ的水平。
3.经颈静脉肝内门体分流术(TIPS)
有助于解除充血肝窦的压力,减轻门脉高压和预防HSOS患者发生肾衰竭。严重HSOS已发生MOF患者一般不建议TIPS治疗。
4.肝移植
可作为对药物治疗无反应的SCT后HSOS患者的抢救性治疗。恶性肿瘤和多器官衰竭的存在是OLT的禁忌证。对肝移植本身之后发生的HSOS,由于肝脏是唯一损伤器官,可再次行肝移植作为抢救性治疗。
【预防】
由于严重HSOS患者缺乏有效的治疗方法,必须优先采取预防措施。
1.误服土三七是我国引起HSOS的主要原因。应加强宣教,提高民众及医务人员警惕性。
2.识别高危患者 危险因素有:①最近使用可引起HSOS的药物(如吉妥单抗);②既往HSOS病史;③罹患某种肝脏疾病如丙型肝炎、肝纤维化;④与HSOS发生危险相关的基因多态性:如谷胱甘肽S转移酶和TNF-α基因多态性。对有HSOS危险因素的患者应避免肝毒性药物或优化治疗方案。
3.药物预防 可考虑使用:①肝素和低分子量肝素;②去纤维蛋白多核苷酸;③己酮可可碱;④熊去氧胆酸(UDCA):作为一种解毒剂和抗细胞凋亡剂的可用做预防性治疗药物。⑤前列腺素E1:是一种具有内皮保护作用的血管扩张剂且具有抗栓活性。
【预后】
HSOS患者体重增加的比例、胆红素、腹水和末梢水肿与存活较差有关。HVPG>20mmHg是独立的死亡预测标志。
主要参考文献
1.Waini ZA,Bhat RA,Bhadoria AS,et al.Extrahepatic portal vein obstruction and portal vein thrombosis in special situations:need for a new classification.Saudi J Gastroenterol,2015,21(3):129-138.
2.Chawla YK,Bodh V.Portal vein thrombosis.J Clin ExpHepatol,2015,5:22-40.
3.EASL clinical practice guidelines:Vascular diseases of the liver.J Hepatol,2016,64:179-202.
第七节
肝脓肿

蒋 炜
肝脓肿(liver abscess)是指肝实质内单发或多发的脓性物积聚,大多是细菌性、阿米巴性或混合性脓肿,是消化系统常见严重疾病。而细菌性肝脓肿是指化脓性细菌侵入肝脏,造成局部肝组织炎症、坏死、液化,脓液积聚而形成的肝内化脓性感染。在本章节中将重点介绍细菌性肝脓肿,阿米巴性肝脓肿参见第十篇第十三章第二节阿米巴病。
【流行病学】
细菌性肝脓肿多继发于体内其他感染,最常见于胆道感染(尤其由胆道手术、胆管结石、恶性肿瘤、蛔虫梗阻所致感染)或身体其他脏器感染所致菌血症,常见于阑尾炎、憩室炎时细菌经肠系膜循环入门静脉侵入肝脏。炎症性肠病(尤其是克罗恩病)时肠黏膜屏障的受损亦为肝脓肿的危险因素。此外,未经治疗的口腔感染和细菌性心内膜炎所致菌血症也不可忽视。而钝性或穿透性肝损伤和邻近器宫脓肿扩大至肝脏引起肝脓肿则较为少见。临床上也有部分患者的传播途径不明,称之为隐源性肝脓肿。细菌性肝脓肿发病率没有明显的性别、种族或地理差异,50~70岁的年龄发病率相对较高,近年来糖尿病成为肝脓肿的易患因素。
【病原学】
20世纪80年代以前,普遍认为引起细菌性肝脓肿的病原体以肠道来源菌群为主,如大肠埃希菌及其他肠杆菌科,链球菌属及肠球菌属。随着病原菌流行病学变化及抗生素的广泛应用,过去10年间,在东南亚,肺炎克雷伯杆菌已取代大肠埃希菌等占据主要地位;在中欧,细菌性肝脓肿主要病原菌是大肠埃希菌、链球菌或金黄色葡萄球菌。其中肺炎克雷伯杆菌性肝脓肿多伴发于糖尿病患者。一方面,糖尿病患者的葡萄糖降解率减少,为白细胞提供能量功能受抑制,中性粒细胞趋化功能缺陷,杀菌活性减弱;另一方面,长期高血糖有利于细菌生长,尤其是呼吸道、泌尿道、皮肤和女性外阴部等处;同时,糖尿病患者易发生血管病变,导致局部血液循环障碍,周围组织供氧减少,不仅影响局部组织对感染的反应,也有利于厌氧菌生长和降低白细胞依赖氧的杀菌能力。
【临床表现】
细菌性肝脓肿的症状都是非特异性的。临床上常见高热、全身乏力、食欲缺乏、体重减轻。也有约5%~20%患者无发热症状。约一半患者有肝区疼痛。约1/3患者有恶心呕吐。少数患者可有黄疸,除非继发于胆道感染,否则一般出现较迟。体格检查可发现肝大、压痛、肝区叩痛。
【实验室检查】
实验室检查白细胞计数明显升高,核左移或有中毒颗粒。部分患者有贫血。大部分患者有血沉增快,部分患者可出现肝功能轻度异常(血清ALP、GGT多增高),同时应对患者行血糖检测。
【影像学检查】
1.X线检查
右叶肝脓肿可有右侧膈肌升高,活动度减小;并发脓胸或支气管胸膜瘘者,肋膈角消失并有肺内阴影。
2.超声
超声常作为诊断首选。脓肿前期,病灶为不均匀、边界不清楚的低回声区,周围组织水肿可产生较宽的声圈。肝脓肿液化后,表现为边缘清楚的无回声区,壁厚。脓腔内可随液化程度形成不同的回声表现。
3.CT检查
平扫时,脓腔为单发或多发低密度区,巨大脓腔的内壁不规则。病灶边界多数不清楚,脓肿壁呈稍高于脓腔低于正常肝的环形带。增强扫描后,脓肿壁可呈单环、双环甚至三环,由外到内分别为水肿、纤维肉芽组织和炎性坏死组织的病理结构。
4.MRI检查
具有多序列成像及功能成像的优势,TIW1中表现为低信号,T2W1中为高信号。脓肿腔可表现为均匀或不均匀信号,注入对比剂后,肝脓肿典型表现为周边强化,而后病变中央信号缓慢升高。
【诊断】
感染性疾病(尤其是胆道感染、菌血症者)出现高热、肝区疼痛及肝区叩击痛、肝大并触痛者,应高度怀疑。结合腹部B超、CT和MRI诊断多不困难,B超、CT可检出>2cm脓肿病灶,而MRI可检出<2cm脓肿病灶。肝穿刺抽得脓液即可确诊。
【鉴别诊断】
1.阿米巴肝脓肿
本病发展过程较为缓慢,主要为发热、肝区疼痛及肝大。粪检常能发现阿米巴包囊或滋养体,超声检查脓肿所在部位可显示不均质的液性暗区(表15-8-13)。
2.右膈下脓肿
多继发于化脓性腹膜炎或上腹部大手术后。全身反应如寒战、发热等和局部体征不如肝脓肿明显,但右肩牵涉痛较显著,深吸气时尤重。X线检查右膈下常有液气面出现,右侧横膈升高,膈肌运动受限。
表15-8-13 细菌性肝脓肿与阿米巴肝脓肿的鉴别诊断
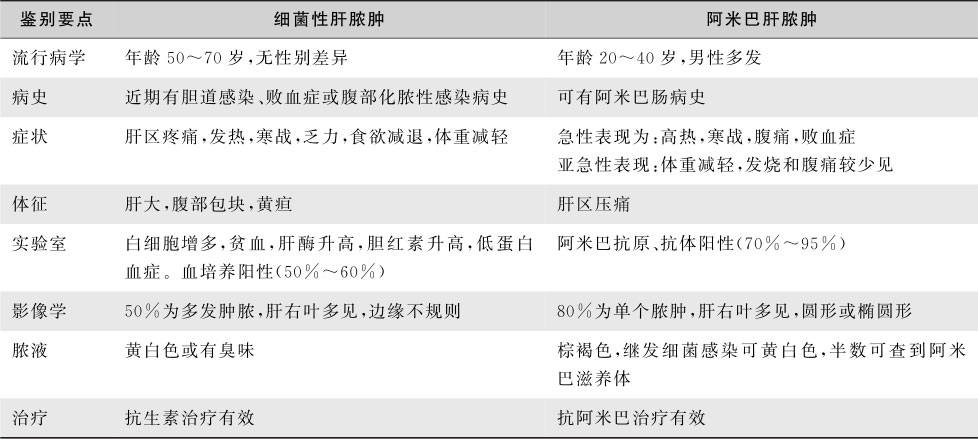
3.原发性肝癌
巨块型肝癌中心坏死液化,继发感染时临床表现与细菌性肝脓肿相近,但前者一般情况较差,肿大肝表面不平有结节感或可触及较硬的包块,血清甲胎蛋白及脓肿穿刺病理学检查有重要鉴别意义。
4.胆道感染
多有右上腹绞痛及黄疸,压痛主要在胆囊区,肝大及肝压痛不明显。X线检查无隔肌升高、运动受限等表现,B型超声检查肝区无液性暗区。
【治疗】
(一)药物
一旦考虑为细菌性肝脓肿,需尽早使用抗生素治疗。对于脓肿直径≤3cm及散在小脓肿、脓肿早期且尚未完全液化、局部中毒症状轻者,选择应用能覆盖G + 及G - 细菌的大剂量广谱抗生素,而该病多合并有厌氧菌感染,应加用抗厌氧菌药物。遵循足量、全程的用药原则,防止耐药菌株的产生。同时对合并糖尿病患者应及时药物控制血糖。
(二)介入治疗
随着影像技术的广泛应用,B超或CT引导下经皮肝穿刺抽脓或置管引流术已作为治疗细菌性肝脓肿的首选方案。指征为:①保守治疗效果不佳。②脓肿液化明显,脓肿壁已形成。③脓肿直径>3cm时且直径<5cm,经反复穿刺抽脓即可获得理想疗效;对于直径≥5cm,脓液多且不易抽净而建议行置管引流;对于脓腔≥10cm,有学者建议在B超引导下从不同部位向同一脓腔分别置入2根引流管以便充分引流。④凝血功能正常,全身状况差不能耐受开腹手术者。随着介入超声技术和操作器械的发展,内镜超声引导下细菌性肝脓肿引流治疗成为一种新的选择,其优势在于可以到达经皮穿刺方式不易处理的部位(如肝尾状叶和肝左叶腹腔面脓肿)。
(三)外科手术治疗
虽经皮肝穿刺抽脓或置管引流术已成为主流,但仍无法取代外科手术治疗。其手术指征为:①经皮肝穿刺抽脓或引流效果不佳;②脓肿直径≥5cm并合并中毒症状重者;③脓肿破溃或有破溃可能者;④特殊部位脓肿(如尾状叶、膈顶部、及左外叶)的脓肿;⑤伴有胆道系统疾病(胆石症、肝硬化,胆道出血等)需手术治疗者;⑥不能很好配合穿刺者。随着微创外科的进步,腹腔镜治疗可有效地处理多房性细菌性肝脓肿及对脓肿破裂后行腹腔灌洗引流。而对于部分局限性肝脓肿、脓肿壁厚或位于肝脏边缘较大脓肿有破溃可能致感染扩散者则可考虑行肝部分切除术。
【预后】
随着诊疗技术的进步,多数病例采取超声或CT定位经皮肝穿刺抽脓、引流、高效广谱抗生素等非手术疗法而治愈。患者预后显著改观,病死率已由原来的70%下降到近年的4%~16%。然而如果不能得到及时有效的治疗,患者可并发败血症死亡。
主要参考文献
1.Liu Y,Wang JY,Jiang W.An Increasing Prominent Disease of Klebsiella pneumoniae Liver Abscess:Etiology,Diagnosis,and Treatment.Gastroenterol Res Pract,2013,2013:258514.
2.Singhal S,Changela K,Lane D,et al.Endoscopic ultrasound-guided hepatic and perihepatic abscess drainage:an evolving technique.Therap Adv Gastroenterol,2014,7(2):93-98.
第八节
肝肿瘤

一、原发性肝癌
任正刚
原发性肝癌(primary carcinoma of the liver,以下简称肝癌)是原发于肝脏的上皮性恶性肿瘤,其中超过80%的肝癌为肝细胞癌,其余为胆管细胞性肝癌和混合型肝癌。
【流行病学】
肝细胞癌的发病率在全世界恶性肿瘤中男性居第六位,死亡率居第三位。全球每年新发病例约70万,其中一半发生在我国。中国是肝癌发病的重灾区,据统计,2011年中国肝癌发患者数约35.6万,发病率为26.39/10万。由于在上世纪90年代开始实行了新生儿乙肝疫苗的接种,肝癌的年龄标化发病率与2000年比较呈现下降趋势,但由于我国人口基数大及老龄化进程加快,肝癌粗发病率仍然呈上升趋势,目前仍然是我国最常见的恶性肿瘤之一。
【病因和发病机制】
(一)病毒性肝炎
乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)和肝癌发生有关。在亚洲(日本除外)HBV感染是肝癌的主要发病因素。在原发性肝癌的患者中,有乙型肝炎感染背景者占80%以上。前瞻性的队列研究结果显示,有HBV感染的人群,发生肝癌的危险性较普通人群高5~100倍。其中,HBsAg阳性者较阴性者危险性更高;病毒载荷量和患肝癌的危险性呈正比。在欧洲、北美,以及日本,HCV感染是肝癌的主要发病因素。HCV在日本肝癌患者中的阳性率为80%~90%;意大利为44%~66%;美国为30%~50%。结果显示,HCV抗体阳性的人群较阴性的人群,患肝癌的危险性高15~20倍。其中伴有肝纤维化或肝硬化者发生肝癌的风险要显著高于无肝纤维化或肝硬化者。
(二)黄曲霉毒素
在流行病学上,黄曲霉毒素(aflatoxin B1,AFB1)与肝癌有密切的关系,在我国的东南沿海,气候温暖、潮湿,适宜于黄曲霉的生长,在谷物中黄曲霉毒素的污染较为普遍,这些地区也是肝癌的高发地区。研究表明,AFB1的摄入量与肝癌的死亡率呈正相关。迄今为止,AFB1是已知最强的致癌物,可使多种动物发生肝癌,但尚缺乏导致人肝癌的直接证据,一般认为,黄曲霉毒素污染进一步增加了感染HBV人群患肝癌的危险性。
(三)代谢因素
随着生活方式的改变,代谢因素与肝癌的关系受到关注。糖尿病患者较对照人群患肝癌的风险高2.5倍;西方的研究提示,肥胖和非酒精性脂肪肝成为西方发达国家肝癌的重要发病因素,并认为是美国肝癌发病率提高的重要原因。
(四)长期饮酒和抽烟
可增加患肝癌的危险性,特别是增加HBsAg阳性患者患肝癌的危险性。在中国台湾一项前瞻性的研究中,HBsAg阳性患者发生肝癌的相对危险性为13.1~19.2倍,而HBsAg阳性患者有长期饮酒和抽烟习惯的患者患肝癌的相对危险性为17.9~26.9倍。在我国的肝癌高发区,有肝癌的家族聚集现象,提示肝癌具有遗传的倾向,尚待进一步研究证实。
【病理】
原发性肝癌主要有三种类型:肝细胞性肝癌、胆管细胞性肝癌和混合型肝癌。约4/5为肝细胞性肝癌,1/5为胆管细胞性肝癌和混合型肝癌。
(一)组织学分型
分为肝细胞癌、胆管细胞性肝癌和混合细胞型肝癌。
1.肝细胞型
大多伴有肝硬化。癌细胞呈多角型,核大,核仁明显,胞质丰富。癌细胞排列成巢状或索状,癌巢之间有丰富的血窦。癌细胞有向血窦内生长的趋势。肿瘤分化程度按Edmondson标准分四级,Ⅰ级分化最好,癌细胞形态和正常肝细胞相似,Ⅳ级分化最差,癌细胞核大,形态变异大。肝细胞癌中以Ⅱ、Ⅲ级为多见,同一病例的癌组织可呈现不同的分化程度。透明细胞癌属肝细胞癌,在肝细胞癌中约占10%,属分化较好的肝细胞性肝癌。纤维板层肝癌是肝细胞癌的一种特殊类型,以癌细胞巢间出现大量平行排列的板层状纤维组织为特点,多见于年轻人,常不伴有HBV感染和肝硬化,甲胎蛋白多为低浓度阳性,但预后较好。
2.胆管细胞型
癌细胞呈柱状或立方状,胞质嗜碱性,无胆汁小滴,偶有黏液分泌;排列成腺泡、囊或乳头状;间质组织多。
3.混合型
癌组织中部分似肝细胞,部分似胆管细胞,或细胞形态介于二者之间。
(二)转移
肝癌是高转移潜能的恶性肿瘤。研究显示,即使直径小于2cm的小肝癌,有20%肝癌结节发现有微血管的侵犯。肝癌的转移包括了肝内转移和肝外的远处转移。
1.肝内转移
肝内血行转移发生最早,也最常见,是肝癌切除术后早期复发的主要原因。肝癌容易侵犯门静脉而形成癌栓。肝静脉发生癌栓后,也可进一步侵犯下腔静脉,甚至达右心腔。
2.远处转移
①血行转移:以肺转移最常见,其他常见的转移部位有骨、肾上腺、脑和软组织;②淋巴转移:肝门淋巴结转移最常见(占12.6%),也可转移至主动脉旁、胰周、锁骨上淋巴结;③种植或直接浸润:腹腔种植可形成腹腔肿块,种植于腹膜可形成血性腹水。肝癌也可直接浸润临近的器官如膈肌、胃、十二指肠和结肠等。
【临床表现】
(一)症状
1.亚临床肝癌或小肝癌
肝癌起病隐匿,一旦出现症状和体征大多已经处于晚期。不少肝癌是在体检或普查中发现,这些肝癌患者既无症状也无体征,只表现为甲胎蛋白升高和影像学上的肿块,这些患者称之为“亚临床肝癌”。在这些亚临床肝癌中,大部分肝癌体积小于5cm,称之为“小肝癌”。故多数小肝癌为“亚临床肝癌”,但也有肿瘤直径大于5cm,没有症状和体征的,故亚临床肝癌也包括了一部分直径大于5cm的肝癌。
2.肝癌的症状
肝区疼痛、乏力、纳差、消瘦是最具有特征的临床症状。一旦出现症状而来就诊者则大多已处于中晚期。不同阶段的肝癌,其临床表现有明显的差别。
(1)肝区疼痛:
最常见,多为肝区的间歇或持续性的钝痛或胀痛,由癌肿迅速生长使包膜绷紧所致。如肿瘤侵犯膈肌,疼痛可放射至右肩;左叶肝癌可出现上腹疼痛,可被误诊为溃疡病、胃炎等。向右生长的肿瘤可致右腰疼痛。突然发生的剧烈的肝区疼痛或腹痛提示有癌结节的破裂出血,可有腹水、腹膜刺激征和休克的体征。
(2)消化道症状:
食欲缺乏、消化不良、恶心、呕吐,因缺乏特异性而易被忽视。腹水或门静脉癌栓可导致腹胀、腹泻等症状。
(3)乏力、消瘦、全身衰弱:
晚期少数患者可呈恶病质状。
(4)发热:
一般为低热,偶达39℃以上,呈持续性或午后低热或弛张型高热。
(5)转移灶症状:
有时成为肝癌的首发症状。如转移至肺可引起咳嗽咯血,胸膜转移可引起胸痛和血性胸腔积液。肺动脉及其分支癌栓栓塞,可突然发生严重的呼吸困难、低氧血症和胸痛。癌栓阻塞下腔静脉,可出现腹水、下肢严重水肿;阻塞肝静脉可出现Budd-Chiari综合征。骨转移可引起局部疼痛,或病理性骨折。转移至脊柱或压迫脊髓神经可引起局部疼痛和截瘫。颅内转移可出现相应的症状和体征甚至脑疝而突然死亡。
(6)伴癌综合征:
有时可先于肝癌本身的症状出现。常见的有:①自发性低血糖:见于10%~30%的患者,系因肝癌细胞的异位分泌胰岛素或胰岛素样物质;或肿瘤抑制胰岛素酶或分泌一种胰岛β细胞刺激因子;亦可因肝癌组织过多消耗葡萄糖所致。严重时可引起昏迷、休克而导致死亡;②红细胞增多症:2%~10%患者可发生,可能系循环中红细胞生成素增多引起;③其他:罕见的有高脂血症、高钙血症、类癌综合征、性早熟和促性腺激素分泌综合征、皮肤卟啉症和异常纤维蛋白原血症等,可能与肝癌组织的异常蛋白合成,异位内分泌及卟啉代谢紊乱有关。
(二)肝癌的体征
1.肝大
进行性肝大为最常见的体征之一。肝质地坚硬,表面及边缘不规则,常呈结节状,少数肿瘤深埋于肝实质内者则肝表面光滑,伴或不伴明显的压痛。肝右叶膈面癌肿可使右侧膈肌明显抬高。
2.脾大
多见于合并肝硬化门静脉高压的病例。门静脉或下腔静脉癌栓或肝癌压迫门静脉或下腔静脉也能引起充血性脾大。
3.腹水
草黄色或血性,多因为合并肝硬化、门静脉高压、门静脉或下腔静脉癌栓所致。腹腔内种植可引起血性腹水,肝癌破裂可从腹腔内抽出不凝血。
4.黄疸
当癌肿广泛浸润可引起肝细胞性黄疸;如侵犯或压迫肝内胆管或肝门淋巴结压迫肝管可引起梗阻性黄疸。
5.转移灶相应的体征
可有锁骨上淋巴结肿大,胸膜转移可出现胸腔积液或血胸。骨转移可有局部压痛,有时可出现病理性骨折。脊髓转移压迫脊髓神经可表现截瘫,颅内转移可出现偏瘫等神经病理性体征。
【临床分期】
肝癌的分期包括了主要有国际抗癌联盟的TNM分期(TNM)、巴塞罗那肝癌分期(BCLC)、意大利肝癌分期(CLIP)、Okuda分期、日本整合计分(JIS)等分期系统。目前的分期系统大多整合了肝功能状态和体能状态,如西班牙的BCLC分期。该分期不仅包括肿瘤的大小、数目,血管侵犯、远处转移,也包括了体能状态评分、肝功能Child-Pugh分级。而且,在循证医学证据的支持下,也明确了不同分期肝癌的治疗方法。因此,巴塞罗那肝癌分期(Bacelona Clinic Liver Cancer,BCLC)为国际上广泛应用。该分期如图15-8-4所示。
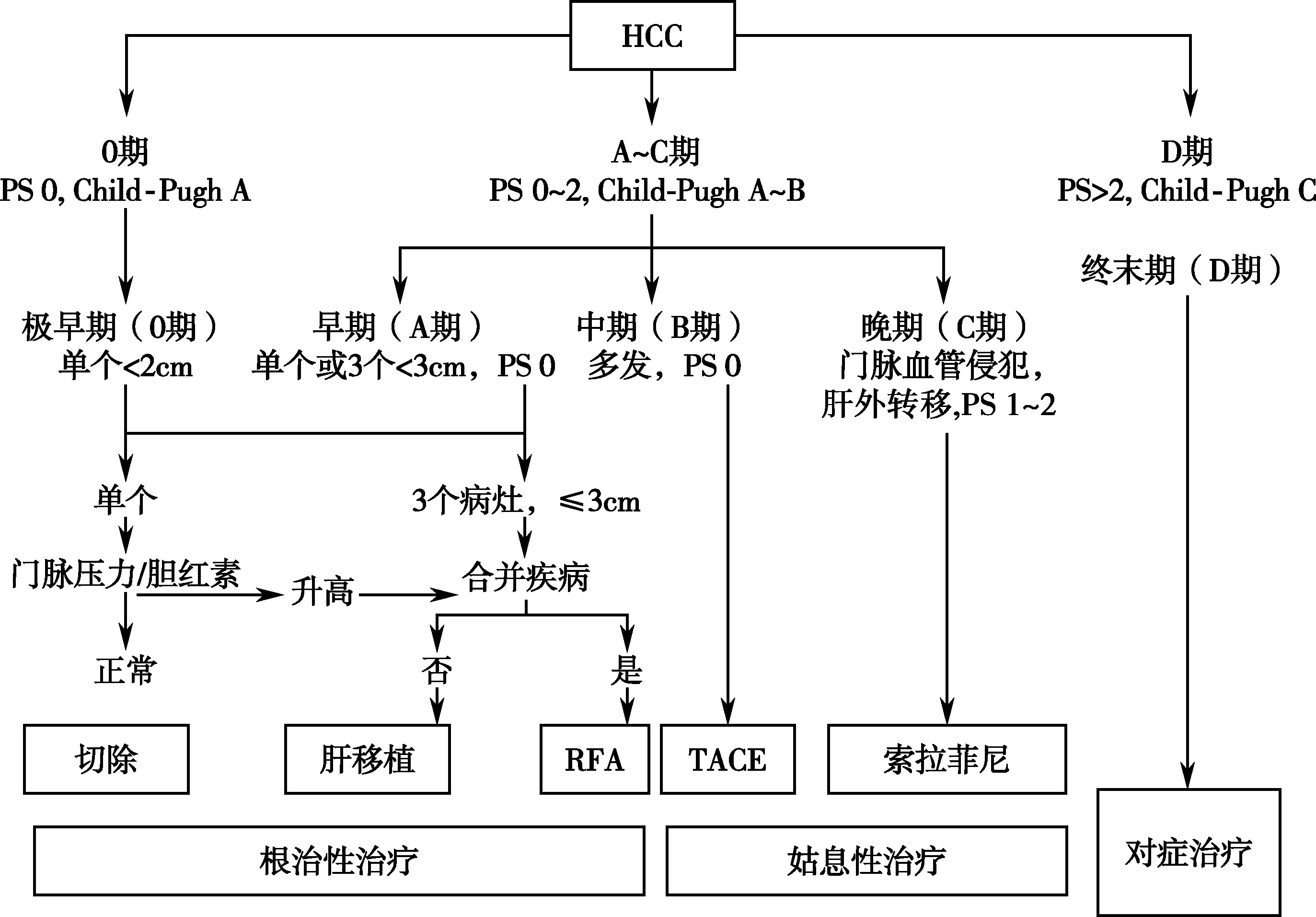
图15-8-4 巴塞罗那肝癌分期
M:转移;N:淋巴结;PS:行为状态;RFA:射频消融;TACE:经动脉化疗栓塞
【并发症】
可由肝癌本身或并存的肝硬化引起,常见于病程的晚期,是肝癌的主要致死原因。
(一)肝性脑病
常为终末期肝癌的并发症。常于肝癌进展、肝功能失代偿后发生,消化道出血、大量利尿或高蛋白饮食等是常见的诱因。
(二)消化道出血
多数因合并肝硬化或及门静脉高压而引起食管或胃底静脉曲张破裂出血。也可因胃肠黏膜糜烂、凝血机制障碍而出血。合并门静脉癌栓可进一步加剧门静脉高压增加上消化道出血的风险。
(三)肝癌结节破裂出血
肝癌组织坏死、液化可致自发破裂或因外力而破裂。多见于巨块型的晚期肝癌,但也可发生于包膜下或外生型小肝癌。如限于包膜下可有急骤疼痛;若破入腹腔引起腹痛,出血性休克或死亡。腹部穿刺抽出不凝固血液可做成诊断。
(四)血性胸腹水
膈面肝癌可直接浸润膈肌或胸膜引起血性胸腔积液,多见于右侧。血性腹水多因腹腔种植转移或肝硬化凝血障碍而致。
(五)继发感染
因癌肿长期消耗,机体抵抗力减弱,尤其在放射或化学治疗后血白细胞下降者,易并发各种感染,如肺炎、肠道感染、自发性细菌性腹膜炎等。
【诊断】
(一)病史和体检
多发于男性,既往有慢性病毒性肝炎、肝硬化、酗酒、非酒精性脂肪肝等病史,或肝癌家族史。近期有无肝区不适、疼痛、发热、黄疸、腹块、黑便、出血倾向、少尿、意识障碍等表现。对于无肝病背景的有肝占位性病变患者,应该了解有无肿瘤手术史和治疗情况。查体要注意肝硬化和门脉高压体征及腹部包块等。
(二)实验室和辅助检查
1.辅助检查
对于超声检查发现肝脏可疑占位性病变的患者,需要进行动态增强CT或MRI检查,以确定肝癌的诊断。CT诊断肝癌的敏感性和特异性分别为55%~80%和89%~96%;MRI的敏感性和特异性为70%~91%和77%~93%。CT和MRI检查中肝癌的特征性改变为动脉期的快速强化,而门静脉期或实质期消退。影像学检查还可发现门静脉或肝静脉癌栓、胆管癌栓、肝门或腹主动脉旁淋巴结转移、远处器官(肺、骨、肾上腺、脑)转移等。
PET-CT对肿瘤分期、治疗方案的选择、预后估计、治疗后随访有较大优势。对肝病患者移植前评估和移植后随访也有重要意义。但由于存在比较高的假阳性率(如炎症)及假阴性率(如高分化肝癌),需要谨慎判断PET-CT的结果。 18 FDG和 11 C-Acetata双显影可明显提高肿瘤诊断和分期的准确性。
2.血清学检查
AFP作为传统的肝癌标志物,可用于肝癌诊断的补充,特别有助于那些缺乏CT或MRI肝癌特征性改变的肝脏结节的鉴别诊断。尽管AFP具有一定的假阳性,但对于AFP值超过400μg/ml的患者,在排除继发性肝癌、生殖腺肿瘤或活动性肝病情况下,对肝癌的诊断具有重要价值。肝癌根治术后定期复查AFP亦是判断肝癌治疗效果及监测是否复发的重要指标之一。
其他肝癌标志物的检测:鉴于AFP的阳性率和特异性有限,其他肝癌标志物的研究有重要的临床意义。目前比较常用的是异常凝血酶原(PIVKA-II),诊断肝癌有较高的敏感性和特异性,且AFP阴性的肝癌患者也可阳性,因此,可联合用于肝癌的诊断。
乙肝、丙肝病毒标志物应常规检查。CEA、CA19-9检查有助于排查其他消化道肿瘤。
3.肝穿刺活检
通过病史及影像学检查一般可以做出肝癌的临床诊断,对于可进行根治性治疗的患者,不必进行肝穿刺活检。但对于CT或MRI表现不具有肝癌特征的结节,可进行肝穿刺活检进行确诊。由于肝穿刺活检有2%~3%患者可发生针道种植,且肝穿刺活检有30%患者有假阴性,需慎重确定肝穿刺活检的指征及判断结果。
根据美国肝病研究协会(AASLD)指南,有肝硬化背景的患者,肝脏内新发生的结节直径大于1.0cm,CT或MRI检查具有肝癌特征性改变(即动脉期快速增强,静脉期造影剂消退)的患者即可诊断为肝细胞癌;对于直径小于1.0cm的结节,指南建议每3个月1次的密切随访,如果结节增大超过1.0cm,则可用上述方法确定肝癌的诊断。
肝癌的早期诊断依赖于肝癌高危人群的筛查。有慢性乙型、丙型肝炎或任何原因的肝硬化患者,应该每年进行2次超声及AFP的检查,发现甲胎蛋白升高或肝脏占位性病变者,应进一步进行CT或MRI检查,以明确诊断。
【鉴别诊断】
原发性肝癌有时需与下列疾病相鉴别。
(一)继发性肝癌
继发性肝癌大多为多发性结节,影像学上多无肝硬化的表现。血清AFP多呈阴性,但其他血清标志物如癌胚抗原、糖类抗原CA19-9可阳性。胸腹部CT、胃镜、肠镜等检查可能发现原发癌。必要时可应用PET-CT发现原发癌。肝穿刺活检有助于鉴别原发性肝癌和继发性肝癌。
(二)肝硬化、慢性肝炎
需要鉴别的主要有两种情况:一是AFP升高。慢性肝炎活动可引起AFP升高,但多伴有血清转氨酶升高,随着肝炎活动的恢复,转氨酶恢复正常,AFP可逐渐下降,并恢复正常;而肝癌引起的AFP升高,血清AFP水平会逐步升高,不随肝功能的恢复而下降。通过同期检测AFP和肝功能多可鉴别。二是肝硬化结节。肝硬化结节有时和小肝癌难以鉴别,如超声检查可表现肝内低回声结节或高回声结节;CT表现为低密度占位。但通过增强CT或MRI,以及超声造影,根据结节的血供情况可资鉴别。
(三)肝脓肿
临床表现发热、肝区疼痛和压痛明显,白细胞总数及中性粒细胞增高,超声检查常可发现脓肿的液性暗区,四周多有较厚的炎症反应区,增强CT可见到肿块周边的炎症反应带。在超声导引下诊断性肝穿刺或抗菌药物试验性治疗有助于确诊。
(四)其他肝脏良恶性肿瘤或病变
如肝海绵状血管瘤、肝细胞腺瘤、炎性假瘤、局灶性结节样增生等良性病变,或邻近肝脏部位的肿瘤如胆囊癌、结肠肝曲癌、胃癌、肾上腺肿瘤等需和肝癌相鉴别。鉴别主要依赖影像学,如超声造影、增强CT或MRI检查。有时需要穿刺活检或剖腹探查方能确诊。详见肝良性肿瘤节。
【治疗】
早期发现和早期治疗是改善肝癌预后的最主要因素,而规范化的治疗是获得最佳治疗效果的保证。对于肝癌的规范化治疗,国际上有BCLC指南(同AASLD指南)、日本的J-HCC指南、亚洲肝癌诊治共识等。2011年在国家卫生计生委的指导下,我国也制定了肝癌诊治规范。
总体而言,根据肿瘤肿瘤的分期确定治疗方案。早期肝癌一般采用根治性的治疗方法,如手术切除、局部消融等;中、晚期的肝癌多采用肝动脉栓塞化疗、系统性化疗、分子靶向治疗等,对于终末期的肝癌,则只能给予支持和对症治疗。
(一)治疗前评估
1.肿瘤情况
依据上腹部增强CT/增强 MRI、胸部CT、放射性核素骨扫描、头颅CT、PET-CT。根据肿瘤大小、数目、门静脉(肝静脉)侵犯、有无远处转移等情况,给予肿瘤分期。
2.肝功能状态(Child-Pugh评分)
依据总胆红素(TB)、白蛋白(A)、凝血酶原时间(PT)、有无肝性脑病及腹水。
3.全身情况
依据ECOG评分。
4.有无系统性合并症
如心、肺功能;糖尿病等:血、尿、粪常规、肾功能、糖化血红蛋白、心电图,超声心动图、肺功能等。
(二)治疗方案
根据肝癌治疗指南和共识决定治疗方案。
1.外科手术治疗
肝癌的外科治疗包括肝切除术和肝移植。
肝切除是传统的根治性治疗方法,根治性切除后5年生存率在50%以上,目前仍为肝癌的首选治疗。手术切除的指征主要根据:①肿瘤的累及范围;②肝功能状态;③全身状况。在我国,肝癌切除术主要适用于肿瘤局限于一个肝叶或虽然位于多个肝叶,但可以完整切除者。一般认为,若肿瘤单个,或肿瘤多发,数目不超过3个,外科切除为首选;若肝癌超过3个,或合并门静脉癌栓者多选择非手术治疗,但如果系分支癌栓,且肿瘤可完全切除者,也可选择手术切除。而西方国家手术切除多为肿瘤单个(肿瘤大小不限)或符合 Milan标准(即单个结节,直径≤5cm或2~3结节,直径均≤3cm)。且无门静脉癌栓及远处转移。肝功能状态是决定患者能否接受手术切除的重要因素,一般为Child-Pugh A或B的肝癌患者,吲哚菁绿试验(ICG)对于判断肝脏的储备功能,确定手术指征很有帮助。
肝移植治疗肝癌除了可完全切除肝癌外,还可治疗肝癌合并的肝硬化,特别适用于合并严重肝硬化的早期肝癌,治疗小肝癌可获得较好的效果。但是,由于肝癌容易发生肝内和远处转移,移植术后应用免疫抑制剂,如适应证选择不严格,术后容易复发。因此肝移植治疗肝癌应该严格掌握适应证。西方国家多采用Milan标准或UCSF标准(单个肿瘤直径≤6.5cm,或多发肿瘤数目≤3个且每个肿瘤直径均≤4.5cm、所有肿瘤直径总和≤8cm)。
肝癌切除术后,复发率较高,术后5年累计复发率可达61.5%~79.9%。故应该密切随访肿瘤标志物、超声、CT或 MRI等,以便能够早期发现复发,及时治疗。肝癌术后复发超过80%发生在肝内,如能及时发现,再手术切除后5年生存率仍可达38.7%。射频毁损治疗或瘤内无水酒精注射治疗术后复发的小肝癌也可获得较好的效果。
2.肝动脉栓塞化疗(TACE)
AASLD指南认为TACE是无血管侵犯和肝外转移的多发肿瘤(BCLC B期)的有效治疗。对于TACE是否能使BCLC C期患者获益,目前仍有争议,缺乏有效循证医学证据。传统的方法是在局部应用化疗药物的基础上,给予碘化油(lipoidol)或明胶海绵(gelfoam)进行肝动脉栓塞。近年来,有采用药物缓释微球或放射性 90 铱微球进行肝动脉栓塞化(放)疗。随机对照研究和荟萃分析结果显示,对于Child-Pugh A级或B级的患者,与支持治疗或全身化疗作对照,肝动脉栓塞化疗均能显著地延长肝癌患者的生存期,从而肯定了肝动脉栓塞化疗的疗效。TACE最主要的并发症是肝衰竭,故应强调术中超选择肿瘤血管,以利肿瘤控制和肝功能保护。其他严重并发症包括上消化道出血、溶瘤综合征、异位栓塞、胆汁瘤继发胆道感染、血管损伤假性动脉瘤形成等。
3.局部频消融
包括射频(radiofrequency ablation)、微波(microwave ablation)、激光(laser ablation)及经皮无水酒精注射(percutaneous ethanol injection)。超过90%的患者可以在超声(或CT)引导下经皮穿刺消融,少数影像学显示不清楚或突出肝包膜的肝癌可在开腹和腹腔镜下消融。射频和微波的适应证为肿瘤直径≤5cm的单发肿瘤或直径≤3cm的3个以内多发结节,无血管、胆管侵犯或远处转移且Child-Pugh A~B级。单发肿瘤直径≤3cm可获得根治性消融。无水酒精对于单发肿瘤≤2cm可取得类似于射频消融的疗效。
4.放疗
放射治疗主要适用于肝门区肝癌的局部放射治疗,也可用于门静脉癌栓、下腔静脉癌栓、肝门淋巴结或腹腔淋巴结转移、远处转移病灶的姑息性治疗。近年来采用立体定向放射治疗可使局部的放射剂量得以增加,减轻了不良反应,提高了疗效。更有采用计算机断层技术与放射治疗结合的断层放射治疗(TOMO)治疗肝癌,使放射治疗应用更为广泛。适应证为肿瘤局限但位于重要解剖部位无法进行手术者,肿瘤压迫致胆道梗阻,胆道、门静脉或下腔癌栓,远处转移灶(淋巴结、肺、肾上腺、骨)。急性毒不良反应包括胃肠道反应、严重肝功能损害、骨髓抑制、放射性胃肠炎和肺炎,严重的放射后期损伤为放射诱导肝病(RILD)。严重肝功能失代偿(Child C级)或全身情况差(KPS评分<50分)不宜放疗。放疗过程中应定期随访肝肾功能及血常规。
5.分子靶向治疗
分子靶向药物主要针对肿瘤发生和发展中的驱动基因,特异性的抑制肿瘤的生长。但迄今为止,尚未能明确肝癌增殖的驱动基因。目前主要应用针对肝癌新生血管形成、抑制肝癌增殖的分子靶向药物如索拉非尼。索拉非尼是有充分循证医学证据而证实能够延长肝癌生存的药物,主要用于有远期转移,或合并门静脉癌栓的晚期肝癌患者,也可联合TACE用于中期肝癌的治疗。
6.其他治疗
肝癌多发生在乙型肝炎的基础上,在手术切除或抗肿瘤治疗同时应该注意监测乙肝病毒DNA载量的变化。如果治疗前或治疗过程发现有乙肝病毒复制,应及时给予核苷类抗乙肝病毒药物治疗。随机对照研究结果显示,如在肝癌切除术后大剂量应用α-干扰素有降低术后复发率的作用。也有研究提示与化疗合用,可提高化疗的缓解率。对于中晚期的肝癌患者,中药可以缓解症状、延长生存。此外,淋巴因子诱导的杀伤细胞—CIK细胞、肿瘤浸润淋巴细胞(TIL)等过继细胞免疫治疗在肝癌切除术后应用,可降低术后的复发率。应掌握适应证应用。
(三)治疗后评估
1.肿瘤情况
①肝癌切除术后,通常需要在1个月行肿瘤标志物、超声等检查。对于复发高危的患者,如有大肝癌、有子灶、或病理发现有血管侵犯,可在术后1~2个月给予辅助性的肝动脉栓塞化疗,能有效发现残留微小病灶并给予早期治疗;②TACE后1个月复查CT平扫(LipCT)评估碘油沉积情况,或增强MRI或超声造影可评估肿瘤存活情况,决定后续治疗方案;③消融治疗后1个月复查增强CT或增强MRI或超声造影,评估消融彻底性,消融不全,或符合适应证的新发灶可重复消融。对于消融彻底的患者,应定期随访超声或 MRI,以便早期发现复发,及时治疗;④随访肿瘤标志物如甲胎蛋白或异常凝血酶原,如术后未降至正常,则提示有残留癌的可能。
2.肝功能状态(Child-Pugh评分)及其他
治疗后再次Child-Pugh评分。TACE及放疗后应随访血常规,观察骨髓抑制情况。随访HBV-DNA和HCV-RNA观察有无免疫抑制引起的病毒复燃。
3.全身情况和并发症评估
重新ECOG评分。
【预后】
由于肝癌大多合并有肝硬化,因此,肝癌患者的预后主要和肝癌的累及范围以及基础疾病(肝硬化)有关。因此,我国的肝癌分期以及巴塞罗那肝癌分期将肝功能的状态作为分期的主要因素之一,对于肝功能为Child-Pugh C级的肝癌,即便是小肝癌,其预后也很差。
早期肝癌能够获得根治性治疗(肝脏移植、手术切除、局部消融)的机会,术后5年生存率在40%~70%之间。肿瘤大小、肿瘤结节的数目、有无血管侵犯与手术后的复发率有显著关系。肝癌结节有血管侵犯,结节周围有子灶,或者多发癌结节的患者术后复发率高。
【预防】
预防HBV和HCV感染是防治肝癌最有效的措施。乙肝疫苗的计划免疫将会显著降低乙肝病毒相关的肝癌发病率。预防HCV的主要措施是切断传染途径,包括血源的管理、使用一次性注射器具、外科器械的彻底消毒等。有效的抗病毒治疗如干扰素及核苷类抗乙肝病毒药物可减少肝炎后肝硬化的发生,以及降低肝癌的发生率。
二、继发性肝癌
任正刚 陈荣新
继发性肝癌指全身其他部位的恶性肿瘤,通过血液转移至肝脏,或邻近器官肿瘤直接侵犯肝脏,在肝脏形成单发或多个病灶,以腹部内脏癌肿如结直肠癌、胃癌、胰胆管癌、肾癌、卵巢癌多见;腹部外脏器如乳腺、肺、鼻咽等部位癌肿也可转移至肝脏;此外,胆囊(管)、胃、肾上腺与肝脏毗邻,癌症容易直接侵犯肝脏,形成浸润转移。
【临床表现】
大多数患者有原发癌肿引起的症状,而肝脏本身的症状并不明显。也有部分患者以肝区疼痛、上腹肿块,甚至黄疸、腹水等继发性肝癌的症状起病。少部分患者原发病灶来源不明。
【诊断】
多依据影像学表现诊断。继发性肝癌影像学表现为多发性结节,大多无肝硬化。典型表现为“牛眼征”,即病灶周边有晕环,中央乏血供而呈低密度。血清肿瘤标志物有助于继发性肝癌诊断,甲胎蛋白(AFP)多为阴性,部分胃肠道癌、生殖腺癌肿肝转移可伴AFP升高。诊断关键在于明确原发病灶。大多数患者有原发癌肿的病史。首次发现继发性肝癌患者通过影像学和内镜检查多可以查明原发病灶;对原发灶不明者,可行PET-CT全身扫描检查,提供原发病灶线索。
大多数患者根据肝外原发性癌肿的病史结合肿瘤标志物、典型的影像学特征可做出诊断。诊断不明的患者,肝肿瘤组织病理活检及免疫组化结果,有助于发现原发癌肿的来源。
【治疗】
如仅为孤立的转移灶或者多发转移结节局限于肝脏一叶,原发癌灶又可切除者,可与原发性癌肿同期或二期手术切除。如原发灶切除后出现肝转移的患者,局部病灶符合切除条件,无其他部位转移,首选手术切除。继发性肝癌患者肝脏一般无基础疾病,可耐受较大范围肝切除。肝切除后剩余肝脏体积不足的患者,术前门静脉栓塞(PVE),使剩余肝叶代偿性增生,使原先无法耐受肝切除患者能接受手术切除,或者采用联合肝实质分割和门静脉分支结扎的分阶段肝切除术。手术无法切除的局限性肝转移灶(病灶<3cm,数目≤3),可行局部消融治疗。
手术无法切除,不能局部消融治疗的患者,根据患者情况及原发癌的病理性质,选用全身化疗、分子靶向治疗、经肝动脉介入治疗、放疗等治疗。部分患者肝转移灶经过“转化治疗”,可再次切除。
【预后】
出现肝转移,提示原发病灶的扩散,预后不佳。但是随着医学技术的发展,尤其是外科技术进步、局部消融、新的化疗药物、靶向治疗、多学科诊治出现,继发性肝癌患者预后较以前已大为改善。
三、肝脏其他恶性肿瘤
任正刚 纪元
(一)肝母细胞瘤
肝母细胞瘤(hepatoblastoma)是儿童最常见的肝脏恶性肿瘤,多见于5岁以下的儿童。肝母细胞瘤是胚胎源恶性肿瘤,主要有两种组织类型,即上皮型和混合型(上皮与间质混合型)。肝母细胞瘤诊断主要依据影像学,如CT或MRI。多数患儿血清甲胎蛋白升高,有利于诊断和判断预后。
肝母细胞瘤如病灶局限,手术切除可获得较好的疗效。不能切除的可给予系统化疗或肝动脉栓塞化疗。肝母细胞瘤多数对化疗敏感,常用药物如顺铂、5-氟尿嘧啶等。部分不能切除的肝母细胞瘤化疗后缩小转化为可手术切除。
(二)肝肉瘤
原发性肝肉瘤(primary sarcomas of the liver)很少见,好发于男性,多见于儿童和老年人。儿童发病可能与先天性或胚胎性结缔组织异常发育有关。约1/3的成人患者可并发肝硬化。病理类型以内皮细胞来源为多,其他尚有平滑肌肉瘤、脂肪肉瘤或淋巴瘤。
本病与血清甲胎蛋白阴性的原发性肝癌仅能从组织学检查上做出鉴别。临床症状有发热和腹块,病程发展急剧。
原发性肝肉瘤对化疗不敏感。如病灶局限,可能获根治者宜首选手术切除,可或满意的效果。如病灶直径在3cm以下,也可考虑行局部消融治疗。
1.肝上皮样血管内皮瘤(epithelioid haemangioendothelioma,EHE)
是由上皮样或梭形细胞沿既有脉管生长或形成的恶性肿瘤。临床表现无特征性,约40%病例是偶然发现的。EHE是缓慢生长的恶性肿瘤,预后明显好于血管肉瘤,手术切除或肝移植后可生存5~28年,部分EHE患者肝切除后行化疗或放疗后有一定治疗效果,但因肿瘤自身的病程长,不能确定各种治疗的确切效果。在未治疗的病例中,54%生存超过2年。
2.肝血管肉瘤(angiosarcoma)
为一种高度恶性的肿瘤,起源于血管或淋巴管内皮细胞的恶性肿瘤。较少见。多为先天性,常见于婴儿,偶见于老年人。曾有报道认为此病与曾用造影剂二氧化钍(thorium dioxide)、雄性激素、避孕药、或摄入砷有关。近来还认为与氯乙烯(vinyl chloride)有关。临床表现为腹痛、乏力、体重下降及腹部包块等。患者肝脏可迅速增大,并伴腹胀、腹痛、厌食和贫血,肝区可听到血管杂音。肿瘤破裂是常见的并发症,部分患者还可发生弥散性血管内凝血(DIC)。肿瘤破裂时有血腹。病理可见肝脏有大小不等充血的血窦,并衬有大小不等核深染的内皮细胞,腔内可见血栓形成,免疫组织化学显示血管内皮标志物CD34、CD31阳性。肝脏血管肉瘤预后差,多数患者在6个月内死亡。病灶局限者,可考虑手术切除。不能手术切除的患者,也可应用系统化疗或肝动脉栓塞化疗,但疗效不确定。
四、肝脏良性肿瘤
任正刚 纪元
(一)肝血管瘤
大多数属海绵状血管瘤(cavernous hemangioma),是一种常见的肝脏良性肿瘤,可发生于任何年龄,女性较多。肿瘤见于肝脏任何部位,常位于包膜下,多为单发(约10%为多发),肿瘤直径多小于4cm,大者至30cm。肿瘤表面呈暗红或紫色,外有包膜,切面海绵状。显微镜下血管瘤是一内壁为扁平内皮细胞的血管管道构成交通的空隙网,其中含红细胞,有时可见新鲜的机化血栓。肿瘤与周围组织分界清楚。
临床表现:<4cm者多无症状,常于腹部超声时偶然发现;4cm以上者约40%伴腹部不适,肝大,食欲缺乏、消化不良等症状。肝血管瘤内可能反复血栓形成,造成肿瘤肿胀,牵拉胀痛。肿块软硬不一,有不同程度的可压缩感,少数呈坚硬结节感。肿块很少自发破裂。肝功能一般正常,过大的血管瘤罕见的综合征为消耗性凝血障碍、血小板减少及低纤维蛋白血症。多种影像学检查可助诊断,超声波显像呈典型的边缘清晰的回声增强区,可见管道通入。大血管瘤可见网状回声不均,有时见钙化。CT造影剂增强或延迟扫描呈先有肿瘤周边过度增强,逐渐向中心填充呈等密度的典型表现。MRI在SET1加权像上,瘤灶示边界清楚的类圆形低信号区,T2加权像上瘤灶信号显著增强且均匀升高,瘤/肝信号强度比明显增加。核素血池扫描呈明显填充现象。在诊断和鉴别诊断有困难者,可考虑剖腹探查,针刺活检常可导致严重出血故属禁忌。
肝海绵状血管瘤多数不需要治疗。但需定期随访。体积较大有明显临床症状的血管瘤,特别是伴有消耗性凝血障碍者应手术切除,如病变广泛不能切除者可予肝动脉结扎术或栓塞治疗。
(二)肝腺瘤(adenoma of liver)
是极罕见的一种良性肿瘤,按细胞来源可区分为肝细胞性、胆管细胞性两种。胆管腺瘤(cholangioadenoma)又可分为管状腺瘤和囊腺瘤两种。后者少见,常为多房性。胆管腺瘤可以单个或多个。直径大小不等。外观可与正常肝组织的色泽相似,外有包膜,肉眼有时不易与肝癌区别。
肝细胞腺瘤(hepatocellular adenoma)是一种非常罕见的良性肿瘤,多见于中年女性,发病年龄多在20~39岁间。发病机制不明,多数有长期口服避孕药史。研究表明,性激素仅起促进作用。5%~10%系偶然发现,25%~35%因腹块,20%~25%有慢性或轻度发作性腹痛,30%~40%为急腹痛。其中30%系肿瘤内出血,70%为腹腔内出血。腹腔内出血是最严重的并发症,须急诊手术处理。
肝细胞腺瘤多为孤立结节,肿瘤呈球形向肝表面膨出,检出时肿瘤直径常为5~15cm,常有大血管横跨于肿瘤表面。切面可见肿瘤与周围肝组织分界清楚。色泽黄褐色到棕色,常伴坏死出血区。显微镜下,腺瘤细胞似良性肝细胞排列呈片状或索状,无腺泡状结构,细胞大小一致,核规则无分裂相。
常用的影像学方法实时超声、CT、肝动脉造影等,均可有助于定位诊断。肝胆显像剂PMT(吡哆醛-5甲基色氨酸)行肝核素扫描,腺瘤区呈强阳性填充,有助于腺瘤诊断。确诊依靠病理组织学检查。
治疗:肝腺瘤可发生危及生命的破裂内出血故应及早手术切除。持续服用避孕药者停用口服避孕药多不再发展。巨大肝腺瘤、肝腺瘤癌变或发生破裂出血时均须外科手术处理。
(三)肝脏非寄生虫性囊肿(non parasitic cysts of liver)
据尸解和剖腹手术资料,发病率为0.14%~5.3%。先天性肝囊肿如孤立性肝囊肿、多囊肝;后天性如创伤性肝囊肿等。肝囊肿多见于女性,多在40岁以后发现。孤立性肝囊肿可为单个,也可多发。而多囊肝多伴有肾或其他脏器的多囊症,约50%伴有多囊肾。囊肿大小不等,增速缓慢。肝右叶囊肿多见。既可布满肝脏,也可局限于胆小管而表现为胆小管的分段扭曲及扩张。囊内液体成分随囊肿类型、大小及有无并发症而改变。多囊肝的囊液澄清,不含胆汁;若囊内出血则囊液呈棕红色;如并发感染,囊液可呈脓性。
临床表现与囊肿大小有关,主要为消化道症状如消化不良、食欲减退、右上腹痛。有时腹痛难忍,平卧后可减轻,继发感染后出现寒战和发热。巨大囊肿压迫胆总管或肝管可致黄疸,但少见。腹部触诊可扪到肿大肝脏或富有弹性的肿块,表面不平整。肝功能多正常。合并其他脏器囊肿者有相应症状,如多囊肾有肾功能不全和高血压。
诊断主要依靠影像学检查,如超声波检查肝区可见多个液性暗区。如有多囊肾,肾区也可见液性暗区。CT示明显低密度区,造影剂无填充。肝囊肿需要和囊肿的癌变或囊腺癌鉴别,CT或MRI显示内部不规则的实质性改变,动脉相有增强,血清CEA或CA19-9升高。穿刺活检的阳性率不高,怀疑或不能排除癌变者可手术切除。
体积较小的肝囊肿无须治疗。对于巨大有压迫症状的肝囊肿,需行开窗术治疗。
(四)肝局灶结节性增生(hepatic focal nodular hyperplasia,FNH)
是少见的肝脏良性肿瘤之一。常为单发,多见于青壮年,45岁以下占80%。70%患者无症状,85%患者无肝炎背景。84.6%患者彩超可以见到特征性的粗大的中央血管,血流流速快,阻力系数低。CT动态扫描75%患者呈现动脉早期增强,50%强化均匀,部分有中央星状瘢痕。75%静脉相等密度。MRI示83.3%增强后早期明显强化,66.7%信号均一。92.9%病灶小于5cm、无包膜,病灶中央见星状纤维瘢痕并向四周放射将病灶分成大小不等的结节。
FNH系良性病变,无恶变的倾向,也很少发生出血,可长期随访观察。FNH需要和HCC以及肝腺瘤进行鉴别,鉴别依赖于影像学检查,必要时可做肝穿刺活检鉴别。
(五)炎性假瘤
发生于任何年龄,患者一般情况好或症状轻微,无肝硬化史,AFP阴性。实时超声示质地均匀、低回声区,CT显示为质地不太均匀、边界清楚的低密度区。手术时肝质地柔软,肿瘤边界清晰,剖面平滑,黄色。病理为多种细胞组成的炎性肉芽肿。炎性假瘤发生癌变的可能性也须注意。
(六)肝硬化再生结节
肝硬化多伴有肝内再生结节。再生结节CT呈低密度区,增强亦无强化,如和肝细胞癌鉴别困难,MRI检查,多可做出鉴别诊断。值得注意的是,有报道肝再生结节长期随访发生癌变,因此需要密切随访。鉴别困难者,可行针刺活检明确诊断。
(七)肝间叶性错构瘤
肝脏发育畸形所形成的肿瘤样肿物,婴幼儿多见。实时超声显示中央有回声增强的光带分隔,内伴有大小不等的囊性暗区或低回声区。应尽可能予以切除。
主要参考文献
1.Forner A,Llovet JM,Bruix J.Hepatocellular carcinoma.Lancet,2012,379(9822):1245-1255.
2.Yang JD,Roberts LR.Hepatocellular carcinoma:A global view.Nat Rev Gastroenterol Hepatol,2010,7(8):448-458.
3.Kremer N,Walther AE,Tiao GM.Management of hepatoblastoma:an update.Curr Opin Pediatr,2014,26(3):362-369.
4.McInnes MD,Hibbert RM,Inácio JR,et al.Focal nodular hyperplasia and hepatocellular adenoma:accuracy of gadoxetic acid-enhanced MR imaging-A systematic review.Radiology,2015,277(2):413-423.
第九节
肝衰竭

李 蕾
肝衰竭(liver failure)是多种因素引起的严重肝脏损害,导致其合成、解毒、排泄和生物转化等功能发生严重障碍或失代偿,出现以凝血功能障碍、黄疸、肝性脑病、腹水等为主要表现的一组临床症候群。我国2012年《肝衰竭诊疗指南》根据病理组织学特征和病情发展速度,将肝衰竭分为急性、亚急性、慢加急性、慢性4类。我国目前临床上以慢加急性肝衰竭为主,疾病进展快,病死率较高。
【病因】
在我国,引起肝衰竭的首要病因是肝炎病毒(主要是乙型肝炎病毒)、其次是药物及肝毒性物质(如乙醇、化学制剂等)。在欧美国家,药物是引起急性、亚急性肝衰竭的主要原因;酒精性肝损害常引起慢性或慢加急性肝衰竭。儿童肝衰竭还可见于遗传代谢性疾病(表15-8-14)。
表15-8-14 肝衰竭的病因

【病理】
目前,肝衰竭的病因、分类、分期与肝组织学改变的关联性尚未取得共识。以HBV感染所致肝衰竭为例,各类肝衰竭典型病理表现为:急性肝衰竭肝细胞一次性坏死,坏死面积≥肝实质的2/3为大块坏死;或亚大块坏死(1/3~2/3肝实质),肝窦网状支架不塌陷或非完全塌陷。亚急性肝衰竭肝组织呈新旧不等的亚大块坏死或桥接坏死;较陈旧的坏死区网状纤维塌陷,或有胶原纤维沉积;残留肝细胞有程度不等的再生,并可见细小胆管增生和胆汁淤积。慢加急性肝衰竭在慢性肝病病理损害的基础上,病因不同,形态学表现不一,HBV相关ACLF的病理表现为肝硬化/肝纤维化基础上沿中央静脉分布的亚大块肝实质坏死(坏死面积15%~90%),酒精性ACLF以严重的炎症和肝细胞变性为特征。此外严重的淤胆、卵圆细胞来源的肝再生以及病理上表现的脓毒血症均是所有慢加急肝衰竭病理共有的特征。而慢性肝衰竭主要为弥漫性肝脏纤维化以及异常结节形成,可伴有分布不均的肝细胞坏死。
【发病机制】
肝衰竭的发病机制十分复杂,受多种因素影响,具体机制目前尚未完全明确,主要包括以下两个方面。
(一)各种因素对肝细胞的直接损伤
各型肝炎病毒都可引起肝衰竭,这些病毒的致病性与其数量、毒力、变异有关。大量临床研究发现肝炎病毒感染,特别是肝炎病毒的重叠感染或混合感染和变异株的感染与肝衰竭的发生密切相关。
(二)免疫损伤机制
1.固有免疫系统功能紊乱
固有免疫在急性、亚急性和慢加急性肝衰竭的发生发展过程中发挥着主要作用。固有免疫系统受到病原刺激,可产生一种非病原特异性的炎症反应,其主要效应细胞是吞噬细胞如巨噬细胞、中性粒细胞和单核细胞,在肝内则为Kupffer细胞。肝衰竭发生过程中,Kupffer细胞的功能紊乱可能发挥了重要作用。
2.细胞因子的作用
细胞因子由活化的免疫细胞和某些基质细胞分泌,可介导和调节免疫。一些促炎因子(如IL-1、IL-6、IL-17、IL-18、TNF-α)和抑炎因子(如IL-4、IL-10、IL-13)的失衡与肝衰竭发生时免疫功能的紊乱有直接关系。细胞因子参与肝衰竭的发生机制主要包括以下两种:①参与肝衰竭、肝细胞坏死发生过程;②参与构成抑制肝细胞再生的细胞外环境,导致肝衰竭时肝细胞再生障碍。
3.微循环障碍与门静脉高压
肝衰竭时内毒素作用于肝窦内皮细胞及微血管,引起肝微循环障碍;肝衰竭患者往往会表现为更严重的高动力循环状态,心输出量增加,周围循环充血且低应答,平均动脉压下降,内脏血管充血,门静脉高压,甚至导致肾灌注不足。肝脏微循环障碍及门静脉高压,使肝细胞营养供应不足,药物难以进入肝脏发挥作用,代谢废物难以排出,从而进一步加重肝细胞损伤,损伤的肝脏进一步释放血管活性物质和各种细胞因子,形成恶性循环,导致肝脏进行性损伤,启动多器官功能衰竭甚至危及生命。
【肝衰竭分类和诊断】
(一)分类
肝衰竭分为四类:急性肝衰竭(acute liver failure,ALF)、亚急性肝衰竭(subacute liver failure,SALF)、慢加急性(亚急性)肝衰竭(acute-on-chronic liver failure,ACLF)和慢性肝衰竭(chronic liver failure,CLF)。
(二)临床诊断
1.急性肝衰竭
急性起病,2周内出现Ⅱ度以上肝性脑病并有以下表现者:①极度乏力,有明显厌食、腹胀、恶心、呕吐等消化道症状;②短期内黄疸进行性加深;③出血倾向明显,血浆凝血酶原活动度(prothrombin activity,PTA)≤40%[或国际标准化比值(INR)≥1.5],且排除其他原因;④肝脏进行性缩小。
2.亚急性肝衰竭
起病较急,2~26周出现以下表现者:①极度乏力,有明显的消化道症状;②黄疸迅速加深,血清总胆红素大于正常值上限10倍或每日上升≥17.1μmol/L);③伴或不伴有肝性脑病;④出血倾向明显,PTA≤40%(或INR≥1.5)并排除其他原因者。
3.慢加急性(亚急性)肝衰竭
东西方诊断上存在差异。西方以酒精性(西方型)为主,因此几乎所有的西方型ACLF均发生在肝硬化基础上。而东方型ACLF以HBV为代表,可以发生在肝硬化或非肝硬化基础上。
西方型ACLF的诊断标准按照CLIF-OF标准(表15-8-15),以多脏器衰竭的数量作为评判依据。
表15-8-15 CLIF-C OFs评分
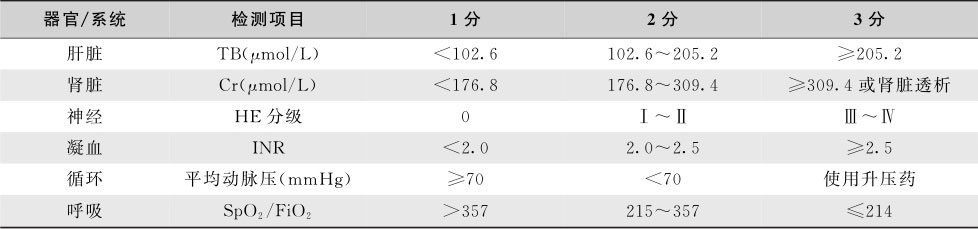
上述六大脏器中出现以下任何一种情况均诊断为ACLF:①单独肾衰竭;②一个脏器衰竭合并肾或神经系统损伤;③两个或以上脏器衰竭。其中达到肾衰竭的评分为2分,其余五个脏器衰竭需达到3分。
东方型ACLF诊断根据亚太肝病协会共识意见来进行诊断:
慢性肝病基础上,短期内发生急性或亚急性肝功能失代偿的临床症候群,表现为:①极度乏力,有明显的消化道症状;②黄疸迅速加深,血清总胆红素大于正常值上限10倍或每日上升≥17.1μmol/L);③出血倾向明显,PTA≤40%(或INR≥1.5)并排除其他原因者;④失代偿性腹水;⑤伴或不伴肝性脑病。
东西方定义和诊断标准主要差异如下:①包含的器官不同。东方诊断标准侧重于肝衰竭的表现,而西方诊断标准强调多器官功能衰竭;②肝衰竭的诊断标准不同。东方诊断标准侧重于早期,INR≥1.5,有或无肝性脑病,而西方对凝血和神经系统衰竭的诊断标准分别是INR≥2.5,肝性脑病Ⅲ/Ⅳ期,侧重于病情晚期。
4.慢性肝衰竭
在肝硬化基础上,肝功能进行性减退和失代偿:①血清总胆红素明显升高;②白蛋白明显降低;③出血倾向明显,PTA≤40%(或INR≥1.5)并排除其他原因者;④有腹水或门静脉高压等表现;⑤肝性脑病。
(三)分期
根据临床表现的严重程度,亚急性肝衰竭和慢加急性(亚急性)肝衰竭可分为早期、中期和晚期。
1.早期
①极度乏力,并有明显厌食、呕吐和腹胀等消化道症状;②黄疸进行性加深(血清总胆红素≥171μmol/L或每日上升≥17.1μmol/L);③有出血倾向,30%<PTA≤40%(或1.5<INR≤1.9);④未出现肝性脑病或其他并发症。
2.中期
在肝衰竭早期表现基础上,病情进一步发展,出现以下两条之一者:①出现Ⅱ度以下肝性脑病和(或)明显腹水、感染;②出血倾向明显(出血点或瘀斑),20%<PTA≤30%(或1.9<INR≤2.6)。
3.晚期
在肝衰竭中期表现基础上,病情进一步加重,有严重出血倾向(注射部位瘀斑等),PTA≤20%(或INR≥2.6),并出现以下四条之一者:肝肾综合征、上消化道大出血、严重感染、Ⅱ度以上肝性脑病。
(四)肝衰竭诊断格式
肝衰竭不是一个独立的临床疾病,而是一种功能性诊断。在临床实际应用中,完整的诊断应包括病因、临床类型及分期。例如:病毒性肝炎,慢性,乙型,慢加急性肝衰竭(早期)。
【实验室检查】
1.血清胆红素测定
常呈进行性增高,多超过171μmol/L,最高可达800μmol/L以上。
2.血清转氨酶
血清丙氨酸氨基转移酶(ALT)及天门冬氨酸氨基转移酶(AST)常明显升高,尤以后者升高明显。AST/ALT比值对估计预后有意义,存活者比值介于0.31~0.63之间,死亡者多在1.20~2.26之间。肝衰竭时,由于肝细胞大量坏死,ALT及AST活性反而迅速下降。与此形成对比的是,血清胆红素显著升高,此现象称为“胆酶分离”现象,对肝衰竭的诊断及预后意义重要。
3.血清胆固醇与胆固醇酯
胆固醇与胆固醇酯主要在肝细胞内合成。如低于2.6mmol/L则提示预后不良,ALF时胆固醇脂也常明显下降。
4.血清胆碱酯酶活力
胆碱酯酶有两种,乙酰胆碱酯酶和丁酰胆碱酯酶。后者在肝细胞内合成,肝衰竭时此酶活力常明显下降。
5.血清白蛋白
最初可在正常范围内,如白蛋白逐渐下降则预后不良。但这种变化的敏感度不高,主要系因白蛋白的半衰期可达3周,其合成明显降低需2~3周才逐渐显现。
6.凝血功能检查
(1)凝血酶原时间(PT):
凝血因子Ⅰ、Ⅱ、Ⅴ、Ⅶ、Ⅹ中任何一种缺乏均可致PT延长。PT的表示方法有三种:①PT延长的秒数,比对照值延长3秒为异常;②国际标准化比值(INR),>1.2为异常;③PTA,由PT计算而来。凝血酶原时间测定是目前最常用的估价肝细胞功能指标之一,但需排除维生素K缺乏所致的PT延长。
(2)活化部分凝血活酶时间(APTT):
参与内源性凝血系统的任何因子缺乏时均可致APTT延长。APTT延长首先提示因子Ⅷ、Ⅸ、Ⅺ、Ⅻ缺乏,但也提示Ⅰ、Ⅱ、Ⅴ、Ⅹ因子缺乏。肝衰竭时APTT延长较为常见。
(3)纤维蛋白原定量:
由于肝细胞合成能力降低及并发DIC等原因,可出现血浆纤维蛋白原含量降低。
(4)凝血因子测定:
Ⅱ、Ⅴ、Ⅶ、Ⅸ、Ⅹ等因子明显减少。
7.其他检查
肝炎病毒标志物及其他病毒抗体的检查有助于病因的诊断。血氨、血浆氨基酸测定有助于肝性脑病的诊断及处理。细菌学检查及鲎试验有利于确定感染的存在。电解质检查对监测患者病情极为重要。
8.其他脏器功能衰竭指标
参见表15-8-15。
【肝衰竭的治疗】
(一)病因治疗
所有的肝衰竭患者应明确病因,并给予必要的病因特异性治疗,包括发病原因及诱因。针对单一病因ALF的特异治疗手段很少,例如以N-乙酰半胱胺酸(NAC)治疗对乙酰氨基酚过量引起的ALF,立即分娩以治疗妊娠相关的ALF。其他虽在使用但未被证明有效的治疗措施包括:应用活性炭和静脉应用大剂量青霉素治疗蘑菇中毒;应用糖皮质激素治疗自身免疫性肝炎;应用铜螯合剂、血浆去除术和抗氧化剂治疗Wilson病;对HBV DNA阳性的肝衰竭患者,不论其检测出的HBV DNA滴度高低,建议立即使用核苷(酸)类药物抗病毒治疗;应用血流动力学支持疗法治疗休克或缺血引起的肝损伤;应用外科减压手术或经颈静脉肝内门体分流术治疗急性Budd-Chiari综合征。
(二)内科综合治疗
1.支持治疗
(1)卧床休息。
(2)加强病情监测:应加强多学科协作综合治疗,并进行凝血功能、血氨及血液生物化学指标的监测,床边B超监测肝脏大小及腹水变化。
(3)推荐肠道内营养,供给足够热量,饮食以高碳水化合物、低动物蛋白、低脂肪为宜。每日总热量成人应在35~50kcal/kg。入液量应控制在2000ml左右,并补充足量的维生素B、维生素C、维生素K等。临床上多给10%~20%葡萄糖,同时配给支链氨基酸。
(4)积极纠正低蛋白血症,补充白蛋白或新鲜血浆,并酌情补充凝血因子。
(5)纠正电解质、酸碱平衡:定期随访血气及电解质检查,及时发现,及时纠正。
(6)保持室内空气流动,注意消毒隔离,加强口腔护理及肠道管理,预防医院内感染发生。
2.其他治疗
(1)免疫调节治疗:
目前对于肾上腺皮质激素在肝衰竭治疗中的应用尚存在不同意见。非病毒感染性肝衰竭,如自身免疫性肝病及急性乙醇中毒(严重酒精性肝炎)等是其适应证。其他原因所致的肝衰竭早期,若病情发展迅速且无严重感染、出血等并发症者,可酌情使用并及早停药。后期为调节肝衰竭患者机体的免疫功能、减少感染等并发症,可酌情使用胸腺素α1等免疫调节剂。
(2)促进肝细胞再生:
疗效不肯定,但可试用:①肝细胞生长因子及肝细胞刺激物质,有促进DNA合成,促进肝细胞再生,抑制肿瘤坏死因子,增加Kupffer细胞功能,增加肝细胞对氨基酸的摄取,增加ATP酶活性等作用。②前列腺E1,能改善组织灌流,但对已有出血的患者不能应用。③生长激素可增加肝细胞再生能力,提高巨噬细胞吞噬功能,增加肠黏膜屏障功能,可考虑使用。
(3)微生态调节治疗:
可应用肠道微生态调节剂、乳果糖等,减少肠道细菌易位或降低内毒素血症及肝性脑病发生。
3.并发症防治
(1)脑水肿治疗:
对于列入肝移植的患者应行颅内压监测;颅内高压发生后,应给予甘露醇及过度通气。但是预防性应用上述方法并无好处,不予推荐。皮质类固醇类药物不宜应用于控制ALF患者的颅内高压。
(2)肝性脑病的治疗:
详见本章第一节“肝硬化及其并发症”。
(3)抗感染治疗:
应行定期监测培养,以早期发现潜在的细菌或真菌感染,以便根据培养结果尽早采取适当治疗措施。
(4)肾功能不全处理:
密切注意肝衰竭患者的液体复苏及血管内血容量的维持。伴急性肾衰竭患者如需要透析支持,建议采用持续性而不是间歇性血液透析。
(5)出血的防治:
只有在出血和进行侵入性操作前才推荐对血小板减少症和凝血时间延长者进行补充治疗。ALF患者应接受H 2 受体阻断药或质子泵抑制剂治疗,以预防因为应激性溃疡导致的酸相关性胃肠道出血。
(三)人工肝支持系统
人工肝是指通过体外的机械、物理化学或生物装置,清除各种有害物质,补充必需物质,改善内环境,暂时替代衰竭肝脏部分功能的治疗方法,能为肝细胞再生及肝功能恢复创造条件或等待机会进行肝移植。人工肝支持系统分为非生物型、生物型和组合型三种。非生物型人工肝已在临床广泛应用并被证明确有一定疗效。生物型及组合生物型人工肝不仅具有解毒功能,而且还具备部分合成和代谢功能,是人工肝发展的方向,现正处于临床研究阶段。
(四)肝细胞和干细胞移植
利用动物或人肝细胞经微载体、球形体、微囊凝胶滴等植入系统植入人的腹腔或脾脏,以取代人的肝脏功能。在动物实验模型中已证实纯化肝脏干细胞灌注具有治疗肝衰竭潜力,但是否适用于人类尚待研究。
(五)原位肝移植
肝移植是目前治疗肝衰竭的有效手段,中长期(5年)生存率可达到70%。应掌握时机,具体指征见本章第十一节。
【预后】
肝衰竭尚缺乏敏感、可靠的临床评估指标或体系。多因素预后评价模型如序贯器官衰竭评估(sequential organ failure assessment,SOFA)、终末期肝病模型(MELD)、Child-Pugh评分等,以及单因素指标如凝血酶原时间、V因子、INR、肾功能、胆红素水平、血钠、动脉血pH等对肝衰竭预后评估有一定价值,可在临床上参考使用。
主要参考文献
1.中华医学会感染病学分会肝衰竭及人工肝学组.中华医学会肝病学分会重型肝病与人工肝学组.肝衰竭诊治指南.中华肝脏病杂志,2013,21(3):177-183.
2.Gustot T,Fernandez J,Garcia E,et al.Clinical Course of acute-on-chronic liver failure syndrome and effects on prognosis.Hepatology,2015,62(1):243-252.
3.Moreau R,Jalan R,Gines P,et al.Acute-on-Chronic Liver Failure Is a Distinct Syndrome That Develops in Patients With Acute De-compensation of Cirrhosis.Gastroenterology,2013,144:1426-1437.
4.Bernal W,Jalan R,Quaglia A.Acute-on-chronic liver failure.Lancet,2015,386(10003):1576-1587.
第十节
肝脏遗传性疾病

孙旭 刘厚钰
一、肝豆状核变性
肝豆状核变性(Wilson disease)是以铜代谢障碍为特征的常染色体隐性遗传病,由于基因突变,其编码的蛋白发生改变,导致血清铜蓝蛋白(CP)合成减少和胆道排铜障碍,铜离子在肝、脑(尤其是基底核)、肾、角膜等沉积,表现为肝硬化、锥体外系症状、肾功能损害、角膜K-F环等。
【发病机制】
常染色体隐性遗传性铜代谢异常疾病,但铜代谢异常的机理,迄今尚未完全阐明。公认的有胆道排泄减少、铜蓝蛋白合成障碍、溶酶体缺陷和金属巯蛋白基因或调节基因异常等学说。
【临床表现】
1.发病情况
绝大多数在5~25岁时发病,10~25岁占85%,最迟可在40~50岁时才发病,5岁前与50岁后几乎不发病。男女之比约为2∶1~5∶1。本病的临床表现差异较大,各系统均可累及。不同年龄组发病时临床表现不同。在儿童期以肝脏受累为主,随着年龄的增长,神经、精神症状则愈来愈明显。本病大多呈缓慢进行性,约于起病后4~5年死于肝衰竭。若无驱铜治疗,能生存10年以上者极少见,预后不良。
2.肝脏症状
肝脏病变常早于中枢神经系统损害,约半数患者在锥体外系症状出现前曾有黄疸或肝脏肿大。临床上肝脏损害症状表现形式多样,多为隐匿发病,表现为疲乏、食欲缺乏、恶心、呕吐等。少数患者可出现大块性肝坏死,进行性黄疸、腹水和肝衰竭等暴发性肝炎的表现。10%~30%的患者表现为慢性活动性肝炎,临床和病理与其他类型的慢性活动性肝炎无法区别。晚期患者可有肝脾大、腹水、水肿、上消化道出血或肝性脑病等表现。
3.神经精神系统症状
震颤早期常限于上肢,渐延及全身,多表现为快速、节律性、粗大似扑翼样的姿位性震颤,可并有运动时加重的意向性震颤。发音障碍与吞咽困难多见于儿童期发病,说话缓慢似吟诗,或音调平坦似念经,或言语断裂似呐吃;暴发性或震颤性语言吞咽困难多发生于晚期患者。肌张力改变,大多数患者肌张力呈齿轮样、铅管样增高,致动作迟缓、面部表情减少、写字困难、步行障碍等。少数舞蹈型患者伴肌张力减退。癫痫发作较少见。少数患者以精神症状为首发症状,易被误诊为精神分裂症。
4.角膜色素环(K-F环)
见于90%以上的患者,是诊断本病的重要体征之一,在神经症状出现前几年已存在,是早期发现无症状型患者的重要依据。此外,K-F角膜环还可见于长期胆汁淤积伴有铜沉积的患者,色素环经驱铜治疗后变淡或消失,可作为判断疗效的指标之一。
【诊断】
①遗传病史;②临床表现;③辅助检查;④血铜和血清铜蓝蛋白降低;⑤尿铜增加;⑥青霉胺排铜试验阳性;⑦放射性铜负荷试验;⑧眼裂隙灯检查:角膜色素环阳性;⑨脑CT扫描:显示脑室扩大或脑实质软化灶;⑩基因诊断:为了能早期诊断,尤其是确定症状前病例,目前国内外已开始致力于基因诊断,详见第二十三篇第六章第一节肝豆状核变性。
【治疗】
1.低铜饮食 每日食物中含铜量不应>1mg,不宜进食动物内脏、鱼虾海鲜、巧克力和坚果等含铜量高的食物。避免使用铜器烹饪储备。
2.驱铜治疗 促进体内铜排泄,减少铜吸收,建立体内铜代谢负平衡,是目前最有效的疗法。常用药物为二巯基丙醇,二巯丁二酸,二巯丙磺酸钠,D-青霉胺,依地酸二钠钙,锌制剂等。
3.护肝治疗及改善脑功能药物。
4.中药治疗 祖国医学对本病以肝风论治,有些中药能促进铜排泄,如大黄、黄连、黄芩、半枝莲等。
二、α 1 -AT缺乏性肝病
α 1 -AT缺乏性肝病(alpha1 anti-trypsin deficiency-associated liver disease)为常染色体显性遗传病,基因定位14q32.1,正常为纯合子 PiMM 基因,变异时成纯合子 PiZZ 或杂合子 Pi MS 、 MZ 、 SZ 等基因,在肝内产生病理性α 1 -AT,无抑制胰蛋白酶和其他蛋白酶作用。病理性α 1 -AT分子量小,溶解度低,肝无法排泌到血中,大量积聚在肝脏造成炎症破坏,可发展为肝硬化和肝癌。 PiZZ 基因型造成肝损害较严重, Pi MS 、 MZ 、 SZ 基因型损害较轻。病理表现为小结节性肝硬化,HE染色见大小不等的球形红色嗜酸性小体,过碘酸Schiff染色阳性,称为PAS小体。
【临床表现】
任何年龄男女均可发病,临床表现多样性。新生儿黄疸,肝损害,15%~20%有肝大。2% PiZZ 型合并肝硬化。儿童,成人表现为慢性活动性肝炎,10%发生肝硬化,男性多于女性,肝癌的发病率明显高于正常。70%~80%的患者伴有肺气肿。结直肠癌风险为正常3倍。
【诊断】
1.原因不明的肝硬化。
2.血α 1 -AT明显减少或缺乏,血清球蛋白减少。
3.肝穿刺活检发现PAS包涵体。
4.家族史。
5.孕期羊膜穿刺或绒毛活检检出 ZZ 基因型。
6. Pi 基因表型分析。
【治疗】
1.肝移植。
2.基因治疗。
3.近年来研究者们还尝试将不同类型的干细胞诱导分化并修饰含有正常基因的肝细胞,作为自体移植的一个潜在体外来源。
三、肝糖原累积病
肝糖原累积病(liver glycogen storage diseases)为常染色体隐性遗传病,因基因变异而致先天性糖代谢酶缺乏,产生正常或不正常结构的糖原,在肝和其他器官组织中累积,造成损害。根据缺乏的酶的类型不同,分为14型,包括0、Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ、Ⅵ、Ⅶ、Ⅷ、Ⅸ、Ⅹ型等。肝是最大的糖原储存器官,故大多型糖原累积病都可引起肝大,但只有0、Ⅰ、Ⅲ、Ⅳ型可引起有临床表现的肝病。
【分型】
1.0型
糖原合成酶缺乏,少见,早期即死亡。
2.Ⅰ型
葡萄糖-6-磷酸酶缺乏,可见于成人。可有肝大,肝硬化,转氨酶轻度增高,反复明显低血糖,高脂血症,乳酸增高,酮症酸中毒。其特征为75%出现肝腺瘤,但恶变少见。治疗:高糖多餐饮食,维持血糖在4.2mmol/L以上。
3.Ⅲ型
淀粉1,6-葡萄糖苷酶缺乏。婴儿期即有肝大,常见肝纤维化,发展为肝硬化少。低血糖及高脂血症表现较Ⅰ型为轻。肝穿刺活检无腺瘤改变。治疗:少量多次高蛋白饮食。
4.Ⅳ型
淀粉1,4→1,6转葡萄糖苷酶缺乏。肝脾大,进行性肝硬化,常在幼年期死亡。
【临床表现】
临床表现轻重不一。重症者新生儿期即可出现严重低血糖、酸中毒、呼吸困难、肝大等症状;轻症病例常在婴幼儿期因生长迟缓、腹部膨胀等就诊。由于慢性乳酸酸中毒和长期胰岛素/胰高糖素例失常,患者身材明显矮小,骨龄落后,骨质疏松。腹部因肝持续增大而膨隆显著。肌肉松弛,四肢伸侧皮下常有黄色瘤。但身体各部比例和智能等都正常。患儿时有低血糖发作和腹泻发生。少数幼婴在重症低血糖时尚可伴发惊厥,但亦有血糖低下无明显症状者。随着年龄的增长,低血糖发作次数可减少。由于血小板功能不良,患者常有流鼻血等出血倾向。
【诊断】
病史、体征、血生化检测可供初步临床诊断。糖代谢功能试验可能有助诊断:如糖耐量试验中因患儿胰岛素分泌不足,呈现典型糖尿病特征;胰高糖素或肾上腺素试验亦不能使患儿血糖明显上升,且注射胰高糖素后,血乳酸明显增高;由于患儿不能使半乳糖或果糖转化为葡萄糖,因此在半乳糖或果糖糖耐量试验中血葡萄糖水平不升高。这类功能试验虽有避免作肝组织活体检查的优点,但由于本病患儿对此类试验反应的个体变异较大,故仍应以肝组织的糖原定量和葡萄糖-6-磷酸酶活性测定作为确诊依据。
【治疗】
本病的病理生理基础是在空腹低血糖时,由于胰高糖素的代偿分泌促进了肝糖原分解,导致了体内6-磷酸葡萄糖累积和由此生成过量的乳酸、三酸甘油酯和胆固醇等一系列病理生化过程。因此,从理论上讲,任何可以保持正常血糖水平的方法即可阻断这种异常的生化过程,减轻临床症状。
四、血 色 病
特发性血色病(idiopathic hemochromatosis,HH)是先天性铁代谢障碍导致体内铁存积过多而引起肝硬化、心肌病、糖尿病、性腺功能减退、皮肤色素沉着、关节炎等多系统表现的遗传性疾病。定位于6qP21.3的 HFE 基因变异引起饮食中的铁吸收大量增加,称为原发性铁过载,大量铁沉积在肝、胰、心和关节皮肤等。肝内铁沉积可超过正常10倍以上,使肝内强氧化剂形成过多,造成细胞膜,脂质,蛋白质和核酸损伤,也增加癌变可能。 HFE C 282 Y 纯合子变异可引起肝损害,杂合子变异可有铁过载但无肝损害。
【临床表现】
新生儿起即有铁过载,但损伤进展较慢。通常40~50岁出现临床症状。75%以上有肝病表现,表现为纤维化、肝硬化、癌变。 HFE 纯合子变异1/3可癌变。女性月经引起失铁,发病晚于或轻于男性,男女发病比为10∶1。如果患者出现难以解释的肝脏肿大、皮肤色素沉着、特发性心肌病、关节炎、糖尿病和(或)性欲减退,则应考虑血色病。16%~58%的患者有腹痛表现。
【诊断】
1.血清转铁蛋白饱和度>45%。
2.血清铁>正常2倍。
3.肝穿刺活检肝组织铁大于1.9mmol/g。
4.基因表型分析。
【治疗】
1.铁螯合剂排铁 去铁敏1分子可络合3个铁离子。
2.控制铁摄入,放血排铁 证据表明,在肝硬化或糖尿病发生前放血疗法可显著降低HH的发病率和死亡率。因此,对高危人群早期诊断和及时处理非常必要。初始治疗:只要能耐受,每周放血1~2次,每次1U(根据红细胞压积,大约相当于250mg铁)。放血后红细胞压积应下降10%或低于初始值的20%。维持治疗:治疗初始阶段每进行10~12次放血治疗后检测血清铁蛋白水平,血清铁蛋白<50ng/ml,则停止常规放血,改为维持放血,使血清铁蛋白水平保持在25~50ng/ml。
3.抗氧化治疗 如维生素E,维生素C。
4.受累器官并发症的相应治疗。
五、肝囊性纤维化
为常染色体隐性遗传疾病,因调节胆汁转运的CFTR基因变异而致。可形成胆汁性肝硬化,表现为肝大、碱性磷酸酶增高、黄疸、腹水等门脉高压症状。
六、半乳糖血症
半乳糖血症(galactosemia)为常染色体隐性遗传性疾病。1-磷酸半乳糖尿苷酰转移酶缺陷,肝内半乳糖无法转变为葡萄糖,导致1-磷酸半乳糖和半乳糖醇积聚肝内,也可积聚在肾、眼晶体、脑等。病理早期出现肝脂肪浸润,汇管区胆汁淤积,假胆管形成,假腺体增生(特征),再发展成纤维化、肝硬化。临床少数表现为急性过程,食乳后即发生,大多为亚急性过程,可有黄疸、腹胀、呕吐、低血糖,2~5周后出现腹水,白内障等。
治疗方面,早期诊断后应在饮食中摒除半乳糖,宜终身坚持。经过及时治疗后,白内障、肝大和肝硬化等均可逆转。限制乳类,改用豆浆、米粉等并辅以维生素、脂肪等营养必需物质,豆浆中虽含有能分解出半乳糖的蜜三糖和水苏糖,但不能被人体肠道吸收,故无碍于治疗。通常在限制乳类3~4天后即见临床症状改善,1周后肝功能好转。须避免一切可能含有奶类的食品和某些含有乳糖的水果蔬菜如西瓜、西红柿等。
七、遗传性果糖不耐受症
为常染色体隐性遗传性疾病。肝内1-磷酸果糖醛缩酶缺乏导致果糖和1-磷酸果糖在肝内结聚,造成肝脏炎症及纤维化、肝硬化等表现。
【临床表现】
1.婴儿期即发病,进食果糖或蔗糖后恶心,呕吐,腹痛,低血糖,甚至昏迷,抽搐,意识障碍。发病率0.3~0.4/10万。
2.可有肝脾大、黄疸、腹水等。
3.可有低血磷、高尿酸血症等。
【诊断】
肝穿刺检查1-磷酸果糖醛缩酶活性。
【治疗】
饮食中要完全去除蔗糖、果糖、山梨糖醇。由于这些糖类经常作为添加剂,甚至大部分药物也存在,可能很难做到完全去除。开始治疗后,患者肝肾功能好转,智力发育一般不受影响。进入成年期,即使患者摄入了果糖,症状也较轻微。
主要参考文献
1.Ferenci P,Czlonkowska A,Stremmel W,et al.EASL clini-cal practice guidelines:Wilson's disease.J Hepatol,2012,56:671-685.
2.Natalia KD,Beata K,Wojciech C.Liver disease in cystic fibrosis.Prz Gastroenterol,2014,9(3):136-141.
第十一节
原位肝移植的内科问题

王吉耀 涂传涛
肝移植(liver transplantation,LT)是目前治疗各种病因所致的急、慢性肝衰竭和终末期肝病的标准方案之一。LT术后可长期生存并有较好的生活质量,甚至包括生殖能力的恢复,目前原位肝移植术后1年和10年生存率已分别能达到96%和71%。
选择适当的LT受者和移植时机是肝移植成功的必要条件,而对于术后并发症及原发病复发的监测与有效防治是提高患者生存率的重要保证。
【肝移植受者的选择】
(一)肝移植受者的一般标准
通常患有存在不可逆的、进行性的、致死性的肝脏疾病,除LT外无其他更有效治疗措施,且能耐受LT手术,无手术禁忌证,患者本人及家属对LT充分理解,可以考虑LT。应由多学科综合治疗团队共同评估决定。
(二)移植指征和时机
1.终末期肝病
对各种病因所致的终末期肝硬化登记移植的指征:终末期肝病模型(model of end-stage liver disease,MELD)评分>20(MELD评分参见本章第一节“肝硬化及其并发症”)或者肝硬化Child-Pugh C级并有以下一种情况者:①反复发生门脉高压性出血;②发生过自发性腹膜炎;③反复出现肝性脑病;④顽固性腹水;⑤肝肺综合征或肝肺动脉高压;⑥内科治疗无效的顽固性瘙痒等。
2.急性肝衰竭
King's College标准为:INR>6.5或者满足以下任何三条者死亡率高,应该做急诊肝移植:①年龄<10岁或>40岁;②病因是药物中毒或病毒性肝炎;③INR>3.5;④黄疸出现到发生脑病时间>7天;⑤血清胆红素>300μmol/L。伴有全身霉菌感染、重症胰腺炎、对治疗有反应者不宜立即手术。
3.肝细胞肝癌(HCC)
国际上多采用米兰标准:单发肿瘤直径≤5cm,或多发肿瘤不超过3个且最大病灶直径≤3cm,不伴有血管及淋巴结累及。采用该标准能获得良好的结局,移植后5年生存率超过70%。目前大多数研究小组认为可将标准放宽至患者移植后5年生存率能达到50%,这是可接受的生存率最低标准,这些放宽的标准包括UCSF标准、上海复旦标准和杭州标准等。
(三)禁忌证
1.感染 除肝脏、胆道以外的严重的全身感染,包括活动性肺结核。
2.恶性肿瘤 肝外恶性肿瘤和晚期肝恶性肿瘤。
3.神经心理严重的精神障碍,不能控制的精神病变。
4.重要器官功能衰竭 心、脑、肺、肾等重要器官功能衰竭不能耐受手术者。
5.其他 吸毒、酗酒;不能依从术后免疫抑制剂治疗方案;对LT无充分理解者(小儿除外)等。
【患者移植前的处理】
应及时处理肝硬化及其威胁生命的并发症以减少患者等待LT时的死亡率。
1.乙型肝炎或丙型肝炎
HBV患者口服核苷类似物,HCV患者口服DAAs抗病毒治疗,以改善肝功能和降低术后病毒性肝炎的复发率。
2.经颈静脉肝内门体分流(TIPS)
顽固性腹水及食管胃底曲张静脉反复出血者应行TIPS以改善症状、减少术中失血,并可缩短手术时间,改善预后。
3.急性肝衰竭
在支持治疗的同时,可短期人工肝处理。
4.HCC
必要时可以先行局部治疗如经肝动脉栓塞化疗,无水酒精注射或射频消融等。
5.静脉内高营养
短期静脉高营养可以改善患者营养不良状态,改善预后。
6.其他
酒精性肝病患者必须戒酒半年以上;对非酒精性脂肪性肝病伴肥胖、高血压、糖尿病及血脂紊乱者必须进行评估并予以控制或纠正。
【肝移植术后并发症及处理】
术后近期并发症及处理
1.感染
感染是肝移植术后最常见的并发症和主要死亡原因。
(1)细菌感染:
最为常见,多发生于术后的1个月内,表现为手术部位感染、肝脓肿、胆道感染、肺炎、尿路感染、全身性菌血症及败血症。发生率为6%~30%,病死率为5%~40%。最常见的细菌是大肠埃希菌、变形杆菌、肠球菌、肺炎球菌和金黄色葡萄球菌等,但多半为混合感染。只要LT患者表现出感染的任何征兆(如发热)及败血症迹象,或者出现部位明确的感染,在获取血或其他相关组织样本后应立即开始经验性抗生素治疗。常用药物是第三代和第四代头孢菌素、哌拉西林-三唑巴坦及喹诺酮类药物。对败血症患者可使用糖肽类药物(万古霉素或替考拉宁)及碳青霉烯类药物(亚胺培南、美罗培南等)。一旦鉴定出致病菌应行药敏试验,并调整治疗方案。
肺炎易发生于移植后早期以及机械通气的患者,应采用侵入性诊断方法,如通过纤维支气管镜行支气管肺泡灌洗或肺活检以及时鉴定致病微生物。适度止痛、加强通气可预防肺部感染;有大量胸腔积液时应及时穿刺放液。如患者伴有ALP、γ-GT、胆红素升高,应行超声检查明确有无胆道梗阻,必要时行ERCP。肝移植后胆道狭窄是行ERCP后发生感染的一个危险因素,建议患者在接受ERCP时预防性应用具有广谱抗菌作用抗生素,如哌拉西林-他唑巴坦和碳青霉烯类。
(2)真菌感染:
发生率在7%~42%之间,其中念珠菌和曲霉菌是最常见的病原体。术后真菌感染是受者患病和死亡的重要病因。研究显示氟康唑、伊曲康唑和脂质体两性霉素B,单独或联合应用5天到10周的预防方案对于降低真菌感染的发病率(RR 0.7)和死亡率(RR0.72)是有益的。侵袭性念珠菌感染应采用氟康唑或伊曲康唑治疗。侵袭性曲霉菌病的治疗可单独或联合应用两性霉素B、伏立康唑或卡泊芬净。在病情允许的情况下应尽可能减少免疫抑制剂的应用。
(3)病毒感染:
巨细胞病毒(CMV)感染是最重要的机会性感染病原体,发生率可达30%~65%,多在移植后3~8周出现。临床表现为发热、乏力、关节痛、白细胞减少,较严重的CMV感染伴肝炎症状及转氨酶升高和恶心呕吐、腹泻等肠炎症状及消化道出血,有时无转氨酶升高而发生淤胆。血清抗原检测或PCR技术检测CMV DNA,组织学检查可及时作出诊断。更昔洛韦5mg/kg,每12小时1次,静脉滴注14~21天,最好用到CMV DNA阴性2周(每周检测1次),接着口服泛昔洛韦共3个月。应同时减少免疫抑制剂用量。供体血清CMV阳性者,受体术后口服泛昔洛韦可预防患者CMV感染。CMV高危患者至少进行CMV预防治疗3个月。
其他的病毒感染常见的有单纯疱疹病毒(发生率最高达40%)和EB病毒(EBV)。LT前EBV血清阳性患者,随着术后免疫抑制剂的逐渐增加,其发生移植后淋巴细胞增殖性疾病(post-transplant lymphoproliferative disease,PTLD)的风险较高。一般采用阿昔洛韦和泛昔洛韦进行治疗和预防。
(4)卡氏肺孢虫:
卡氏肺孢虫性肺炎多发生在术后3~6个月,临床表现为干咳和呼吸困难,血气提示中重度低氧血症而胸片可正常。怀疑该病时应静脉用TMP/SMZ。通过支气管镜作气管冲洗、拉网、银染色查到肺孢虫可诊断。测定血中卡氏肺孢虫抗原与抗体,可获快速诊断。出现肺浸润难以诊断时应做肺活检,早期诊断可缩短病程,诊断延误常造成死亡。LT患者可以给予SMZ 6~12个月预防。
2.排斥反应
肝移植后患者肝功能稳定情况下,突然出现ALT升高和黄疸,排除感染、肝动脉栓塞和胆道疾病,应考虑排斥反应。由于临床表现和实验室检查缺乏敏感性和特异性,肝脏组织学仍然是诊断排斥反应的金标准。急性排斥反应可以用泼尼松龙500mg/d,共3天。丙肝患者慎用,可以加大钙调磷酸酶抑制剂的剂量。
目前大部分肝移植患者还需要接受终身免疫抑制治疗。基于钙调磷酸酶抑制剂(CNI)包括环孢素A(CsA)和他克莫司(Tacrolimus,Tac,FK506)的免疫抑制治疗,尤其是 Tac的应用,改善了肝移植患者移植物的长期生存率,是免疫抑制治疗的基石。一般半年后可停用激素(自身免疫性肝病可用小剂量激素泼尼松5mg/d维持)。低剂量的CsA或Tac与抗代谢药(硫唑嘌呤或吗替麦考酚酯)或mTOR抑制剂(西罗莫司、everolimus)合用是最常用的方案(免疫抑制药物的作用机制和不良反应见第十七篇第五章)。
3.肾脏损害
肾功能不全是移植后致死和致病的主要原因。移植后1年和3年的累计发生率分别为8.0%和13.9%。慢性CNI毒性导致肾实质结构的改变是肾衰竭的主要原因。防治措施包括:控制血压和糖尿病;避免肾毒性药物;缩短CNIs药物使用时间。1/3肝移植患者需要做短期血透,5%需长期治疗血透。指征为尿量<0.25ml/(kg·h)(心功能正常、血容量充足时),血钾>7mmol/L,BUN>100mg/dl,pH<7.2,对药物治疗无反应者。
4.药物性肝损伤
应减少不必要的药物和缩短静脉高营养时间,密切监测肝功能,一旦出现肝损伤尽可能停用可疑药物。
【术后远期并发症及处理】
1.高血压
是肝移植后最常见的心血管系统并发症,发生率达40%~85%。CNI和糖皮质激素是导致高血压的主要原因。对于持续性高血压应给予钙通道拮抗剂、β受体阻断药或利尿药联合治疗,应控制血压<140/90mmHg,ACEI制剂可用于伴糖尿病患者的治疗。
2.糖尿病
移植后新发糖尿病高达10%~64%,如果糖化血红蛋白>6.5%,应该开始治疗。必要时调整免疫抑制剂。
3.脂质紊乱
发生率40%~66%。CsA易导致高脂血症,应用他克莫司替代CsA可能减轻高脂血症,治疗可应用他汀类药物。需注意他汀类药物与CNIs均通过细胞色素P450酶代谢,可相互作用。
4.胆道并发症
术后发生率10%~40%,包括胆道狭窄、胆漏、胆道感染、结石等,6%~13%需再次移植,病死率约19%,其中缺血型胆道病变(ischemic-type biliary lesion,ITBL)受到重视,术后发生ITBL的高危因素为:原发病为重型乙肝、ABO血型不符,供肝冷保存时间>12小时和术后肝动脉病变。ERCP和MRCP诊断率高,ERCP可识别87%的胆漏患者。根据不同病因和病变可采用药物、胆道扩张或支架、胆道手术和再移植处理。
5.骨质疏松症
LT术前有骨密度减低和骨量减少者应每年监测骨密度。对骨质疏松症或反复骨折患者应予钙剂与维生素D-二磷酸盐治疗。
6.恶性肿瘤
(1)PTLD:
和EBV相关,可累及淋巴结及结外组织,出现类似于感染性单核细胞增多症的反应性浆细胞增生或形成淋巴瘤。治疗包括在病情允许的情况下免疫抑制剂减量,当PTLD进展为淋巴瘤时采取化疗,对有肿物的患者行外科手术和放疗。
(2)皮肤癌:
是LT后患者最常见新生恶性肿瘤,非黑色素瘤皮肤癌如鳞状细胞癌和基底细胞癌比黑色素瘤更常见。
(3)其他:
PSC和炎症性肠病患者移植后结直肠癌的风险较高,因此,推荐每年行结肠镜筛查。
【原发肝病复发监测与防治】
(一)原发肿瘤的复发
严格掌握HCC移植指征(米兰标准)可以减少复发。
(二)病毒性肝炎
1.慢性乙型肝炎
在肝移植前1~3个月需服用核苷(酸)类似物(NUCs)恩替卡韦或替诺福韦。术中无肝期加用乙型肝炎免疫球蛋白(HBIG),术后长期联合使用NUCs和HBIG。
HBs Ag阴性受体接受抗HBc阳性供肝时,立即给予NUCs预防治疗。
2.慢性丙型肝炎
在移植前进行抗病毒治疗。移植后应随访,所有丙型肝炎复发患者建议采用直接抗病毒药物。
3.其他
酒精性肝病患者移植后应继续戒酒。NAFLD患者LT后应当避免体重超重,控制糖尿病、血脂紊乱和高血压。
【术后妊娠】
成功LT对男性和女性的性激素紊乱均有改善作用,但是免疫抑制药物干扰激素的代谢。移植后性功能可得到显著改善。移植后最初12个月避免妊娠,也有些中心建议等待24个月。妊娠期间免疫抑制剂仍应当维持治疗,尚未报道类固醇激素、CNIs和硫唑嘌呤有致畸作用,不推荐吗替麦考酚酯和硫唑嘌呤联合应用。
主要参考文献
1.Webster DP,Klenerman P,Dusheiko GM,et al.Hepatitis C.Lancet,2015,385(9973):1124-1135.
2.Burra P,Burroughs A,Graziadei I,et al.EASL Clinical Practice Guidelines:Liver transplantation.J Hepatol,2016,64(2):433-485.
第十二节
肝酶异常的评估

涂传涛 王吉耀
肝功能检查(liver function tests,LFTs)是一组反映肝脏合成、分泌与代谢功能状态以及肝损伤的相关生化指标。本节主要介绍肝酶异常(abnormal liver enzyme)的临床意义与评估思路。肝酶异常在临床上非常常见,可因健康体检或其他疾病行LFTs时偶然发现,患者往往无症状或症状轻微;也可以因恶心、腹胀、皮肤或巩膜黄染等症状在进一步检查中发现。临床实践中检查肝酶的意义在于:对肝胆疾病的筛查与随访;对药物潜在肝毒性的监测;对已知肝病严重程度、预后及治疗应答的判断等。
【肝酶的分类及其临床应用价值】
(一)提示肝细胞炎症坏死的酶类
1.氨基转移酶
氨基转移酶包括丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)。ALT广泛存在机体组织细胞内,以肝细胞含量最多,其次为心肌、脑和肾组织中,肝脏中ALT主要存在于肝实质细胞的胞质内,其肝内活性较血清高100倍;AST主要分布于心肌,其次为肝脏、骨骼肌、肾、胰腺等组织中,肝脏中80%存在于肝细胞线粒体中,胞质中占20%。因此,ALT是肝脏相对特异性酶,其敏感性与特异性均超过AST,且比AST释放血循环更早,临床上ALT常用于肝脏疾病的筛选与诊断。
血清氨基转移酶升高主要反映肝细胞损伤。许多病因可导致ALT和AST升高,包括病毒性肝炎、药物或毒物肝损伤、酒精性肝病、缺血性肝病、自身免疫性肝炎、肿瘤浸润和全身性疾病等(表15-8-16)。慢性肝病时血清氨基转移酶常低于5倍正常上限(ULN);急性肝损伤时则显著升高(常超过10倍ULN),如急性病毒性肝炎、药物性肝损伤或酒精中毒、低血容量、缺血-再灌注或休克等,部分患者可在临床症状出现之前就急剧升高。一般而言,急性肝炎时血清ALT高低与临床病情轻重相平行,肝炎恢复期ALT往往最后才降至正常,可作为判断急性肝炎是否恢复的良好指标。特别注意的是急性肝衰竭或重症肝病时由于大量肝细胞坏死“耗竭”,血清ALT短期逐渐降低或迅速“正常化”,而胆红素却进行性升高,出现所谓“胆酶分离”现象,是预后不良的征兆。这时需要结合白蛋白、前白蛋白、凝血酶原时间、胆碱酯酶等指标来判断。
表15-8-16 导致氨基转移酶升高的病因
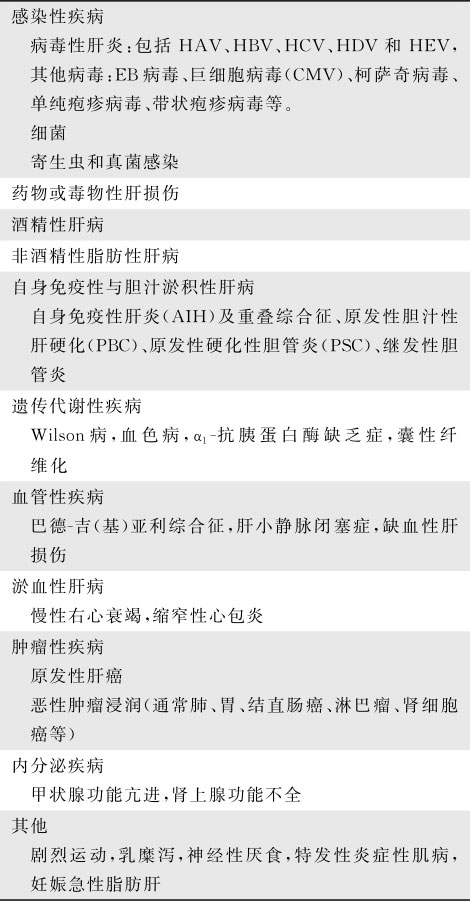
AST通常和ALT联合应用于肝病的评估与诊断,尤其是AST与ALT的比值(即De Ritis指数)有助于鉴别酒精性肝炎,AST/ALT比值>2高度提示酒精性肝病;在慢性肝炎时,尤其是肝硬化患者,AST升高程度往往超过ALT,这可能与慢性肝病时ALT合成降低而AST合成不受影响有关。
2.乳酸脱氢酶(Lactate dehydrogenase,LDH)
广泛存在于机体各组织中,其中以心肌、骨骼肌和肾含量最丰富,其次为肝脏、脾脏、胰、肺、肿瘤组织和红细胞。LDH对诊断具有较高的敏感性,但特异性较差。血清中存在5种LDH同工酶,借助同工酶分析有助于对肝实质性损伤的诊断,LDH检测对肝病诊断的敏感性和特异性均不及氨基转移酶,但对心肌梗死和溶血诊断更有价值。
(二)提示胆汁淤积的酶类
1.碱性磷酸酶(alkaline phosphatase,ALP)
在碱性环境下能水解多种磷酸单酯化合物,该酶活性依赖于锌。广泛存在于肝脏、骨、小肠、肾脏、胎盘等组织器官。血清中ALP主要来自于肝脏、骨骼和肠道,在肝脏ALP主要分布在肝细胞胆管侧细胞膜,肝病时ALP升高可能与胆汁酸诱导该酶合成增加有关。在评估ALP异常时可结合ALP同工酶进行分析,其同工酶通常分为3大类,即胎盘、肠和肝/骨/肾ALP同工酶。病理情况下还可以出现肝ALP和胆汁ALP等“高分子ALP”,以及一些和肿瘤有关的变异ALP。
成人血清ALP升高最常见临床状况包括肝胆疾病、骨骼疾病及妊娠。Wilson病、恶性贫血、甲状腺功能减退、先天性低磷酸盐血症、锌缺乏以及儿童的某些类型进行性家族性肝内胆汁淤积等疾病时ALP通常低于正常值。
2.γ-谷胺酰转肽酶(γ-glutamyltransferase,GGT)
分布在多种组织包括肾、胰腺、肝脏、脾脏、心脏、脑及生精管的细胞膜上。GGT在肝脏中广泛分布于肝细胞的毛细胆管一侧和整个胆管系统,因此GGT是胆道疾病最敏感的血清标志物。GGT的临床价值在于它有助于判断ALP升高的组织来源,因为GGT活性在骨骼疾病时并不升高。血清GGT升高通常见于肝、胆道及胰腺疾病,该酶在肝胆疾病中的表现模式与ALP、5'-NT及LAP类似,GGT测定对诊断肝病较ALP和LAP更敏感。另外,高GGT水平也见于服用巴比妥类药物或苯妥英钠患者以及酗酒者,此时其他血清酶和胆红素浓度可能正常。
3.5'-核苷酸酶(5'-nucleotidase,5'-NT)
广泛分布在肝、肠、脑、心脏、血管及胰岛,但血清5'-NT仅来源于肝胆组织。在肝脏该酶主要位于毛细胆管和窦状间隙膜上,血清5'-NT升高主要见于肝胆疾病,其升高程度与ALP相似,两种酶变化的平行关系提示它们存在于肝细胞类似的亚细胞部位。大量的研究表明,ALP与5'-NT对胆道梗阻、肝浸润性或占位性病变的诊断具有同等价值,然而部分患者可见到一种酶升高而另一种酶正常的情况。5'-NT活性水平在正常妊娠过程中的变化报道不一。因此,5'-NT检测的最大价值在于对肝胆疾病诊断的特异性。除妊娠者外,对血清ALP升高的患者,若同时存在5'-NT升高,则提示血清ALP升高是肝源性的。
4.亮氨酸氨基肽酶(leucineaminopeptidase,LAP)
是一种蛋白水解酶,广泛存在于人体各组织,但以肝、胰、胆、肾、小肠和子宫肌层中含量最丰富。LAP在肝脏中的活性较强,主要位于胆管上皮。LAP水平升高似乎对肝脏疾病是特异性的,这一点与ALP和5'-NT相似。骨病患者LAP不升高,儿童与成人测定值之间也无差别。除肝胆疾病之外,唯一能引起该酶血清水平升高的情况是妊娠;氯丙嗪、雌激素、吗啡等可使血清LAP升高。血清LAP在诊断阻塞性、浸润性或占位性病变时与ALP及5'-NT同样敏感。尽管绝大多数类型的肝病均出现LAP水平升高,但以胆道梗阻时活性最高,因此LAP是鉴别阻塞性肝病与肝细胞性肝病的可靠检查指标。
(三)临床应用价值
ALT、AST和LDH升高通常提示肝细胞炎症坏死;ALP、GGT、LAP和5'-NT升高则提示胆汁淤积。基于肝酶升高的程度及特征将血清肝酶大致分为三类:肝细胞损伤型、胆汁淤积型和混合型,各型界定的标准如下:①肝细胞损伤型:ALT≥3×ULN(正常值上限),且ALT/ALP≥5;②胆汁淤积型:ALP≥2×ULN,且ALT/ALP≤2;③混合型:ALT≥3×ULN,ALP≥2×ULN,且2<ALT/ALP<5。
【对肝酶异常的评估与分析思路】
肝酶异常不具有特异性,对肝酶异常的评估应基于完整病史及其相关临床资料,既要贯彻规范化的评估思路,又要有针对性的分析策略,避免过度检查。同时,应当记住肝酶正常也不能完全排除肝胆疾病存在,而一过性或轻度肝酶升高是非特异性的,注意动态观察随访。评估肝酶升高通常遵循以下思路:首先,基于病史资料,初步判断或排除肝酶异常是由肝胆疾病所致;其次,基于酶学特点,判断肝脏损伤的大致类型,如炎症坏死、胆汁淤积性、代谢性或浸润性疾病;第三,结合必要实验室检查,明确或发现潜在的病因;第四,评估严重程度及预后,以便及时、有效地处理。
(一)临床分析
1.病史
系统而有重点地询问病史,往往能发现导致肝病的潜在危险因素或初步判断肝酶异常的大致方向。如有无慢性肝病史尤其是慢性病毒性肝炎史;有无大量饮酒史;近期有无药物(包括中药、保健品等)服用史;生活和工作环境中有无有害物质或毒物接触史;有无心、脑、肾、糖尿病、甲状腺功能亢进、胆道结石和胆囊炎等慢性疾病史;有无手术、外伤、纹身及输血史;有无慢性肝病及胆道疾病家族史;近期有无上呼吸道感染史,有无缺血-再灌注史,有无疫区旅游史,有无不洁性接触史;是否存在乏力、厌食、纳差、皮肤瘙痒、发热、右上腹痛、关节与肌肉疼痛;以及女性的月经、妊娠史等。
2.体格检查
寻找病因的线索和慢性肝病的体征。如体型肥胖和腰围增粗提示脂肪性肝病可能;皮下瘀点或出血点提示凝血功能异常;皮肤巩膜黄染提示急、慢性肝损伤或胆汁淤积;肝掌、蜘蛛痣、腹壁静脉曲张、男性乳房发育、睾丸萎缩等提示存在慢性肝病;颈静脉充盈或怒张提示右心衰竭和缩窄性心包炎;突眼和甲状腺肿大提示可能存在甲状腺功能亢进;浅表淋巴结肿大尤其Virchow淋巴结肿大提示消化道肿瘤可能;肌肉触疼、软弱提示酒精性肝病可能,肌肉萎缩与关节变形可能存在风湿免疫疾病;眼科裂隙灯下检查有K-F环及神经系统异常提示可能存在Wilson病等。
体格检查还要重点检查腹部,如肝脏大小、质地、硬度,脾脏大小,腹部移动性浊音,腹部压痛及包块,墨菲征或触及肿大胆囊等。也不能忽视其他部位检查。
(二)实验室和辅助检查的选择
1.实验室检查
血、尿、便三大常规,疑为 Wilson病患者检查24小时尿铜含量;凝血功能检测;生化指标主要包括:其他肝功能试验、肾功能、血脂、血糖、电解质、铜蓝蛋白、铁蛋白、免疫球蛋白(IgE、IgM、IgG和IgG4),胆碱酯酶;免疫指标主要包括:病毒性肝炎标志物、EB病毒抗体、巨细胞病毒抗体、自身免疫性肝病相关抗体、甲状腺功能、消化道肿瘤标志物(AFP、CEA、CA19-9)等。对于HBV和HCV患者行病毒学检测。
2.影像学检查
腹部超声检查最常规的、重要检查手段,能发现肝外胆汁淤积或黄疸的病因线索,以及脂肪肝、肝硬化、肝脏占位及浸润性疾病。必要时行腹部CT、MRI或MRCP、ERCP、超声内镜检查进一步明确。对于怀疑巴德-吉(基)亚利综合征患者可行血管彩超多普勒检查或门静脉及下腔静脉CT血管造影检查;怀疑淤血性肝病者行心脏超声检查。
3.肝穿刺
最后考虑的步骤,主要目的:第一,为排除或证实诊断,或为病因诊断提供线索;第二,病因虽明确,需要进一步明确肝脏炎症与纤维化程度以指导治疗。
(三)临床诊断路径
根据临床资料及必要的检查,明确肝酶异常以肝细胞损伤为主还是以胆汁淤积为主,前者以氨基转移酶升高为特征,后者以ALP升高伴或不伴有胆红素升高为特征。还存在一部分混合型患者。肝酶升高的分析与评估思路如图15-8-5。
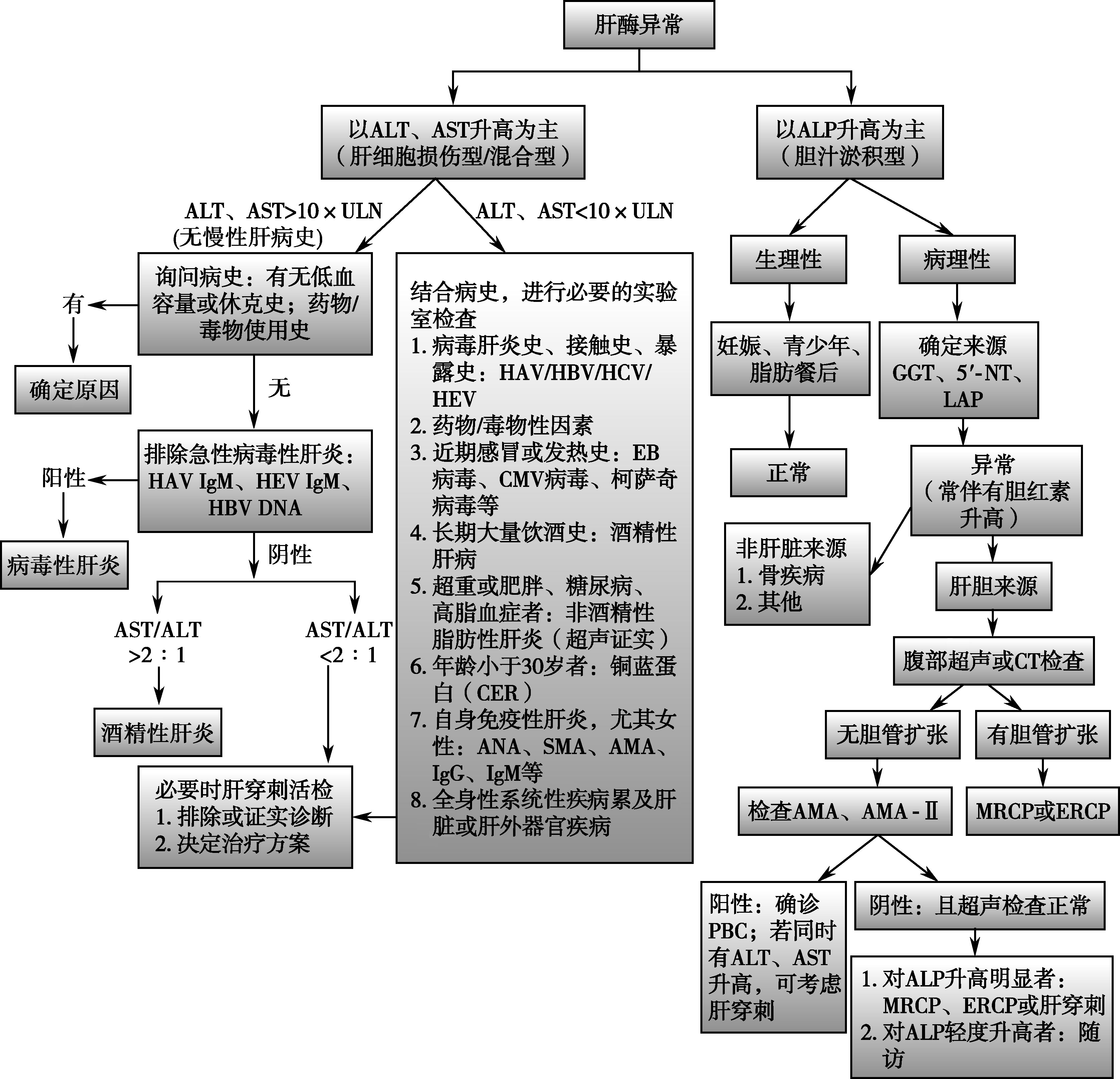
图15-8-5 肝酶升高的诊断评估路线
主要参考文献
1.Fitz JG.Approach to the patient with abnormal liver chemistries or jaundice.In Podolsky DK,Camilleri M,Fitz JG,et al.Yamada's Textbook of Gastroenterology,6th ed.Oxford:John Wiley&Sons Ltd,2016,819-833.
2.Lee TH,Kim WR,Poterucha JJ.Evaluation of elevated liv-er enzymes.Clin Liver Dis,2012,16(2):183-198.

