第六章
粒细胞、组织细胞疾病
第一节
中性粒细胞减少与粒细胞缺乏症

李 锋
正常白细胞总数为(3.5~9.5)×10 9 /L。当白细胞计数<3.5×10 9 /L时称为白细胞减少症(leukopenia)。因为中性粒细胞在白细胞中占绝大部分(50%~70%),所以白细胞减少在大多数情况下是因为中性粒细胞减少所致。当中性粒细胞绝对计数<1.5×10 9 /L时称为中性粒细胞减少症(neutropenia),<0.5×10 9 /L时称为粒细胞缺乏症(agranulocytosis),简称粒缺,为重症粒细胞减少症,极易发生严重的难以控制的感染。
【病理生理】
正常人每日在骨髓内生成大量的中性粒细胞(约10 11 个/日),粒细胞集落刺激因子(G-CSF)和粒-单核巨噬细胞集落刺激因子(GM-CSF)能促使骨髓增殖池内的静止期造血干细胞进入细胞增殖周期,诱导粒系祖细胞进一步增殖和分化。晚幼粒细胞停止增殖,在骨髓成熟池内继续分化成熟为杆状核和中性分叶核粒细胞。这些细胞在进入周围血液前可在骨髓贮备池内逗留5天左右,数量可达血液中的8~10倍。
进入血管内的中性粒细胞约有1/2进入边缘池,也就是紧贴于毛细血管和小静脉的内皮细胞,它们不随血液流动。临床所测得的白细胞计数,只是剩下随血液循环流动的也就是循环池内的白细胞。循环池与边缘池内的粒细胞可相互转换。
粒细胞在血管内一般仅逗留数小时即凋亡或游移至血管外进入组织,执行其防御病原体及清除“废物”的功能,约1~2天死亡。在细菌、病毒、真菌或立克次体感染、过敏反应等情况下,受GM-CSF、G-CSF、黏附分子、趋化因子IL-8和IL-1等的调节,粒细胞生成增加,从骨髓释放和进入组织增多,吞噬作用和杀菌活性增强。在严重感染时,机体对上述体液因子缺乏足够的反应,同时中性粒细胞上的黏附分子(CD11/CD18等)和血管内皮细胞上的黏附分子(ICAM-1)被炎症介质所激活,使粒细胞易于黏附血管壁并迁移至组织。
【病因】
(一)先天性中性粒细胞减少症
为一组罕见的先天性遗传性疾病,多见于婴幼儿发病,有三种类型:①严重先天性中性粒细胞减少症(大多具有 ELANE 基因突变);②周期性中性粒细胞减少症:每间隔21天发作粒缺1次,每次持续3~5天;③伴随其他先天性综合征包括一些免疫缺陷和代谢异常综合征同时出现的中性粒细胞减少症。此外,尚有种族性和良性家族性中性粒细胞减少症(ethnic and benign familial neutropenia)。
(二)获得性继发性中性粒细胞减少症
1.药物诱发中性粒细胞减少症
是临床最常见中性粒细胞减少的病因。多种药物可以引起中性粒细胞减少。抗肿瘤药物和免疫抑制剂都能直接杀伤增殖细胞群,抑制或干扰粒细胞的代谢和分裂。药物的直接毒性作用造成粒细胞减少的程度,与药物剂量相关。其他多类药物亦可通过直接的细胞毒性或药物作为半抗原在敏感者体内经免疫机制产生抗体,使粒细胞生成减少或破坏增多。
特应性药物性粒细胞缺乏症(idiosyncratic drug-induced agranulocytosis)是临床上的严重情况,呈急性发作,多数病例中性粒细胞<0.1×10
9
/L,伴严重深部组织感染和败血症,特别是老年(>65岁),伴休克及脏器功能衰竭,病死率极高,近年来随着静脉用广谱抗生素及G-CSF的应用,病死率已降低为5%。据欧洲统计,这种粒缺发生率为1.6~9.2/100万人口,最常见的药物为抗生素(特别是β-内酰胺类及复方磺胺甲异
 唑)占25%,抗甲状腺药物(卡比马唑)23%,抗血小板药(噻氯匹定)16%,抗癫痫药11%,非甾体抗炎药8%等。
唑)占25%,抗甲状腺药物(卡比马唑)23%,抗血小板药(噻氯匹定)16%,抗癫痫药11%,非甾体抗炎药8%等。
2.骨髓损伤引起中性粒细胞减少
见于慢性苯中毒;放射线可导致急性自限性和慢性骨髓损伤;骨髓被异常细胞浸润损伤骨髓包括各种癌肿(包括肺、乳房、前列腺和胃等)转移骨髓,可使骨髓造血功能衰竭,恶性造血系统疾病骨髓衰竭综合征及骨髓纤维化等,都能引起骨髓正常血细胞的生成减少,使中性粒细胞减少。
3.感染相关中性粒细胞减少症(infection-related neutropenia)
许多病毒感染可引起暂时性中性粒细胞减少,其机制可能和粒细胞产生减少,重新分布和免疫性破坏有关。病毒性肝炎引起中性粒细胞减少十分常见。其他感染如伤寒、分枝杆菌(特别是结核分枝杆菌)和布鲁菌病、立克次体也可引起中性粒细胞减少。新生儿和老年人发生严重脓毒败血症可引起中性粒细胞减少,其机制和骨髓贮备池中性粒细胞消耗过多或由于补体激活,使边缘池粒细胞增多有关。
4.免疫性中性粒细胞减少症(immune neutropenia)
有4种类型:①新生儿同种免疫性中性粒细胞减少症,由于母亲体内产生针对来自父亲遗传的中性粒细胞特异性抗原的IgG抗体,通过胎盘进入胎儿体内引起,平均7~11周后会自行恢复;②原发性自身免疫性中性粒细胞减少症,见于<4岁的儿童,其IgG抗体是针对粒细胞FcγⅢb受体抗原,导致补体介导粒细胞溶解和脾扣押,95%的患儿可在2年内自发缓解;③继发性自身免疫中性粒细胞减少症,是成人最常见的免疫性中性粒细胞减少症,常继发于系统性红斑狼疮(见于50%病例)、类风湿关节炎(RA)[Felty综合征(Felty syndrome,系RA、脾大、粒缺三联症)]、Sjögren综合征、免疫性甲状腺病、胸腺瘤、T大颗粒淋巴细胞增多症(常伴粒缺)等,中性粒细胞减少机制可因抗粒细胞抗体、细胞介导的破坏及抑制G-CSF抗体;④药物免疫性中性粒细胞减少症。
5.慢性特发性中性粒细胞减少症(chronic idiopathic neutropenia)
是成人慢性中性粒细胞减少的常见原因(约占粒细胞减少病例的34%),无症状,呈良性过程,中性粒细胞绝对值很少低于0.8×10 9 /L,无须治疗。机制不详,有认为和转化生长因子-β(TGF-β)位点的多态性有关。
6.其他
中性粒细胞减少尚见于巨幼细胞贫血、阵发性睡眠性血红蛋白尿、脾功能亢进症、补体激活综合征(边缘池粒细胞增多)及假性粒细胞减少(循环池粒细胞减少,边缘池增多)等。中性粒细胞减少症分类见表16-6-1。
表16-6-1 中性粒细胞减少症分类

注:APLS为X连锁自身免疫性淋巴增生综合征;CMV为巨细胞病毒;CVID为普通变异免疫缺陷症;CLL为慢性淋巴细胞白血病;HBV为乙型肝炎病毒;HCV为丙型肝炎病毒;SLE为系统性红斑狼疮
【临床表现与诊断】
1.临床表现
中性粒细胞减少患者除乏力外并无特殊临床表现。其临床表现主要与原发病和中性粒细胞减少引起的各种感染有关。中性粒细胞减少患者发生感染的概率和中性粒细胞减少的程度和持续时间呈正相关;当中性粒细胞数(×10 9 /L)达<0.1、<0.5、<1.0、<1.5,发生感染的概率分别为53%、36%、20%、9%~10%;并随中性粒细胞减少的程度加重,感染严重度也加重。粒细胞缺乏持续10天,几乎100%有感染,超过1周真菌和特殊病原菌的感染概率就大大提高。严重粒缺患者常起病急骤,突然畏寒、高热、周身不适。肺、泌尿系、口咽部、肛周和皮肤是最常见的感染部位,黏膜可有坏死性溃疡。由于介导炎症反应的粒细胞缺乏,所以感染的局部表现可不明显。如严重的肺炎在胸片上仅见轻微浸润,亦无脓痰;严重的皮肤感染不形成脓液;肾盂肾炎不出现脓尿等。感染极易迅速播散发展为败血症,若不积极救治则病死率甚高。
2.临床特点
要注意中性粒细胞减少症的临床特点,中性粒细胞减少方式是否系暂时性,慢性或周期性。要注意中性粒细胞减少是单纯粒细胞减少或同时伴贫血和血小板减少;分析患者的发病年龄对诊断也有帮助,如无原发病,新生儿粒细胞减少以同种免疫性粒细胞减少症及先天性中性粒细胞减少症最为可能,婴幼儿期以原发性自身免疫性中性粒细胞减少症最为常见,成人慢性中性粒细胞减少以慢性肝病、继发性自身免疫性中性粒细胞减少症及慢性特发性中性粒细胞减少症最为多见;以急性粒细胞缺乏起病,有药物暴露史,病情凶险者以特应性药物性粒细胞缺乏症最为可能。
3.急性中性粒细胞缺乏症
外周血粒细胞数均在0.5×10 9 /L以下,多数<0.1×10 9 /L,分类中粒细胞只占1%~2%甚至更少,粒细胞核呈固缩,胞质中出现空泡及粗大颗粒,淋巴细胞及单核细胞相对增多。骨髓象有两型:①再生障碍型,骨髓增生极度低下,几乎不见各期粒细胞,浆细胞、淋巴细胞及网状细胞增多;②成熟停滞型,骨髓增生尚可,但粒细胞仅见于早幼粒细胞,中幼粒阶段以下几乎不见,而红细胞系及巨核细胞系正常。前者预后比后者更差。当恢复期,外周血粒细胞数增加,有时可超过正常值几倍,甚至出现类白血病反应。
4.诊断思路
对原因不明的慢性粒细胞减少症可依据图16-6-1思路进行诊断。下列实验室检查可明确粒细胞减少的原因:①骨髓粒细胞贮备功能检测:用肾上腺糖皮质激素后可使骨髓粒细胞释放,以了解骨髓贮备粒细胞的量及释放功能。静脉滴注氢化可的松200mg或口服泼尼松40mg,5小时后白细胞计数较用药前增加2×10 9 /L以上者为正常。②粒细胞边缘池功能检测:皮下注射肾上腺素0.2mg,20分钟后白细胞计数较注射前增高2×10 9 /L或较注射前增高1倍以上者,提示粒细胞过多地聚集于血管壁或血窦的内皮细胞上(边缘池)。如无脾大,则可考虑为假性粒细胞减少。③白细胞凝集素或中性粒细胞抗体检测:免疫性粒细胞减少者的粒细胞表面和血清中可测得抗体,但多次输血者或经产妇亦可阳性。④体外骨髓细胞培养:观察CFU-G,可了解干细胞和骨髓基质有无缺陷。
【治疗】
中性粒细胞减少症的治疗原则和方法取决于其病因、中性粒细胞减少的严重度和是否合并有感染性发热。
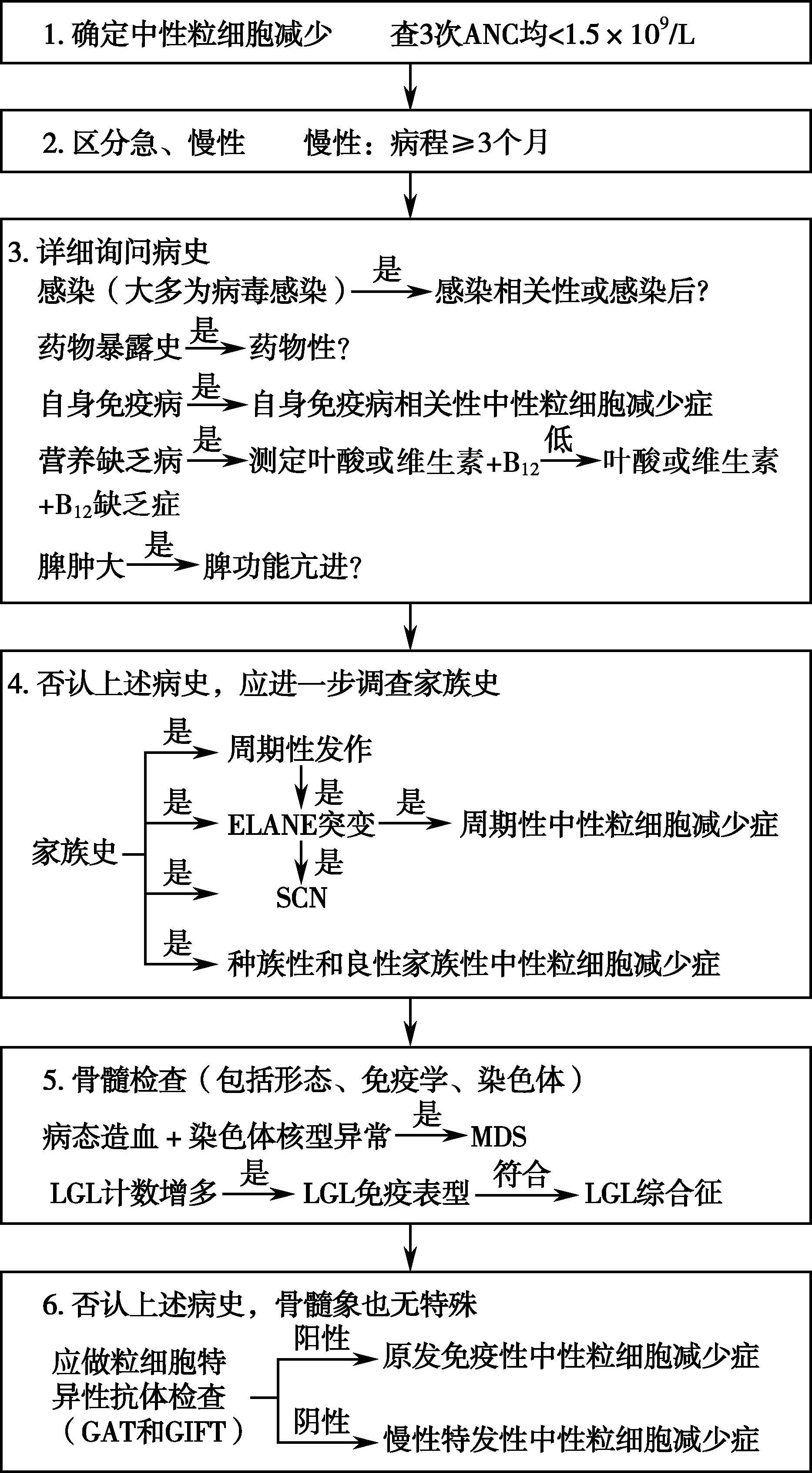
图16-6-1 中性粒细胞减少症诊断步骤流程
ANC:中性粒细胞绝对值;SCN:严重先天性中性粒细胞减少症;MDS:骨髓增生异常综合征;LGL:大颗粒淋巴细胞;GAT:粒细胞凝集试验;GIFT:粒细胞免疫荧光试验
1.急性粒细胞缺乏症伴感染性发热
应视为急重症处理,应立即抽取血、尿等有关标本进行病原微生物培养,按经验性治疗的“广覆盖”原则立即选用抗生素治疗,遇严重感染者应遵循“广谱、高效、足量”原则,选用杀菌剂并静脉给药,不能有丝毫延误。立即选用人重组粒细胞(粒-单核细胞)集落刺激因子[rhG-CSF和rhGM-CSF],rhG-CSF较rhGM-CSF作用强而快,常用剂量为5~10μg/(kg·d),皮下注射,待粒细胞上升到0.5×10 9 /L以上可停用。如合并严重感染而合适抗生素不能控制,rhG-CSF治疗无效者应选用粒细胞输注,每天输注1次,连续3~4天,输注时应加过滤器。
2.粒细胞缺乏症不伴感染性发热
应立即给予住院保护性隔离,最好收住层流病房,常规口腔护理杀菌性漱口液,保持大便柔软而通畅,肛门、外阴部位清洗,保持皮肤清洁,当中性粒细胞<0.2×10 9 /L应预防使用抗生素和抗真菌药。同时按上述方法及时选用rhG-CSF。
3.慢性良性中性粒细胞减少症
除积极寻找粒细胞减少原因外,可选用一般口服促进白细胞增生药(如利血生、脱氧核苷酸、碳酸锂等),但均缺乏肯定疗效,可选用1~2种,每4~6周更换一组,直到有效,若连续数月无效,可不必继续使用。
4.病因治疗
应立即停用可疑药物和毒物的接触,免疫介导的中性粒细胞减少应选用免疫抑制剂治疗,大颗粒淋巴细胞增多症可选用小剂量MTX和CsA治疗。只有积极治疗原发病,中性粒细胞减少才有可能恢复。
5.特殊治疗
异基因骨髓移植适用于先天性中性粒细胞减少症和先天性造血衰竭综合征的治疗,Felty综合征和脾功能亢进可选用脾切除治疗。
主要参考文献
1.林果为,王小钦.免疫性粒细胞减少症的诊断及治疗.中国实用内科杂志,2006,26(4):487-489.
2.Gibson C,Berliner N.How we evaluate and treat neutropenia in adults.Blood,2014,124(8):1251-1258.
3.Palmblad J,Papadaki HA.Chronic idiopathic neutropenias and severe congenital neutropenia.Curr Opin Hematol,2008,15(1):8-14.
4.Goldman L,Schafer AI.Goldman-Cecil Medicine.25th ed.Philadelphia:Elsevier Sauders,2016,1129-1138.
5.Andr
 s E,Zimmer J,Mecili M,et al.Clinical presentation and management of drug-induced agranulocytosis.Expert Rev Hematol,2011,4(2):143-151.
s E,Zimmer J,Mecili M,et al.Clinical presentation and management of drug-induced agranulocytosis.Expert Rev Hematol,2011,4(2):143-151.
6.Mariotti J,Caberlon S,Bertinato E,et al.Primary autoimmune neutropenia in adults:case report and review of the literature.Transfusion,2014,54(11):2906-2910.
第二节
中性粒细胞功能障碍

李 锋
一、概 述
成熟中性粒细胞的完整结构和生化功能保证了其能识别和杀伤病原微生物,成为人体抵御病原微生物侵袭的第一道防线,在保护皮肤、黏膜、呼吸道和胃肠道免受感染中起重要作用。在病原微生物侵入后2~4小时内,中性粒细胞已到达侵入的部位。粒细胞表面的糖蛋白CD11/CD18被炎症介质激活,使粒细胞很容易黏附于血管内皮上。被病原微生物侵袭的组织不断地释放趋化因子,使黏附于血管内皮细胞的粒细胞移出血管壁,定向运动至炎症部位。此时,中性粒细胞吞食被调理素(常为IgG和某些补体成分)覆盖的病原微生物,在中性粒细胞内形成吞噬泡。在吞噬泡内,微生物主要通过中性粒细胞脱颗粒和呼吸爆发激活两种方式被杀死。中性粒细胞脱颗粒时将颗粒内容物释放入吞噬泡内或泡外,这些颗粒内容物包括多种蛋白酶、水解酶、溶菌酶、过氧化物酶、胶原酶、C5裂解酶等。呼吸爆发激活的结果产生过氧化物。多种颗粒内容物和过氧化物一起杀死被吞噬的病原微生物。中性粒细胞的黏附、趋化、吞噬、脱颗粒及杀菌功能中的任何一项缺陷,均可导致粒细胞功能障碍。
中性粒细胞功能障碍(disorders of neutrophil function)性疾病临床上可分遗传性和获得性两组。前者罕见,好发于婴幼儿,系基因突变引起中性粒细胞功能障碍;后者常见,好发于成人,常继发于全身性疾病,由于随病因的控制粒细胞功能可获得改善,加上粒细胞功能检验临床开展较少,因而后者常不易被觉察。中性粒细胞功能障碍虽然种类繁多,但其主要的临床表现相似,即反复发生严重的细菌感染。亦常伴有中性粒细胞减少、免疫球蛋白或补体的异常。中性粒细胞功能异常的筛选试验主要有:①血涂片观察中性粒细胞的形态;②Rebuck皮窗试验:观察粒细胞的趋化和移动功能;③四唑氮蓝还原试验(NBT):检测粒细胞的吞噬功能和呼吸爆发产生过氧化物的活力;④特殊染色:检查中性粒细胞内的髓过氧化物酶、碱性磷酸酶等;⑤流式细胞术检测外周血中性粒细胞膜表面CD11、CD18或CD15受体的表达,观察粒细胞的黏附功能。
二、遗传性中性粒细胞功能障碍
(一)中性粒细胞颗粒功能缺陷
脱颗粒作用是中性粒细胞杀菌主要机制之一,颗粒内含多种抗微生物蛋白。嗜天青颗粒含水解酶、杀菌肽及髓过氧化物酶;特异性颗粒含胶原酶和乳铁蛋白。中性粒细胞颗粒功能缺陷可直接影响其杀菌作用。
1.Ch
 iak-Higashi综合征(Ch
iak-Higashi综合征(Ch
 diak-Higashi syndrome,CHS
diak-Higashi syndrome,CHS
是一种罕见的常染色体隐性遗传性疾病,系 LYST 基因突变(该基因编码溶酶体运输调节蛋白)导致中性粒细胞膜改变,胞质内出现巨大畸形和功能异常的溶酶体颗粒,在瑞氏染色的血片中很易发现。这类异常不仅限于中性粒细胞,在其他细胞内也可存在。中性粒细胞的趋化及杀菌作用下降,患者易发生感染。患者还可有轻度出血倾向、眼和毛发及皮肤局部白化、进展性周围神经病变等。CHS还常合并自然杀伤细胞功能缺陷和中性粒细胞数量减少,这更加重了患者的免疫缺损。患者能在一生中任何时候发生疾病加速,出现淋巴瘤样病变,肝、脾和骨髓内多克隆T淋巴细胞增殖,在没有细菌性脓毒症的情况下出现肝脾大和高热,全血细胞减少加重。本征的处理主要是防治感染,预防性用药难以奏效。维生素C口服0.5~1.0g/d,对部分患者可有帮助。有合适供者时可进行异基因造血干细胞移植。发生淋巴瘤样疾病时,可试用大剂量甲泼尼龙治疗后切除脾。
2.先天性特异颗粒缺乏(congenital specific granule dificiency,CSGD)
是一种非常罕见的常染色体隐性遗传性疾病。中性粒细胞趋化性缺陷,难以迁移至炎症部位。CSGD的中性粒细胞在电镜下可见嗜天青颗粒正常,而特异性颗粒稀少或阙如。细胞核分叶异常,常呈两叶,似Pelger-Huёt畸形。白细胞碱性磷酸酶活力减弱。与颗粒相关的蛋白质也缺乏,杀菌能力受损。患者易发生各种常见病原菌引起的反复、严重感染。皮肤和皮下组织感染常见,且可引起瘢痕和毁形。鼻窦炎、支气管炎和肺炎也常见。为预防感染,可长期服用复方SMZ或双氯苯甲异
 唑青霉素。异基因粒细胞输注可用于非常严重的感染者。
唑青霉素。异基因粒细胞输注可用于非常严重的感染者。
(二)中性粒细胞杀菌作用缺陷
中性粒细胞有两种杀菌机制:①脱颗粒作用与非氧化型杀菌,随着中性粒细胞吞食细菌后,中性粒细胞的颗粒移位并与质膜内陷形成吞噬泡,进而与溶酶体融合形成吞噬体,颗粒中各种抗菌蛋白水解酶随即释放出来,此过程称脱颗粒作用;②氧依赖性杀菌机制,主要通过NADPH氧化酶的激活,利用氧大量生成活性氧物质(ROS),ROS有杀菌效应,又称呼吸爆发作用。遗传性中性粒细胞杀菌作用缺陷见于慢性肉芽肿病,髓过氧化物酶缺乏症、G6PD缺乏症、谷胱甘肽还原酶和谷胱甘肽合酶缺乏症。
1.遗传性髓过氧化物酶缺乏
髓过氧化物酶(MPO)存在于中性粒细胞和单核细胞内的嗜天青颗粒中。 MPO 基因突变引起的MPO缺乏是最常见的遗传性中性粒细胞功能缺陷,它以常染色体隐性遗传方式传递。有报道其发病率可达1/4000。MPO缺乏的中性粒细胞吞噬细菌和真菌的功能正常,其烟酰胺腺嘌呤磷酸二核苷酸(NADPH)氧化酶活性并不受累。因此,患者发生感染的机会并不增加,亦常无其他临床表现。由于H 2 O 2 杀死微生物的作用有所降低,当糖尿病患者或其他免疫功能缺陷者合并本症时,会发生内脏念珠菌感染和其他细菌的反复感染。本症患者大多是在做血细胞MPO染色时偶然被发现,亦可用分光光度计来定量测定。患者一般无须治疗。
2.慢性肉芽肿病
慢性肉芽肿病(chronic granulomatous disease,CGS)是一组吞噬细胞不能表现出呼吸爆发的遗传性疾病。大约2/3的患者为X连锁隐性遗传病,由编码NADPH氧化酶膜结合亚单位的糖蛋白91吞噬细胞氧化酶基因(glucoprotein 91 phagocyte oxidase gene,gp91 phox gene)突变引起。其余1/3左右患者为常染色体隐性遗传,由NADPH 氧化酶胞质组成部分P47 phox (25%)、P67 phox (5%)或小的膜结合亚单位P22 phox (5%)基因缺陷所致。
诊断本病的初筛试验有细菌杀伤实验和四氮唑蓝还原试验,确诊需用抗NADPH氧化酶不同亚单位的单克隆抗体做Western blot法检测。如果Western blot检测各亚单位蛋白表达水平均正常但呼吸爆发功能异常,表明蛋白质功能存在异常。有缺陷的吞噬细胞可以正常处理许多细菌(肺炎链球菌、链球菌),但其不能产生足够的过氧化氢,因而对主要依赖吞噬细胞氧化产物杀灭的细菌(金黄色葡萄球菌、假单胞菌属、白念珠菌和曲霉菌等)则不能有效地处理。患者自婴幼儿期即可出现反复、严重、难以治疗和恢复的多种细菌感染,病灶部位有微脓肿和肉芽肿形成。往往在10岁或20岁前死亡。大量新型抗菌药物的应用使CGS的治疗结果有一定的改善,但最终难免死于不能控制的感染及合并症(特别是曲霉菌)。对CGS患者应长期使用抗菌药物预防感染,可选用复方SMZ。急性感染时应用足量的抗菌药物。白细胞输注可能有帮助。γ干扰素可能有助于某些患者杀菌功能的改善。异基因造血干细胞移植可作为最后的治疗手段。极严重的G-6-PD缺乏症患者中性粒细胞也不能表现足够的呼吸爆发,亦可有类似CGS的临床表现。
(三)中性粒细胞趋化性缺陷
当中性粒细胞自血管内皮层游出,进入组织后即暴露在趋化物质的浓度梯度中,开始趋化运动。趋化因子与中性粒细胞受体结合引起中性粒细胞形态变化,使中性粒细胞极化,通过伸缩的伪足爬向感染源,准备捕捉病原体。趋化性缺陷可直接影响中性粒细胞的运动。遗传性中性粒细胞趋化性缺陷十分罕见。如高免疫球蛋白E综合征(hyperimmunoglobulin E syndrome)又称Jobe综合征(Jobe syndrome),为常染色体显性遗传,最常见的类型是由于 STAT3 基因突变,引起细胞因子信号传导异常,导致粒细胞趋化功能障碍。表现为中性粒细胞活动性降低伴有反复皮肤和肺部感染,血清IgE水平显著升高。皮肤感染的显著特点是没有周围红、热、痛的“冷脓肿”。
(四)中性粒细胞黏附缺陷
中性粒细胞与内皮细胞的黏附作用分别是由中性粒细胞表面的黏附分子和内皮细胞表面的黏附分子共同作用的结果。中性粒细胞黏附性增加的分子基础是整合蛋白β 2 亚族的CD11/CD18在趋化因子作用下表达增加并被激活。内皮细胞上的黏附分子主要是免疫球蛋白超家族的ICAM-1和VCAM-1及E-选择素,它们被细胞因子或细菌产物内毒素等激活,通过配体-受体反应相互识别发生相互黏附作用。中性粒细胞黏附缺陷导致中性粒细胞在循环中积蓄,而感染灶处粒细胞却很少。遗传性白细胞黏附缺陷症(leukocyte adhesion deficiency,LAD)是一组常染色体隐性遗传性疾病。发病率约为百万分之一。因为黏附分子表达缺失,中性粒细胞无法牢固地黏附在炎症部位的内皮表面并进行跨内皮细胞迁移所致。临床特征为反复软组织感染,创伤愈合延迟,感染部位炎症反应不明显,局部没有红、肿和脓液形成。严重者在胎儿或幼儿期即发生顽固的“隐匿的”皮肤、口腔、呼吸道、肠道和泌尿道细菌感染,脐带脱落延迟伴脐炎。难以到达感染部位的中性粒细胞在循环血液中明显增多(可高达100×10 9 /L),易被误诊为类白血病反应。临床上有三型:①LAD-Ⅰ型是由于编码CD18的基因突变引起CD11/CD18缺乏;②LAD-Ⅱ型是LAD-Ⅰ的变异型,是由于基因缺陷导致CD15s表达缺乏;③LAD-Ⅲ型系由于白细胞上三种β 2 整合素缺陷引起。可用单克隆抗体标记流式细胞仪直接检测中性粒细胞和淋巴细胞膜表面黏附蛋白CD11/CD18,如无CD11/CD18表达即可作出诊断。有的患者仅部分中性粒细胞上可测得CD11/CD18,亦有患者CD11/CD18表达正常,但其功能异常,中性粒细胞不能稳定地黏附于血管内皮细胞及移行。约3/4以上的患儿在10岁以前死亡。因而,对CD11/CD18完全缺乏者应争取及早进行异基因造血干细胞移植。基因替代治疗被认为很有希望,但尚在研究中。
此外,中性粒细胞肌动蛋白功能不良也是因基因缺陷影响中性粒细胞黏附功能,细胞不能形成伪足发生趋化和吞噬反应。出生后即反复发生感染,但不会化脓。异基因造血干细胞移植有效。
三、获得性中性粒细胞功能障碍
疾病、应激、药物或某些治疗可直接或通过免疫异常间接影响中性粒细胞的功能,造成获得性中性粒细胞功能障碍。获得性中性粒细胞功能缺陷患者易发生反复的化脓性感染,而中性粒细胞被过度激活也会造成组织损伤,促使病情恶化。多种血液系统恶性疾病,包括急、慢性白血病、骨髓增殖症、骨髓增生异常综合征、多发性骨髓瘤和淋巴瘤等,均有不同程度的中性粒细胞功能缺陷。糖尿病和肾衰竭患者中性粒细胞的趋化、黏附、吞噬和杀菌功能均有受损。特别是病情未被适当控制的患者,发生感染的可能性明显增加。中性粒细胞的激活在糖尿病血管并发症的发生发展中亦起一定的作用。类风湿关节炎和系统性红斑狼疮患者体内的免疫复合物可与中性粒细胞表面的Fc受体结合,引起其趋化功能受损。肝硬化、麻风和结节病患者的粒细胞趋化功能降低。缺铁和营养不良者中性粒细胞的杀菌功能明显减弱。G - 细菌败血症、胰腺炎、严重创伤、血液透析及人工心肺机的应用等,均可诱发补体C5活化(C5a)和肿瘤坏死因子(TNF)的生成增加,使中性粒细胞过度激活,这些过度激活的中性粒细胞由于活动能力减弱,常黏附于基质,造成炎症部位的大量积聚。与此同时,它们还可以释放一些蛋白酶和有毒物质,诱导产生多种细胞因子,使组织损伤进一步加重。如在肺毛细血管床内过多聚集,严重时可引起急性呼吸窘迫综合征(ARDS)。许多药物可抑制或增强中性粒细胞的功能。秋水仙素、非甾体抗炎药、抗疟药、糖皮质激素、肾上腺素和酒精等,均可使粒细胞的一项或多项功能受损。肾上腺素能直接引起血管内皮细胞释放cAMP,使粒细胞的黏附能力减弱,而从边缘池迅速释放至循环池,血液中粒细胞显著增多。糖皮质激素和酒精亦可使粒细胞的活动和吞噬功能受损。众多的抗菌药物,对粒细胞的功能亦有不同程度的抑制或增强作用。获得性中性粒细胞功能障碍的处理以治疗原发疾病为主。
四、遗传性中性粒细胞形态异常
如遗传性 Pelger-Huёt 畸形(中性粒细胞核分叶异常,多为双叶核,为常染色体显性遗传性疾病)、Alder-Reilly异常(中性粒细胞内出现紫黑色粗大颗粒的Alder-Reilly小体,为常染色体隐性遗传)。Jordan异常(家族性白细胞内出现多个空泡)等。它们均有粒细胞形态改变,但多不引起临床症状,其粒细胞功能基本正常。
主要参考文献
1.Greer JP,Foerster J,Rodgers GM,et al.Wintrobe's Clini-cal Hematology.12th ed.Philadelphia:Williams&Wilkins,2009,1553-1559.
2.Laurence A,Boxer.Neutrophil disorder:qualitative abnormalities of the neutrophil//Beutler E,Lichtmad MA.Williams Hematology.6th ed.New York:McGraw Hill,2001,835-854.
3.Newburger PE.Disorders of neutrophil number and func-tion.Hematology Am Soc Hematol Educ Program,2006,104-110.
4.Goldman L,Schafer AI.Goldman-Cecil Medincine.25th ed.Philadelphia:Elsevier Saunders,2016,1142-1151.
第三节
噬血细胞综合征

陈 彤
噬血细胞综合征(hemophagocytic syndrome,HS),又称噬血细胞淋巴组织细胞增生症(hemophagocytic lymphohistiocytosis,HLH),于1939年最早报道,是由遗传性或获得性因素引起免疫紊乱,进而导致活化的淋巴细胞和组织细胞增生、以及组织器官非可控性高炎性反应的一组综合征。部分HS与染色体缺陷有关,属原发性(家族性);非遗传性HLH常继发于感染、恶性肿瘤和自身免疫疾病。近年来,HLH的发病率明显上升,每30万出生婴儿中约有1~225个,且有地域差异。半数以上的继发性HLH与恶性肿瘤相关(52%),感染次之(34%),免疫紊乱和原发性HLH分别占8%和6%。HLH可以表现为某一因素触发,但随着疾病进展,其他因素叠加可加重病情恶化。
【临床类型】
(一)原发性(家族性)噬血细胞综合征(family hemophagocytic syndrome)
为常染色体或性染色体隐性遗传性疾病,可分为家族性噬血细胞综合征和伴发于某些原发性免疫缺陷病。家族性HLH(FHLF)常表现为 PRF1 、 UNC13D ( MUNC13-4 )、 STX11 、 STXBP2 ( MUNC18-2 )等基因的纯合突变,分别与FHLH2-FHLH5亚型有关。FHLH1亚型的基因突变现已知位于9q21。患有先天性免疫缺陷的患者亦可因免疫相关的基因突变而伴发HLH,如 LYST (Chediak-Higashi综合征)、 AP3B1 (Hermansky-Pudlak综合征,Ⅱ型)、 RAB27A (Griscelli综合征,Ⅱ型)、 SH2D1A (X连锁淋巴增殖性疾病,Ⅰ型)、 BIRC4 / XIAP (X连锁淋巴增殖性疾病,Ⅱ型)、 IL2RG (X连锁重症免疫缺陷)、IL-2诱导T细胞激酶( ITK )等。
(二)继发性(反应性)噬血细胞综合征(secondary hemophagocytic syndrome)
该型 HLH无遗传学异常,儿童或成人均可发病,常伴发于免疫缺陷或潜在的感染、恶性肿瘤和自身免疫病。
1.感染相关噬血细胞综合征(infection-induced hemophagocytic syndrome)
与病毒、细菌、真菌和寄生虫感染有关,某些原发性(家族性)噬血细胞综合征也可由感染诱发。儿童多见,患者常在轻度病毒血症2~6周后突然出现明显的全身症状,多发生于有免疫缺陷的患者。
2.恶性肿瘤相关噬血细胞综合征(malignancy-induced hemophagocytic syndrome)
见于急性白血病、淋巴瘤、多发性骨髓瘤、胚细胞肿瘤、胸腺瘤、胃癌等,但以非霍奇金淋巴瘤和急性白血病最常见。间变性大细胞淋巴瘤合并噬血细胞综合征以往常误诊为恶性组织细胞病。可与感染伴发。
3.伴发于自身免疫病的巨噬细胞活化综合征(macrophage activation syndrome)
也是一种继发性噬血细胞综合征,见于幼年类风湿关节炎、成人Still病和红斑狼疮(SLE)等。
【临床与实验室特征】
1.典型的临床表现
起病急骤,进行性加重,高热、寒战、关节肌肉酸痛,肝、脾、淋巴结肿大,黄疸及中枢神经系统症状。
2.血细胞减少
外周血细胞减少,可一系、两系或三系血细胞减少。
3.肝功能异常
血清转氨酶、胆红素可增高,甘油三酯、LDH、铁蛋白(SF)增高,糖化铁蛋白百分比降低,LDH可超过1000U/L,SF可>1000μg/L。
4.凝血障碍
凝血酶原时间延长,血浆纤维蛋白原减低,纤维蛋白降解产物增多。尤以血浆纤维蛋白原降低甚为突出,甚至可<1g/L。
5.免疫学检查异常
多数病例示周围血液或骨髓T细胞增多,CD8 + 细胞比例增高,CD4 + 和CD8 + 细胞比值异常。疾病活动期血清IFN-γ水平和IFN-α水平增高,IL-10浓度也多增高,血浆巨噬细胞炎症蛋白(MIP)-1α增高,NK细胞活性降低或缺乏,血浆可溶性CD25(可溶性IL-2受体)升高,可≥2400U/ml。
6.骨髓、脾、脑脊液或淋巴结细胞形态学或病理学检查
骨髓涂片示增生减低,组织细胞显著增生,可有明显的吞噬血细胞现象,称噬血细胞,每个组织细胞吞噬血细胞的数量少则2~3个,多则10多个,可为红细胞,也可为有核细胞。
【诊断与鉴别诊断】
国内尚无统一的诊断标准,国外组织细胞协会2004年修订的诊断标准,凡有HLH相关分子生物学异常或符合以下8条标准中5条即可以诊断(表16-6-2)。依据骨髓涂片发现噬血细胞诊断本症的灵敏度不高,常需要连续多次骨髓穿刺或骨髓活检以提高阳性率,有主张将噬血细胞数量定为≥2%(占骨髓有核细胞),≥5%(占组织细胞),但必须注意人为因素混淆。
本症须与恶性组织细胞病(简称恶组)相鉴别,恶组可见异常组织细胞、多核巨组织细胞浸润,其组织细胞的吞噬现象不及本症明显,且恶组淋巴结病变是沿窦状隙向实质侵犯,此与本症有所不同。
表16-6-2 HLH 诊断标准

【治疗】
治疗的目标除治疗原发病外,应尽快抑制危及生命的过度的炎症反应。可选择地塞米松等肾上腺皮质激素;环孢素(CsA)可抑制T细胞活化;静脉用大剂量免疫球蛋白对病毒相关噬血细胞综合征有特殊作用;依托泊苷(VP-16)在单核细胞和组织细胞有很高的活性,对抑制组织细胞有明显疗效,宜及早使用。具体用法可参考HLH-2004方案:①初始治疗(第1~8周),包括地塞米松10mg/(m 2 ·d)共2周,依次5 mg/(m 2 ·d)共2周,2.5mg/(m 2 ·d)共2周及1.25 mg/(m 2 ·d)共1周,逐渐减停;依托泊苷150mg/m 2 静脉滴注,第1、2周每周2次,第3~8周每周1次;环孢素6mg/(kg·d)口服。如有神经系统症状,则在第3、4、5、6周各加用1次鞘内注射 MTX联合地塞米松。②继续治疗(第9~40周),地塞米松10mg/(m 2 ·d)共3天,隔周1次;依托泊苷150mg/m 2 静脉滴注,隔周1次;环孢素用法同前。③后续治疗(第40周后),仅用地塞米松和环孢素。HLH的诊断和治疗流程见图16-6-2。
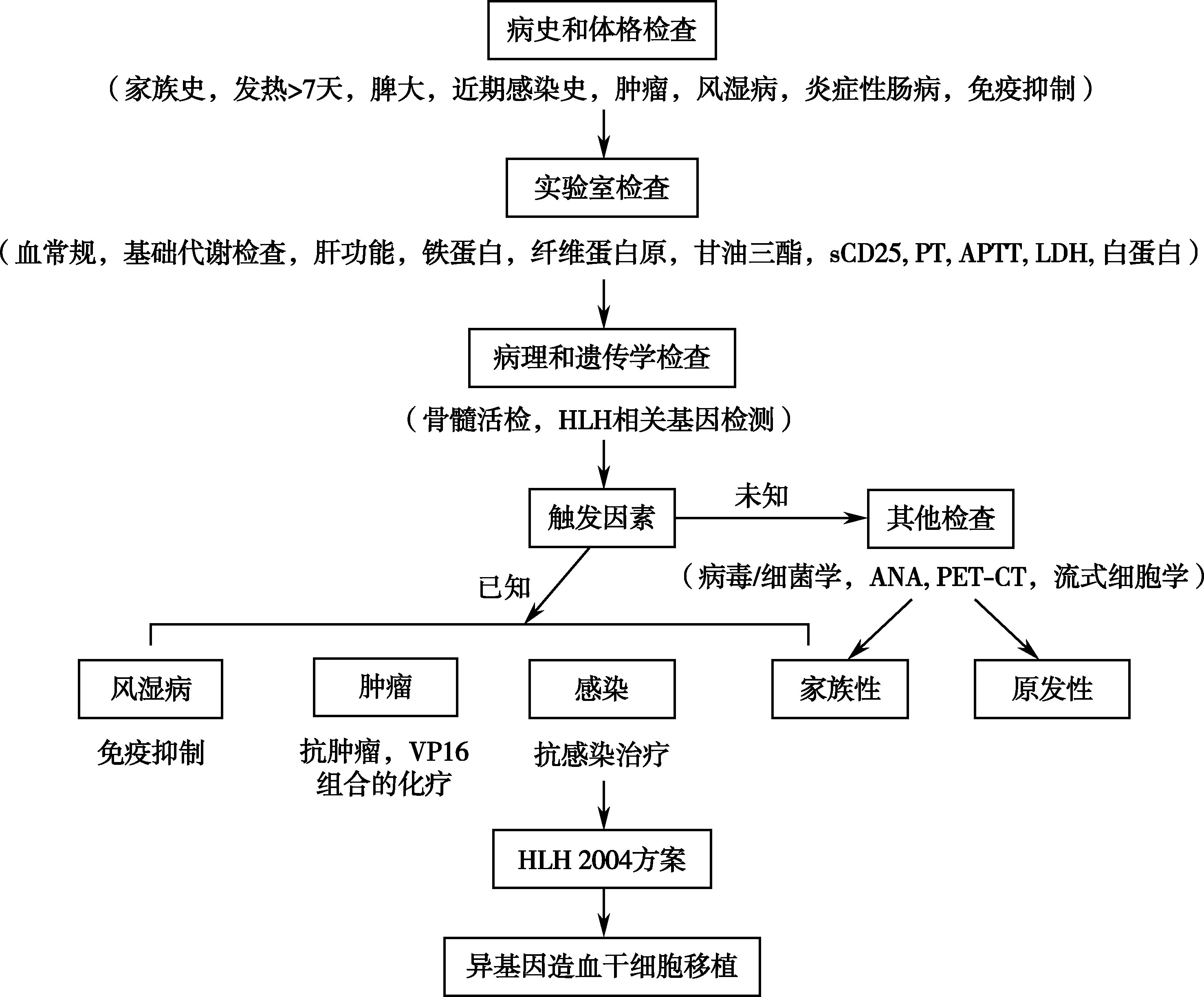
图16-6-2 成人HLH诊断和治疗流程
主要参考文献
1.Henter J,Horne AC,Arico M,et al.HLH-2004:Diagnostic and Therapeutic Guidelines for Hemophagocytic Lymphohistiocytosis.Pediatr Blood Cancer,2007,48:124-131.
2.Schram AM and Berliner N.How I treat hemophagocytic lymphohistiocytosis in the adult patient.Blood,2015,125(19):2908-2914.
第四节
朗格汉斯细胞组织细胞增生症

王宏胜
朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH),是一组以免疫表型和功能不成熟的朗格汉斯细胞克隆性增殖为特征的疾患,旧称组织细胞增生症X(histiocytosis X),包括嗜酸性肉芽肿(eosinophilic granulomas)、汉-薛-柯综合征(Hand-Schüller-Christan Syndrome)和莱特勒-西韦病(Letterer Siwe disease)。
【病因与发病机制】
病因尚不明确,可能是类似于表皮朗格汉斯细胞(LCs)的LCH细胞克隆性增殖。正常情况下,LCs是naïve T淋巴细胞主要抗原递呈细胞,LCH病灶部位LCs是一类不完全成熟的树突状细胞(DCs),其细胞具有一定的迁徙能力,与正常DC相比,细胞增殖能力强而抗原递呈作用弱。某些特定细胞因子的持续高水平如白介素-10和转化生长因子-β与这些LCs功能和表型发育不成熟有关。但LCH是反应性疾病还是恶性疾病仍有争论。最近发现约60%的LCH活检标本中存在 BRAF 基因V600E突变,倾向LCH是一种克隆性肿瘤疾病。
【临床表现】
临床表现极为多样,从单纯骨质破坏到多器官病变。骨骼病变约见于70%~80%患者。以颅骨、长骨、脊柱和扁平骨受累最多。可表现为骨缺损、痛性肿胀、突眼和乳突炎导致顽固性中耳炎(耳流脓)及牙齿松动脱落等。皮疹约见于30%~50%患者。多少不一,成批出现,主要分布于躯干、头皮、发际和颈部,为淡红色粟米大小斑丘疹,中央可结痂脱屑,也可为出血性、湿疹样或脂溢性皮炎样。肺部病变、肝脾及淋巴结肿大、骨髓受累各约见于30%患者。肺部受累,轻者表现为咳嗽,重者出现呼吸急促、呼吸困难,甚至气胸。肝脏受累患者会出现黄疸和水肿等。骨髓受累者可出现苍白和出血等表现。肠道病变可表现为腹泻,垂体或下丘脑受累可导致生长发育落后和中枢性尿崩症的表现。一般而言,年龄越小患儿临床表现越重,发热、消瘦等全身症状明显,年长儿多临床表现较轻,常以骨质破坏为唯一表现。孤立的肺部病变几乎仅见于青年,特别是吸烟者。肝、脾或骨髓受累时,患者死亡风险增加,故肝、脾和骨髓被认为是LCH的危险器官(RO)。
【辅助检查】
骨质破坏X线检查多呈现典型的“穿凿样”溶骨性改变,颅骨缺损呈地图样;脊椎病变呈扁平椎,椎间隙正常或增宽;长骨缺损多呈囊状;颌骨破坏可出现漂浮齿。LCH的骨质破坏,放射性核素检查的敏感性不如X线片检查,但可能对小婴儿较好。肺部受累在胸部X线上表现为广泛间质改变,可呈弥漫网状或点状阴影或蜂窝样、粟粒样病变,晚期可出现多发囊肿、大泡和广泛纤维化;肺部受累患者需行胸部高分辨CT检查。头颅CT有助于了解脑部病变尤其是蝶鞍部病变,MRI检查对了解伴尿崩症患者下丘垂体系统病变十分有用。骨髓受累时,血常规可以呈现全血细胞减少表现,骨髓涂片可见LC细胞,严重病例可出现噬血现象。B超检查可发现部分患者肝脾、淋巴结肿大。肝脏受累时除肝脏肿大外还可有肝功能异常、黄疸和低蛋白血症等。PET/CT扫描也是评估治疗反应的有效手段,但目前国内开展少。病变部位活检有助于明确诊断。新鲜皮疹印片可见大量组织细胞,皮肤、肝、肺和软组织包块活检病理检查,常规切片光镜下可见LC细胞,电镜下可见Birbeck颗粒,组织免疫组化染色见到CD1a、S100和朗格素(langerin)即CD207(即电镜下之Birbeck颗粒)阳性。
【诊断】
需要依靠临床表现、影像学及实验室检查。确诊依赖于病理诊断。受累组织免疫组化染色见到CD1a和(或)朗格素阳性的组织细胞是诊断LCH的“金标准”。以往的一些诊断指标,如皮疹印片中找到形态正常的网状细胞或组织切片中S-100蛋白、α-D甘露糖酶和花生凝集素阳性等已不能作为确诊指标。
【分组】
(一)根据患者受累器官/系统分组
1.单系统LCH(SS-LCH)
包括单个器官或系统受累(单系统单部位或多部位),如皮肤、骨骼、胸腺、淋巴结、垂体、甲状腺等。
2.多系统LCH(MS-LCH)
指出现包括骨骼、消化系统(肝、脾)、肺、骨髓、内分泌系统、眼、中枢神经系统、皮肤、淋巴结在内的两个或以上器官系统受累。
(二)根据有无危险器官分组
1.低危组
即无RO受累组,无肝、脾或骨髓危险脏器病变。
2.高危组
即RO受累组,一个或多个危险脏器受累,死亡率高。
【治疗】
治疗LCH的方法包括手术、放射治疗或化疗,应根据病变部位和疾病程度进行选择。单纯皮肤受累可以临床观察,如皮疹广泛、疼痛、溃疡或出血可予局部类固醇激素治疗,或口服化疗(如甲氨蝶呤)。单一部位骨骼损害可以手术时予以手术刮除。某些椎体及股骨颈病变由于存在瘫痪风险,应进行系统化疗,并可尝试低剂量放疗缓解病变。颅面骨如乳突、颞骨或眼眶病变时引起中枢性尿崩症概率较大,称为“中枢神经系统危险”部位,建议进行系统性化疗。高危组和低危组多系统病变患者应进行联合化疗。国际组织细胞协会LCH-Ⅰ/Ⅱ/Ⅲ系列治疗方案、由德国等欧洲国家参加的DAL HX-83/90系列治疗方案以及日本LCH协作组JLSG-96/02系列治疗方案均是国际上比较知名的治疗LCH的多中心研究。
(一)一线治疗
目前国内多使用国际组织细胞协会根据LCH-Ⅲ临床研究的结果于2009年4月发布的LCH评估与治疗指南进行联合化疗,具体如下:
1.初始治疗1(6周):
长春碱(VBL)6mg/m 2 ,静脉注射,每周1次;泼尼松(PRED)40mg/(m 2 ·d),口服,4周后减停2周。
治疗6周后评估,无RO受累患者病变没有改善或RO受累患者对初始治疗有效者,进行第2疗程VBL和PRED,即初始治疗2。完全缓解者进入维持治疗。
2.初始治疗2(6周)
VBL 6mg/m 2 ,静脉注射,每周1次;PRED 40mg/(m 2 ·d),每周口服3天。
6~12周初始治疗后完全缓解的患者进行维持治疗。12周后仍无效者即转入其他二线治疗挽救方案。
3.维持治疗
VBL 6mg/m 2 ,静脉注射,每3周1次;PRED 40mg/(m 2 ·d),每3周口服5天。多系统病变患者加用6-巯基嘌呤(6 MP)50mg/(m 2 ·d),每晚1次,口服。总疗程至12个月。
体重<10kg的婴儿,药物剂量按年龄调整:小于6个月者按体表面积的50%计算;6~12个月按体表面积的75%计算;>12个月按体表面积的100%计算。
诊断时有RO受累或诊断时未发现RO受累,但治疗时发展成RO病变的患者可直接进行备选挽救方案治疗。
(二)二线治疗
病变持续或复发的LCH病例,现今临床没有最佳的治疗方案。无RO受累者可使用包括病灶内注射类固醇激素;联合VBL、PRED和阿糖胞苷(Ara-C)化疗或单用克拉屈滨(2-CDA)化疗。RO受累者克拉屈滨和Ara-C联合化疗以及减低剂量预处理方案后异基因造血干细胞移植(RIC-SCT)挽救治疗有一定疗效。
(三)中枢神经系统病变的治疗
中枢神经系统病变患者应根据疾病的类型和程度及以往接受过治疗的情况,进行个体化治疗,选用可透过血脑屏障的药物,克拉屈滨或其他核苷类似物,Ara-C可能有效。
(四)支持治疗
化疗期间及化疗结束后3个月内口服复方磺胺甲
 唑预防卡氏肺囊虫肺炎。化疗后骨髓抑制时予以输注红细胞、血小板等支持。持续粒细胞缺乏者,予粒细胞集落刺激因子(G-CSF)支持。尿崩症一旦发生,较难逆转,可用1-脱氨基-8D-精氨酸加压素(DDAVP)治疗。因生长激素缺乏而引起的生长发育落后可用生长激素治疗。
唑预防卡氏肺囊虫肺炎。化疗后骨髓抑制时予以输注红细胞、血小板等支持。持续粒细胞缺乏者,予粒细胞集落刺激因子(G-CSF)支持。尿崩症一旦发生,较难逆转,可用1-脱氨基-8D-精氨酸加压素(DDAVP)治疗。因生长激素缺乏而引起的生长发育落后可用生长激素治疗。
【预后】
LCH-Ⅲ研究总生存率为84%,预后与疾病的程度、危险器官受累和对初始治疗的反应密切相关。单系统或骨/皮肤病变通常均能存活。治疗6周反应不佳者,死亡率可高达35%。新生儿和小年龄儿童伴有危险器官受累者生存率低。LCH患者最常见的后遗症有骨骼畸形、尿崩症和神经退行性病变等。多系统病变患者的慢性并发症有肺纤维化、肝纤维化、听力损失、骨骼畸形、身材矮小、永久性共济失调、神经认知缺陷和牙列不齐。肝脏病变可能会导致硬化性胆管炎,除肝移植外对其他治疗反应差。
主要参考文献
1.Badalian-Very G,Vergilio JA,Fleming M,et al.Pathogenesis of Langerhans cell histiocytosis.Annu Rev Pathol,2013,8:1-20.
2.Gadner H,Grois N,Pötschger U,et al.Improved outcome in multisystem Langerhans cell histiocytosis is associated with therapy intensification.Blood,2008,111(5):2556-2562.
3.Minkov M,Grois N,McClain K,et al.Langerhans cell histiocytosis:Histiocyte Society evaluation and treatment guidelines.2009.http://www.histiocytesociety.org/document.doc?id=290.
4.Allen CE,Ladisch S,McClain KL.How I treat Langerhans cell histiocytosis.Blood,2015,126(1):26-35.
第五节
恶性组织细胞病

林果为
恶性组织细胞病(malignant histiocytosis)简称恶组,1939年由Scott及Robb-Smith首次报告定名为“组织细胞髓性网状细胞增生症”,1966年Rappaport改为恶性组织细胞病。国内于20世纪50年代开始报道本病,初定名为“恶性网状细胞病”,70年代改为恶组。近年来随着免疫学、细胞遗传学和分子生物学的进展,对恶组肿瘤细胞来源提出了异议,认为过去诊断的恶组极大多数病例实为间变性大细胞淋巴瘤,仅有极少病例肿瘤细胞确有组织细胞标记,而认为存在真性恶组。因此目前临床诊断恶组必须十分慎重,确定本病前应认真排除反应性组织细胞增多症、噬血细胞综合征(特别是淋巴瘤相关性噬血细胞综合征)、间变性大细胞淋巴瘤。WHO分类已无此疾病名称,而将具有多器官累及的恶组归入组织细胞肉瘤(histiocytic sarcoma)。
本病可见于任何年龄,以15~40岁占多数(68.4%),男女之比约为3∶1,起病急骤,病程短促、凶险。常以不明原因发热为首发症状,多为持续高热,也有不规则热、弛张热、间歇热。大多数患者有全血细胞减少,呈进行性贫血、粒细胞缺乏、出血及各种继发性感染。肝、脾、淋巴结肿大,后期出现黄疸,其他非造血器官均可累及,如肺、消化道、心、肾、浆膜腔、皮肤等。由于病灶散在呈多发性、不均匀和不规则性,故临床表现多种多样,缺乏特异性,极易误诊。
骨髓涂片可找到多少不一的各种异常组织细胞,其中具有诊断价值:①异形组织细胞:细胞体积大,可达20~40μm,形状畸异,核卵圆或不规则,核膜较厚而清晰,核染色质粗网状,核仁隐显不一,常较大,胞质丰富嗜碱性,常见空泡,亦可见细的嗜苯胺蓝颗粒;②多核巨组织细胞:体积甚大,达50μm以上,外形不规则,胞质浅蓝,无颗粒或仅有少数细颗粒,通常含3~6个或多叶核,核仁隐显不一。吞噬型、淋巴样和单核样组织细胞也见于其他疾病,因此没有特异诊断价值。由于骨髓受累程度不一,病灶分布不均匀,宜反复多部位穿刺。受累组织的病理切片也可见各种异常组织细胞浸润,呈多样性,成灶性或片状分布,极少形成团块,组织结构可部分或全部破坏,有助于诊断。
确定真性恶组的关键在于发现的异常组织细胞至少具有一种以上组织细胞标记(包括CD163,CD68及溶菌酶),而缺乏特异性T、B、朗格汉斯细胞,滤泡树突状细胞及髓系细胞标记。
恶组的化疗方案与非霍奇金淋巴瘤相仿。可选用:CHOP(环磷酰胺、阿霉素、长春新碱、泼尼松),BCHOP(上述方案加博来霉素)、BCHOP加大剂量甲氨蝶呤或依托泊苷与阿糖胞苷联用。国内郁知非等报道应用米托蒽醌、环磷酰胺、洛莫司汀、长春新碱和泼尼松联合化疗取得较好疗效。有报道应用同种异基因骨髓移植治疗取得满意疗效。
主要参考文献
1.张之南,沈悌.血液病诊断及疗效标准.第3版.北京:科学出版社,2007,245-248.
2.Schmidt D.Malignant histiocytosis.Curr Opin Hematol,2001,8:1-4.
第六节
溶酶体贮积症

翟晓文
溶酶体贮积症(lysosomal storage diseases)是一组遗传代谢性疾病,主要是由于溶酶体水解酶缺乏功能缺陷所致。包括:①神经鞘脂贮积症,如戈谢病、尼曼-匹克病、法布里病等;②黏多糖贮积症;③黏脂质贮积症;④糖原贮积症Ⅱ型。其中以神经鞘脂贮积症临床最常见。
一、戈 谢 病
戈谢病(Gaucher disease)是为常染色体隐性遗传,突变基因位于1q21,导致β-葡萄糖脑苷脂酶(β-glucocerebrosidase)缺乏,葡萄糖脑苷脂在胞质内沉积形成戈谢细胞,浸润各种脏器如肝脾、肺、肾、骨骼等。
根据神经系统是否受累,分为3个亚型。Ⅰ型(非神经病变型):多见,起病慢,约2/3患者在儿童期发病,肝脾大,尤以脾大为主伴脾功能亢进,呈全血细胞减少。多数患者骨骼受累,表现为骨痛。部分患者肺部受累,表现为间质性肺病、肺实变和肺动脉高压等。成年以后或老年起病者临床表现多不典型,骨骼病变更显著。Ⅱ型(暴发性神经病变型):罕见,以迅速进展的急性神经系统表现为特征。新生儿期及婴儿期发病,病死率高,常2岁内死亡。Ⅲ型(慢性或亚急性神经病变型):早期与Ⅰ型相似,逐渐出现神经系统受累表现,常发病于儿童期,进展缓慢。
可根据临床及骨髓或肝、脾、淋巴结等组织中找到戈谢细胞作为初步诊断,该细胞体积大,直径约20~80μm,卵圆形,含一或数个偏心胞核,核染色质粗,胞质量多,无空泡,呈淡蓝色,充满洋葱皮样条纹结构,糖原和酸性磷酸酶染色呈强阳性。必须注意假性戈谢细胞可见于慢性粒细胞白血病、多发性骨髓瘤、骨髓增生异常综合征、地中海贫血及肺结核等。确诊依赖于检测外周血白细胞或培养细胞内β-葡萄糖脑苷脂酶活性检测。标本可采集新鲜全血,也可使用干血纸片法。当其外周血白细胞或皮肤成纤维细胞中葡萄糖脑苷脂酶活性降低至正常值的30%以下时,即可确诊。少数患者酶活性减低不到此标准,则需参血浆壳三糖酶活性并进一步做基因突变检测确诊。产前诊断采用对胎盘绒毛或羊水进行葡萄糖脑苷脂酶活性和(或)DNA基因突变检测。
治疗包括对症治疗,纠正贫血和血小板减少,止痛、理疗及骨折处理。脾切除可减轻脾大引起的症状,但是脾切除会加速葡萄糖脑苷脂在肝、肺、骨等器官的贮积,使症状加剧,应谨慎考虑。特异性治疗是注射用伊米苷酶(Imiglucerase)替代治疗,为目前Ⅰ型戈谢病治疗的标准方法,可明显改善患者的症状,该酶不能透过血脑屏障,对于有神经系统改变的患者无效。其他如底物减少疗法、分子伴侣疗法、基因治疗等方法均在探索中。国外曾使用造血干细胞移植成功治疗多名儿童患者,凡能够接受酶替代疗法的患者中不推荐造血干细胞移植。
二、尼曼-匹克病
传统上,尼曼-匹克病(Niemann-Pick disease,NPD)又称为神经鞘磷脂沉积病(sphingolipidosis),是一组常染色体隐性遗传疾病,是由于酸性神经鞘磷脂酶缺乏导致其底物神经鞘磷脂在单核-巨噬细胞中堆积所致。
NPD分为A、B、C、D四型,不同类型在致病基因、生化改变及临床表现等方面差异较大。A型和B型基因定位于11p15,C型95%定位于18q11-q12,5%定位于14q24,D型突变是发生在引起C型突变主基因上。A型和B型均为神经鞘磷脂酶缺乏引起。A型(急性神经型或婴儿型)最常见,婴儿早期即出现进行性肝、脾、淋巴结肿大,以及严重的神经系统退行性病变,约1/4患儿眼底检查可见黄斑区樱桃红斑,患儿常因反复呼吸道感染在2~3岁死亡。B型(慢性非神经型或内脏型)发病较A型稍晚,在儿童期或成年期诊断,慢性病程,内脏受累明显,但不累及神经系统。C型(亚急性神经型或少年型)主要由胆固醇转运缺陷引起,NPC1和NPC2已发现胆固醇转运缺陷相关的基因。常于1~6岁出现症状,主要表现为神经系统受累呈现亚急性病程,同时伴有轻微内脏受累,随后发现肝脾大,多数患者20~30岁时死于吸入性肺炎。D型(Nova-Scotia型)临床表现同C型患者类似,仅见于加拿大Nova Scotia省西部。
NPD的诊断可依据临床表现结合骨髓涂片见NPD泡沫样细胞又称尼曼-匹克细胞可初步诊断。该细胞直径20~100μm,有一个胞核,呈偏心位,胞质中充满脂滴呈泡沫样,PAS反应为弱阳性,而戈谢细胞为强阳性。当胞质呈蓝色时,则称“海蓝组织细胞”。外周血淋巴细胞可见空泡。因骨髓找到泡沫样细胞,还可见于其他溶酶体贮积症和某些组织细胞病,故确诊需要依据酶活性检测及基因检测。A型和B型NPD患者酸性鞘磷脂酶活性明显减低(正常值的1%~10%),而C型NPD患者酸性鞘磷脂酶活性仅轻微减低(正常值的50%~75%)。
尼曼-匹克病的治疗主要为对症支持疗法,尚无特异性治疗。异基因骨髓移植仅对极少部分B型患者有效,C型患儿可试用二甲基亚砜。
三、法布里病
法布里病(Fabry disease,FD)是X连锁隐性遗传病,突变基因位于Xq22。由于α-半乳糖苷酶A(α-GalA)活性部分或全部丧失,其代谢底物三己糖酰基鞘脂醇(GL3)和相关的鞘糖脂在溶酶体进行性贮积,导致多系统受累出现相应临床表现,如神经痛、皮肤血管角质瘤、少汗、角膜混浊和晶状体混浊、蛋白尿、肾衰竭、心肌病、心律不齐和暂时性脑缺血发作或脑卒中等。
按临床表现可分两型:①经典型:α-GalA活性明显下降甚至完全缺失(<5%),儿童期就可以出现临床表现,且男孩比女孩症状出现更早。以疼痛和血管角质瘤最为常见。疼痛从肢端开始逐渐向肢体及身体其他部位蔓延。血管角质瘤可累及全身,但一般在脐周和膝部最多。②迟发型:α-GalA活性部分下降(>5%),成人期发病,往往限于肾脏或心脏受累。
法布里病的诊断,男性病例确诊有赖于测定血浆或培养细胞中α-GalA的活性。而部分女性患者由于临床表现不典型,且酶活性测定可能正常,需行基因诊断。此病可通过绒毛膜或羊膜细胞的酶活性检测及DNA分析进行产前诊断。
治疗包括非特异性治疗和特异性治疗。特异性治疗目前使用重组α半乳糖苷酶(fabrazyme)进行替代治疗,减少患者细胞内GL3沉积,有效减轻患者肢端疼痛及胃肠道症状,改善心肌肥厚,稳定肾功能,从而改善患者的生活质量和预后。
主要参考文献
1.中华医学会儿科学分会遗传代谢内分泌学组,中华医学会儿科学分会血液学组,中华医学会血液学分会红细胞疾病(贫血)学组.中国戈谢病诊治专家共识(2015).中华儿科杂志,2015,53(4):256-261.
2.施惠平.溶酶体贮积症.实用儿科临床杂志,2007,22(8):261-263.
3.中国法布里病(Fabry病)诊治专家共识.中华医学杂志,2013,93(4):243-247.
第七节
其他少见组织细胞与树突状细胞疾病

许小平
一、树突状细胞肿瘤
(一)指突树突状细胞肉瘤
指突树突状细胞肉瘤(interdigitating dendritic cells sarcoma,IDCS)国内文献也有译为并指状树突状细胞肉瘤、指突状树突状细胞肉瘤或交指状树突状细胞肉瘤等。正常情况下,指突树突状细胞定居于淋巴结副皮质区。发生恶性转化的病因和机制尚不清楚,偶有报道与低级别的B细胞淋巴瘤及T细胞淋巴瘤有关。IDCS极为罕见。中位发病年龄51.4岁(6~77岁),男性略多于女性。病变主要累及淋巴结,但皮肤和软组织等结外部位也有报道。淋巴结病变主要累及副皮质区,可存在残留的滤泡。肿瘤细胞一致表达S100和波形蛋白(virmentin),CD1a和langerin阴性。束蛋白(fascine)通常阳性或变异,CD68、CD45和溶菌酶弱阳性,p53核染色可以强阳性。滤泡状树突细胞标记CD21、CD23和CD35阴性,其余MPO、CD34、特异的B细胞和T细胞相关抗原、CD30、内皮膜抗原(epithelial membrance antigen,EMA)、结蛋白(desmin)和细胞角蛋白(cytokeratin)均不表达。Ki-67指数通常为10%~20%(中位数11%)。间杂的小淋巴细胞多数为T细胞系列,B细胞几乎缺乏。电镜检查Birbeck颗粒阴性。
临床过程多数呈侵袭性。内脏器官如肝、脾、肾和肺常被累及。治疗多采用局部手术切除,辅以放疗或(和)化疗,也有接受骨髓移植的病例报道。通常死于诊断后1年之内,疾病分期与预后关系较为密切。
(二)滤泡树突状细胞肉瘤
滤泡树突状细胞肉瘤(follicular dendritic cell sarcoma,FDCS)是与FDC具有相似的形态和表型特征的梭形及卵圆形细胞的肿瘤性增生。
病因和发病机制不清楚,炎症性假肿瘤样变异型(inflammatory pseudo-tumor-like variant)与EB病毒明显相关。在肿瘤性梭形细胞可检测到EB病毒编码的RNA(EBER),Southern blot研究证明病毒以单克隆性游离体形式存在。
发病以成年人为主,中位发病年龄44岁(范围17~76岁),性别无明显差异。但炎症性假肿瘤样变异型以女性为多见。少数病例发病与Castleman病有关,以透明血管型为常见。一些患者有长期精神分裂症病史。
1/2~2/3的患者存在淋巴结病变,以颈部淋巴结累及最为多见。也可累及腋下、纵隔、肠系膜和腹膜后。淋巴结外的肿瘤常可见于扁桃体、口腔、胃肠道、肝、脾、软组织、皮肤以及乳腺。肿块常较大,中位直径5cm。肿瘤发生转移的部位以淋巴结、肺和肝为多见。肿瘤一般呈无痛性缓慢生长过程,除炎症性假肿瘤样变异型外,一般全身症状并不多见。
免疫表型特征为一个或多个滤泡树突细胞标记阳性,如CD21、CD35、CD23、Ki M4p以及 CAN42。Clusterin几乎总是强阳性,而在其他树突状细胞肿瘤通常阴性或弱阳性。此外,肿瘤细胞桥粒斑蛋白(desmoplakin)、波形蛋白(vimentin)、束蛋白(fascine)、表皮生长因子受体和 HLADR表达常为阳性。表皮膜抗原、S100蛋白和CD68阳性率变异较大。CD1a、溶菌酶、MPO、CD34、CD3、CD79a、CD30和HMB45表达阴性。Ki-67标记范围1%~25%(平均13%)。肿瘤细胞超微结构检查不应见到Birbeck颗粒。
肿瘤的生物学行为呈惰性。大部分患者治疗策略是采取手术完全切除肿瘤,然后根据情况是否加以放射治疗及化疗。40%~50%的患者会出现局部复发。肿瘤转移约见于25%的患者,多发生于复发后。
具有以下特征的FDCS患者预后较差:①显著的细胞异型性;②广泛的凝固性坏死;③高增殖指数;④肿瘤最大直径>6cm;⑤肿瘤位于腹腔内。
(三)其他罕见的树突状细胞肿瘤
其他罕见的树突状细胞肿瘤(other rare dendritic cell tumour)可以是起源于髓系起源的树突细胞,也可能是起源于基质细胞。除此以外,临床上可能还会遇到一些起源不明的树突状细胞肿瘤,WHO(2008)分类建议暂将它们称之为“树突状细胞肿瘤/非特指型”。
1.成纤维细胞性网状细胞肿瘤
成纤维细胞性网状细胞肿瘤(fibroblastic reticular cell tumour)极为罕见,一般认为起源于淋巴结副皮质区参与转运可溶性介质如细胞因子、趋化因子的成纤维细胞性网状细胞。文献报道的“细胞角蛋白阳性间质性网状细胞瘤(cytokeratin-positive interstitial reticulum cell tumour)”可能与其是同一实体。肿瘤可发生在淋巴结、脾脏及软组织。组织学特点与滤泡树突状细胞肉瘤和指突树突状细胞肉瘤相似,但缺乏这些肿瘤的免疫表型谱。组织学检查的另一发现是分散存在的细长胶原纤维。电镜下可见梭形细胞有细致并延伸的细胞质和类似于肌纤维母细胞的特征。肿瘤细胞对平滑肌肌动蛋白、结蛋白(desmin)、细胞角蛋白和CD68的免疫反应不一。
2.不能确定的树突状细胞肿瘤
不能确定的树突状细胞肿瘤(Indeterminate dendritic cell tumour)表型特征与正常的不能确定的细胞(可能为朗格汉斯细胞的前体细胞)相似。临床极为罕见,可与低度恶性B细胞淋巴瘤有关。
患者的典型表现为一个或多个普通的丘疹、结节或斑块,通常无全身症状。病变一般发生在皮肤,但也可发展至皮下脂肪组织。浸润为弥漫性,增生的肿瘤细胞与朗格汉斯细胞类似。嗜酸性浸润通常不存在。超微结构显示这些细胞缺乏Birbeck颗粒。可混合有指突状细胞突起,但缺乏桥粒。增生细胞表达S100和CD1a,但Langerin阴性。特异的B细胞和T细胞标记、CD30、组织细胞标记CD163、滤泡树突状标记CD21、CD23、CD35均为阴性。CD45、CD68、溶菌酶、CD4可不同程度阳性表达。Ki-67阳性指数变异不一。有个案报道雄激素受体基因检测为克隆性。
(四)播散性幼年性黄色肉芽肿
播散性幼年性黄色肉芽肿(juvenile xanthogranuloma,JXG)的细胞起源尚有争论,尽管表达巨噬细胞表型,但因FⅧa和fascine表达阳性,故有可能起源于表皮/间质树突状细胞。
病因未明。有人认为与神经纤维瘤病1型(neurofibromatosis type1,NF-1)有关。两者共存者易患幼年型慢性粒单核细胞白血病(JMML)。
本病最常见于从婴儿期至10岁的儿童,也可见到较大儿童和成人患者(Erdheim-Chester病)。患者以前可有恶性肿瘤病史。除并发JMML外,少数患者可见合并淋巴母细胞性淋巴瘤。
病变累及皮肤者50%左右,其他累及部位包括肾、肺、软组织、中枢神经系统、呼吸道和消化道,心肌、心包、后腹膜、脾以及骨骼较少见。
早期受累器官显示密集的形态学单一的组织细胞浸润。病变后期常见体积较大的淡染的泡沫样组织细胞、Touton巨细胞和异物巨细胞,以及混合性炎症细胞浸润,包括中性粒细胞、淋巴细胞和嗜酸性粒细胞,罕见肥大细胞。免疫表型检测通常对FⅧa、CD68、CD163、溶菌酶和vimentin抗体发生反应,fascine、CD4以及S-100呈不一致阳性。一般不表达CD1a和Langerin。
虽然已报道的病例都呈良性表现。但脑组织、硬脑膜,垂体等部位的病变可以导严重后果甚至死亡。
二、其他少见组织细胞疾病
(一)窦状组织细胞增生伴巨大淋巴结病
窦状组织细胞增生伴巨大淋巴结病(sinus histiocytosis with massive lympha-denopathy,SHML)是一种原因不明的良性淋巴结增生性疾病,又称Rosai-Dorfman病(RDD)。该病多发生于淋巴结,约25%~43%的病例发生于淋巴结外。病理组织学特征是显著增生的组织细胞体积巨大,胞质丰富,吞噬活跃。淋巴结外RDD可发生于皮肤、软组织、中枢神经系统、呼吸道、肾脏骨骼系统等。
RDD的病因仍不清楚。少数学者曾对RDD做病原学研究,发现部分RDD病变组织中可检测到人类疱疹病毒6型(HHV6)、HHV8、EBV、HPV和巨细胞病毒。本病的组织学改变较特殊,诊断并不困难。但如果对本病缺乏认识,则可能发生误诊。
大多数文献认为SHML是良性增生性病变,少数病例预后不良。治疗包括手术切除、放疗、化疗和应用激素等,部分病例可自行消退。淋巴结外RDD由于术前很难确诊,目前报道以手术切除为主,适当扩大手术范围,彻底清除病变组织以预防复发。对病变残留或复发者可采用糖皮质激素治疗或放疗。
(二)Erdheim-Chester病
Erdheim-Chester病(ECD),又称脂质肉芽肿病,是一种罕见的非朗格罕细胞组织细胞增生症,病因不明。
ECD以男性更常见,确诊时的平均年龄53岁。临床表现多样化,但所有患者均有骨骼破坏,骨痛是最常见的临床表现,在有些患者可能是唯一的症状,主要对称性累及下肢骨骼,尤其膝关节和踝关节处。半数以上患者伴有骨骼外病变,如神经系统、眼眶内、皮肤、腹膜后器官如肾脏、肾上腺和胰腺等;心脏累及达40%,肺部累及约20%。部分患者有全身症状,表现为发热、乏力、体重减轻。
X线检查特征性表现为双侧对称性长骨干骺端和长骨骨干骨皮质硬化,尤其股骨远端和胫腓骨的近端部位,骨骼和骨骺部分有明确的界限。受累及骨骼主要为股骨、胫骨、腓骨,尺骨、桡骨和肱骨受累少见。脊柱、肋骨、颅骨和骨盆的影像学检查一般正常。
不同病变部位均可获取标本做组织病理学检查,但以骨骼和眼眶后受累部位最有诊断价值。组织学表现常描述为由泡沫样组织细胞或“充满脂质”的巨噬细胞或组织细胞浸润的黄色瘤或黄色肉芽肿,病变周围纤维化,免疫组织化学染色显示CD68(+)、S-100(+)和CD1a(-)。
疾病呈进展性,目前报道的病例中有60%的患者死亡。骨外受累及者预后很差。
主要参考文献
1.Jaffe ES,Harris NL,Vardiman JW,et al.血液病理学.陈刚,李小秋主译..北京:科技出版社.2013.944-956.
2.Swerdlow SH,Campo E,Harris NL,et al.WHO Classification of Tumors of Haematopoietic and Lymphoid Tissues.4th ed.Lyon:IARC,2008,361-367.
3.Li L,Shi YH,Guo ZJ,et al.Clinicopathological features and prognosis assessment of extranodal follicular dendritic cell sarco-ma.World J Gastroenterol,2010,16(20):2504-2519.
4.Orii T,Takeda H,Kawata S,et al.Differential immunophenotypic analysis of dendritic cell tumours.J Clin Pathol,2010,63(6):497-503.
5.Skiner M,Briant M,Morgan MB.Erdheim-Chester disease:a histiocytic disorder more than skin deep.Am J Dermatopathol,2011,33(2):e24-26.

