第三章
消化系统主要症状和体征
第一节
腹痛

石 虹
腹痛(abdominal pain)为临床常见症状,病因复杂,多为器质性病变所引起,但也可为功能性腹痛。病变多来自腹腔或盆腔内器官,但腹腔或盆腔外器官病变亦可引起腹痛。按病程可将腹痛分为急性腹痛和慢性腹痛。
【病因】
(一)引起腹痛的腹腔与盆腔脏器的病变
常见的有:
1.炎症
阑尾炎、胰腺炎、胃炎、肠炎、憩室炎、胆囊炎、肾盂肾炎、腹膜炎、腹腔内脓肿、盆腔炎等。
2.溃疡
胃十二指肠溃疡、溃疡性结肠炎等。
3.肿瘤
胃癌、肝癌、肠癌、胰腺癌等。
4.阻塞或扭转
肠梗阻、胆绞痛、肾绞痛、肠粘连、嵌顿疝、肠扭转、卵巢囊肿扭转等。
5.穿孔或破裂
消化性溃疡、憩室穿孔,异位妊娠、黄体、卵巢囊肿、脾、肝癌结节、腹主动脉瘤破裂等。
6.血管病变
肠系膜动脉血栓形成、脾梗死等。
7.其他
肠痉挛、急性胃扩张等。
(二)引起腹痛的腹腔或盆腔外脏器与全身性的疾病
常见的有:
1.胸部疾病
心肌梗死、心包炎、大叶性肺炎、胸膜炎、肺梗死、带状疱疹等。
2.变态反应性疾病
腹型紫癜症、腹型风湿热等。
3.代谢性或内分泌疾病
糖尿病、Addison病、血卟啉病、高钙血症等。
4.药物或毒物
皮质类固醇、硫唑嘌呤、铅、酒精、阿片类药物等。
5.血液系统疾病
镰型细胞病、溶血性疾病。
6.神经系统疾病
脊髓损害、脊髓痨、神经根病、腹型癫痫等。
7.精神心理性疾病
中枢性腹痛综合征、抑郁症、焦虑症、疑病性神经症等。
【发病机制】
内脏的感觉通过自主神经传导,腹壁的感觉通过脊神经传导,两者均汇集于脊髓背根。根据发生机理的不同,可将腹痛分为四类。
(一)内脏性腹痛
痛觉冲动主要经内脏神经传入,因空腔脏器平滑肌过度收缩、扩张、扭曲、拉伸,或实质脏器的包膜张力增高或炎症而引起。疼痛弥漫、定位不明确,前者多为阵发性绞痛,而后者多为钝性疼痛。
(二)躯体性腹痛
痛觉冲动经脊神经传入。疼痛来源于腹壁,腹膜壁层,肠系膜根部或膈肌。与内脏性腹痛相比,疼痛更强烈、定位更局限。
(三)感应性腹痛
是内脏神经与脊神经共同参与引起的疼痛。感觉疼痛的部位与疼痛的来源部位不同,但为同一脊髓节段背根神经所支配的皮肤感觉区。如胆囊疼痛牵涉到背部或右肩体表。
(四)心理性腹痛
文化、情感和社会心理的因素影响每个人的疼痛体验。部分腹痛患者经充分检查不能发现器质性的病因,中枢性超敏反应、心理性的原因(抑郁或躯体化障碍)是其腹痛的原因。
【诊断和鉴别诊断】
腹痛是一个非常常见的临床症状。在进行诊断时应详细询问病史,尤其注意询问疼痛的特征和伴随症状。结合症状、体征及实验室检查结果等各方面的资料,进行综合分析。
(一)诊断
1.病史采集
(1)一般资料:
首先应了解患者的年龄、性别和职业。儿童腹痛常见的病因是蛔虫症、肠系膜淋巴结炎与肠套叠等。青壮年则多见溃疡病、胰腺炎。中老年则多胆囊炎、胆结石、癌症与心肌梗死的可能性。异位妊娠、卵巢囊肿扭转、黄体破裂则是妇女急腹症的常见病因。有长期铅接触史的患者要考虑铅中毒性腹痛。
(2)现病史
1)腹痛的诱因:
饮酒和进油腻食物可诱发急性胰腺炎或胆道疾病;饮食不洁可导致急性胃肠炎;近期有外伤史者应考虑内脏破裂。
2)起病方式:
起病隐袭的多见于溃疡病、慢性胆囊炎、肠系膜淋巴结炎等。起病急骤的则多见于胃肠道穿孔、胆道结石、输尿管结石、肠系膜动脉栓塞、卵巢囊肿扭转、肝癌结节破裂、异位妊娠破裂等。
3)腹痛的部位:
应了解腹痛是局限性的还是弥漫性的、腹痛的具体部位、最痛的部位以及疼痛开始的部位。
4)腹痛的性质和节律:
胀痛常为器官包膜张力增加、系膜牵拉或肠管胀气扩张等所致。空腔脏器的梗阻常引发急性绞痛,如肠梗阻、胆管结石或输尿管结石等,并常有阵发性加重;阵发性钻顶样痛是胆道、胰管或阑尾蛔虫梗阻的特征;消化性溃疡穿孔则引发烧灼样或刀割样的持续性锐痛,可迅速扩散到全腹。空腔脏器慢性病变引起的腹痛多呈阵发性,程度较轻。实质脏器慢性病变引起的腹痛多为持续性隐痛或钝痛。溃疡病引起的中上腹痛常有节律性和周期性。
5)腹痛的程度:
腹痛程度在一定意义上反映了病情的轻重,通常腹膜炎或腹腔脏器梗阻、狭窄、缺血等病变引起的腹痛程度剧烈。但老年人、应用过镇痛药物、反应差或意识模糊的患者有时病变虽重,腹痛表现却不明显。
6)腹痛的放射:
由于神经分布的关系,某些部位病变引起的疼痛常放射至固定的区域,如胆道病变右上腹痛伴右肩或肩胛下疼痛;肾盂、输尿管病变引起的疼痛多向腹股沟方向放射;子宫和直肠痛常放射至腰骶部等。
7)腹痛的伴随症状:
伴发热的提示为炎症性病变。伴便血的可能是肠套叠、肠系膜血栓形成或肿瘤性疾病等。伴血尿的多为输尿管结石。伴休克的多为内脏破裂出血、胃肠道穿孔并发腹膜炎。
8)与腹痛有关的因素:
应了解是否存在加重或缓解腹痛的因素(食物、药物、酒精、体位、运动、排便等)。
(3)既往史:
胆绞痛与肾绞痛者以往多曾有类似发作史。有腹腔手术史者有肠粘连的可能,有心房纤颤史的则要考虑肠系膜血管栓塞等。
(4)月经史:
对女性患者应了解末次月经日期、既往月经周期是否规律、有无停经及停经后再出血、经血量等。
2.体格检查
检查生命体征,初步判断患者病情的轻重缓急。对危重患者,可以在有重点地进行问诊和最必要的体检后,先进行抢救生命的处理,待情况允许再作详细检查。如果腹部和直肠检查结果正常,应该仔细检查有无腹外疾病引起腹痛的证据,尤其是脊椎、脊髓、肺部和心血管系统。
3.实验室检查
根据患者的症状和体征合理选择实验室检查,如:血常规、尿常规和其他尿液检查、粪常规和隐血试验、血液生化、肿瘤标志物、心电图、X线、超声、CT、MRI、内镜、脑电图、阴道后穹隆穿刺、选择性肠系膜血管造影、腹腔穿刺检查。必要时可考虑手术探查。
(二)鉴别诊断
1.急性腹痛部位与可能诊断
腹痛的部位有助于引导初始诊断,并缩小鉴别诊断的范围。急性腹痛具有起病急、病情重、转变快的特点。表15-3-1列举了急性腹痛部位与部分可能的诊断,供临床鉴别诊断参考。
表15-3-1 急性腹痛部位与可能诊断

续表

2.慢性腹痛部位与可能诊断
慢性腹痛是指起病缓慢、病程长的腹痛,或急性腹痛起病后又反复发作,有时可迁延达数月或数年之久。慢性腹痛患者就诊时通常能明确指出腹痛的部位。表15-3-2列举了慢性腹痛部位与部分可能的诊断,供临床鉴别诊断参考。
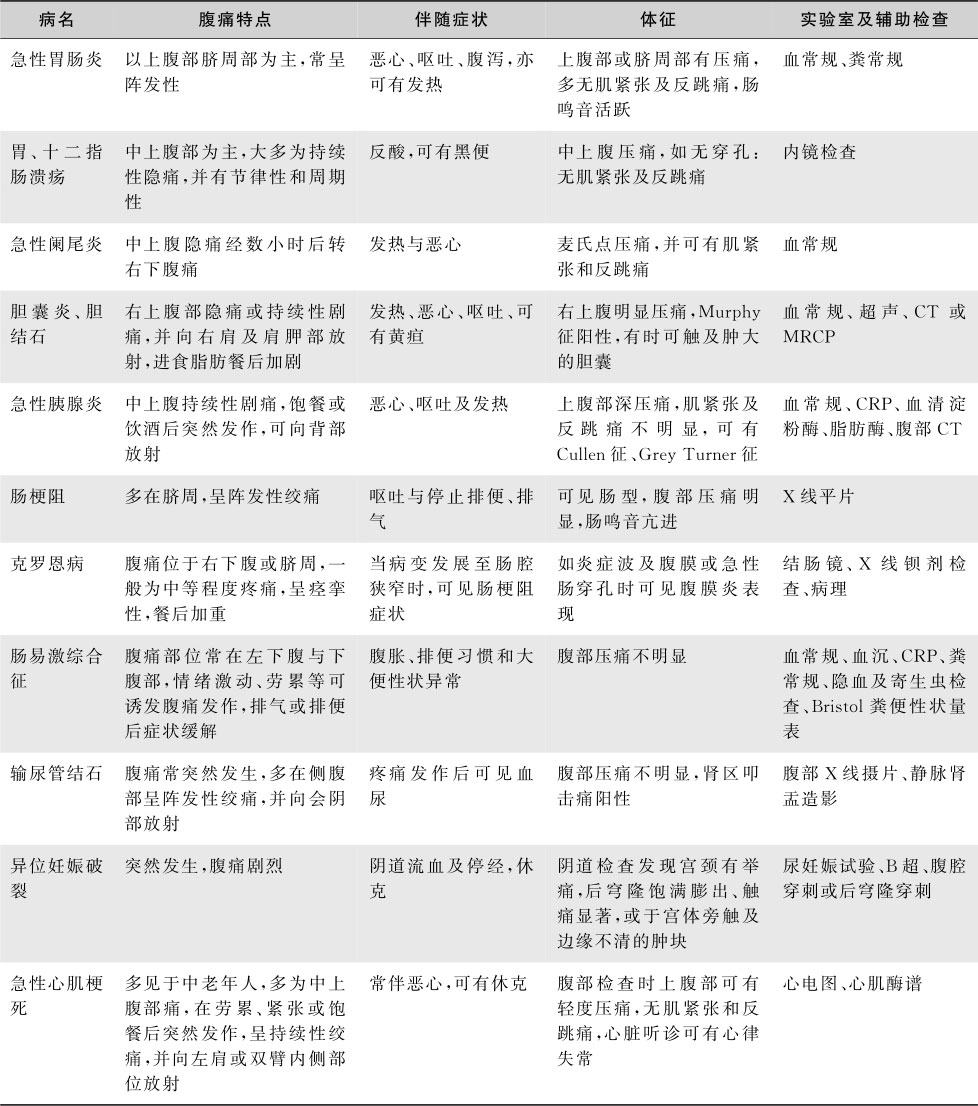
3.腹痛常见疾病的鉴别诊断
腹痛常见疾病的腹痛特点、伴随诊断、体征和实验室及辅助检查请参见表15-3-3。
表15-3-2 慢性腹痛部位与可能诊断

注:IBD,炎症性肠病(inflammatory bowel disease);IBS,肠易激综合征(irritable bowel syndrome)
表15-3-3 腹痛常见疾病的鉴别诊断
4.特殊人群
在评估病情及诊断、鉴别诊断的过程中应该注意妇女或老年腹痛患者的特殊性。妇女的腹痛可能与盆腔器官的病变有关。卵巢囊肿、子宫纤维瘤、输卵管卵巢脓肿、子宫内膜异位征是妇女下腹痛的常见病因。对于育龄期的妇女,需注意评估患者是否妊娠,包括异位妊娠。老年患者某些疾病的发病率(如憩室)和疾病的严重度可能更高(如泌尿系统感染)。老年患者腹痛的临床表现也可能不典型,患者的记忆能力下降和症状严重程度的下降可能导致漏诊和误诊。隐匿的泌尿系统感染、内脏穿孔、缺血性肠病是老年患者中经常被漏诊或延迟诊断的潜在致命疾病。
【诊疗流程】
腹痛是一个症状,治疗腹痛应查明病因,针对引起腹痛的疾病进行治疗。如果在初始临床评估时发现患者有腹膜炎的体征(肌卫、反跳痛、板状腹),应立即对患者实施抢救,给予吸氧、静脉补液、抗感染治疗、并评估是否需行剖腹手术。急性及慢性腹痛的诊疗流程分别见图15-3-1及图15-3-2。
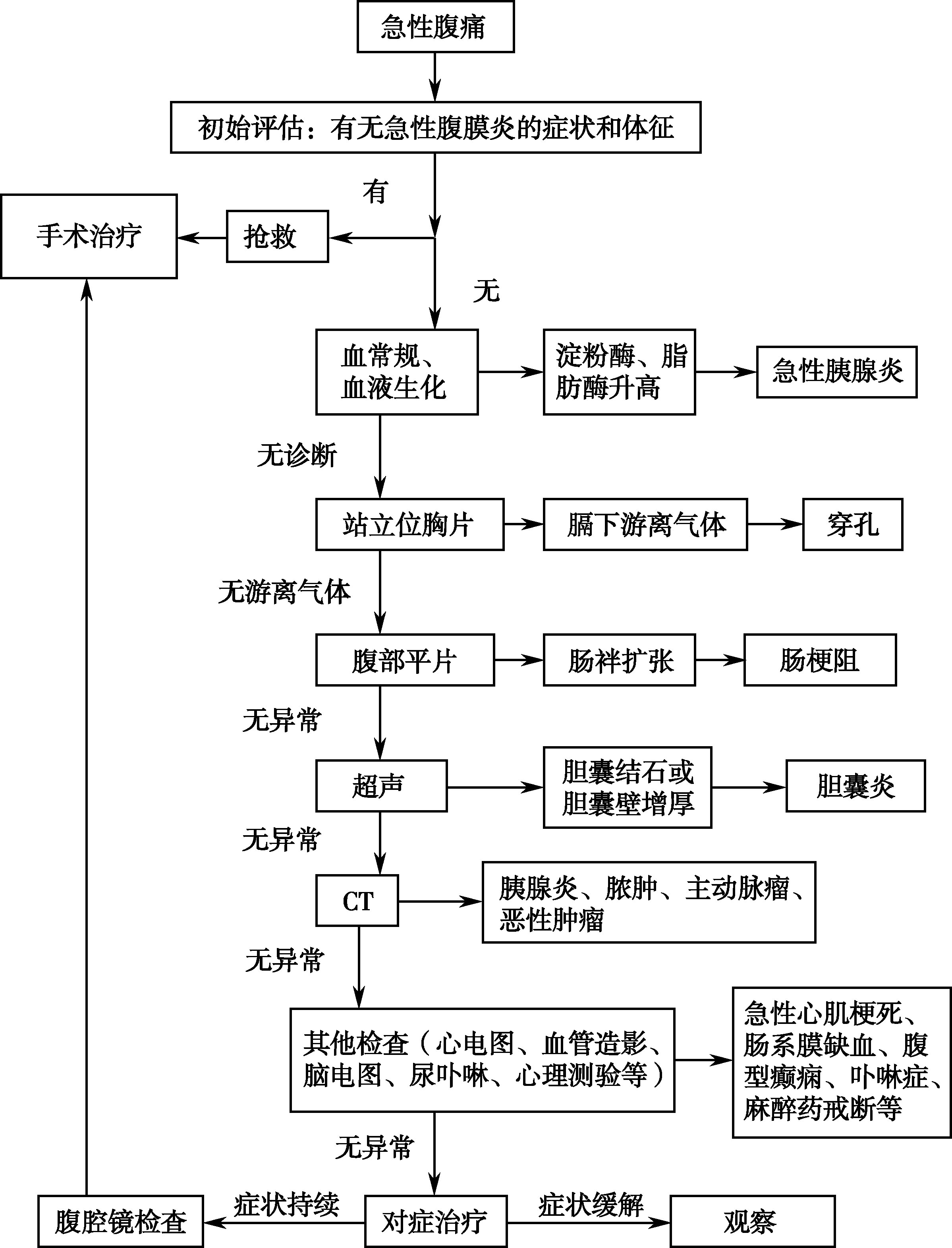
图15-3-1 急性腹痛诊疗流程

图15-3-2 慢性腹痛诊疗流程
主要参考文献
1.Penman ID,Lees CW.Chapter 22,Abdominal pain.Walker BR,Colledge NR,Ralston SH,Penman ID,eds.Davidson's principles and practice of medicine,22th ed.London,UK:Churchill Livingstone,2014:861-863.
2.Keefer L,Drossman DA,Guthrie E,et al.Centrally mediated disorders of gastrointestinal pain.Gastroenterology,2016,150:1408-1419.
第二节
黄疸

李 蕾
黄疸(jaundice)是指由于血浆胆红素浓度增高(>34.1μmol/L或>2mg/dl)沉积于组织中,引起巩膜、皮肤、黏膜以及其他组织和体液发生黄染的现象。当胆红素超过正常值但<34μmol/L时无肉眼黄疸,称隐性或亚临床黄疸。高胆红素血症作为疾病状态的一种表现具有很大的临床和病理生理意义。
一、胆红素代谢
(一)胆红素的来源
成人平均每日产生胆红素250~350mg,其中70%~80%源自衰老红细胞,在脾脏、骨髓和肝脏中由网状内皮细胞捕获并降解生成的血红素,另10%~20%主要来源于无效红细胞生成以及其他血红蛋白。
(二)运输和排泄
开始形成的胆红素为游离胆红素,因未经肝细胞摄取、未与葡萄糖醛酸结合,称非结合胆红素,又名间接胆红素。非结合胆红素与血清白蛋白结合而输送,非水溶性,不能从肾小球滤过,故尿液中不出现非结合胆红素。非结合胆红素通过血循环运输至肝后,经葡萄糖醛酸转移酶(UGT)的催化作用和葡萄糖醛酸结合,形成水溶性的结合胆红素,可通过肾小球滤过从尿中排出。
(三)肝脏对胆红素的处理
①肝细胞通过易化转运机制及扩散作用实现对非结合胆红素的摄取;②主要与谷胱甘肽-5-转移酶族的各种胞液蛋白进行细胞内结合;③通过由UGT1基因复合体编码的特异性UDP-葡萄糖醛酸基转移酶同工型(UGT1A1),把非结合性胆红素转化为胆红素单/双葡萄糖醛酸酯(BMG/BDG);④由小管膜三磷酸腺苷(ATP)依赖性运载蛋白即多元耐药相关蛋白2(MRP2)或小管多元特异性有机阴离子运载蛋白(cMOAT)把胆红素单、双葡萄糖醛酸酯转移到胆汁。
(四)胆红素的肝后处理
结合胆红素进入肠腔后,经肠道细菌脱氢作用还原为尿胆原,大部分(68~473μmol)随粪便排出,称为粪胆原。小部分(10%~20%)经回肠下段或结肠重吸收,通过门静脉血回到肝脏,转变为胆红素或未经转变再随胆汁排入肠内,这一过程为胆红素的“肠肝循环”。从肠道重吸收的尿胆原,有很少部分(每日不超过6~8μmol)进入体循环,经肾排出。
二、黄疸的分类
(一)病因发病学分类
分为:①溶血性黄疸;②肝细胞性黄疸;③胆汁淤积性黄疸;④先天性非溶血性黄疸。临床上以前三类为常见,特别是肝细胞性黄疸和胆汁淤积性黄疸。
(二)按胆红素的性质分类
根据胆红素代谢过程中主要环节的障碍,可分为:
1.以非结合胆红素升高为主的黄疸
血清总胆红素升高,其中非结合胆红素占80%~85%以上。由肝前性因素引起,主要见于:①胆红素生成过多,如先天性和获得性溶血性黄疸、旁路性高胆红素血症等;②胆红素摄取障碍,如Gilbert综合征、某些药物及检查用试剂引起的黄疸等;③胆红素结合障碍,为葡萄糖醛酸转移酶活力减低或缺乏引起的黄疸,如Gilbert综合征、Crigler-Najjar综合征、新生儿生理性黄疸等。
2.以结合胆红素增高为主的黄疸
结合胆红素在总胆红素中所占比例大于30%,可由胆红素在肝内转运、排泄障碍或同时由胆红素摄取、结合和排泄障碍引起:①肝外胆管阻塞,如胆结石、胰头癌等;②肝内胆管阻塞,如广泛肝内胆管结石、华支睾吸虫病等;③肝内胆汁淤积,如肝炎、药物性肝病、妊娠期多发性黄疸、Dubin-Johnson综合征等。
此分类方法的优点是以胆红素性质为依据,对胆红素代谢障碍的环节及其可能的病因大致指出了范围,对诊断和治疗有所帮助,但不少黄疸的发生机制涉及多种因素,可能有胆红素的摄取、结合和排泄障碍分别或同时存在,应结合临床,认真分析。
三、溶血性黄疸
【病因和发病机制】
大量红细胞的破坏,形成大量的非结合胆红素,超过肝细胞的摄取、结合及排泄能力,另一方面,由于溶血造成的贫血、缺氧和红细胞破坏产物的毒性作用,削弱了肝细胞对胆红素的代谢能力,使非结合胆红素在血中潴留,超过正常的水平而出现黄疸。
【临床特征】
1.可有与溶血相关的病史 如输血、特殊药物、感染及溶血家族史等。
2.急性溶血或溶血危象时起病急,溶血反应剧烈,如寒战、高热、呕吐、腰背酸痛、全身不适等,慢性溶血症状轻微,但可有面色苍白。
3.巩膜见轻度黄染,呈浅柠檬色。
4.皮肤无瘙痒。
5.可有肝脾大,特别是慢性溶血者。
6.有骨髓增生活跃表现,如周围血出现网织红细胞增多、出现有核红细胞、骨髓红细胞系增生活跃。
7.血清总胆红素增高,除溶血危象外,血清胆红素一般不超过85μmol/L(5mg/dl),其中以非结合胆红素升高为主,占80%以上。
8.尿中尿胆原增加而无胆红素,急性发作时可有血红蛋白尿,呈酱油色。慢性溶血者尿内含铁血黄素增加。
9.其他检查 遗传性球形红细胞增多时红细胞脆性增加,地中海贫血时脆性降低,自身免疫性溶血时Coombs试验阳性。
四、肝细胞性黄疸
【病因和发病机制】
肝细胞广泛病损,对胆红素摄取、结合和排泄功能发生障碍,以致有相当量的非结合胆红素潴留于血中,同时因肝细胞损害和肝小叶结构破坏,致使结合胆红素不能正常地排入细小胆管而反流入血,发生黄疸。
【临床特征】
1.肝病本身表现 如急性肝炎者,可有发热、乏力、纳差、肝区痛等表现;慢性肝病者,可有肝掌、蜘蛛痣、脾脏肿大或腹水等。
2.皮肤和巩膜呈浅黄至金黄色,皮肤偶有瘙痒。
3.血清总胆红素升高,一般<170μmol/L,其中以结合胆红素升高为主(>35%)。
4.尿中胆红素阳性,尿胆原常增加,但在疾病高峰时,因肝内淤胆致尿胆原减少或缺如,同样粪中尿胆原含量可正常、减少或缺如。
5.肝功能试验 根据不同肝病可出现下列某些试验异常:①转氨酶升高;②凝血酶原时间异常,提示肝细胞损害严重;③严重肝病时,也可出现胆固醇、胆固醇酯、胆碱酯酶活力下降等;④伴有肝内淤胆时,碱性磷酸酶可升高;⑤血清白蛋白下降。
6.免疫学检查 血中肝炎病毒标记物阳性支持病毒性肝炎的诊断,线粒体抗体阳性常支持原发性胆汁性肝硬化的诊断,血清甲胎蛋白对原发性肝细胞癌诊断有参考价值。
7.肝脏活组织检查对弥漫性肝病的诊断有重要价值,光镜、电镜、免疫组化、原位杂交、免疫荧光等检查,有利于肝病的诊断。
8.B超、CT等对肝病的诊断有帮助。
五、胆汁淤积性黄疸
【病因和发病机制】
胆汁淤积可分为肝内性或肝外性。
1.肝外胆汁淤积
即原来所称梗阻性黄疸,可由于胆总管结石、狭窄、炎症水肿、肿瘤及蛔虫等阻塞胆总管。
2.肝内胆汁淤积
主要见于毛细胆管型病毒性肝炎、药物性胆汁淤积、原发性胆汁性肝硬化、妊娠期复发性黄疸等。
【临床特征】
1.肝外梗阻者,常见的胆石症、胆管炎。常有发热、腹痛、呕吐等症状,黄疸来去迅速。胰头癌及壶腹周围癌常缺乏特征性临床表现,但可有乏力、纳差、消瘦等症状,黄疸常进行性加重。
2.肤色暗黄、黄绿或绿褐色,甚至黑色,胆红素浓度逐渐升高,一般>170μmol/L(30mg/dl)以上,其中以结合胆红素升高为主。
3.皮肤瘙痒显著,常出现在黄疸之前,可能与血中胆盐刺激皮肤神经末梢有关。
4.尿胆红素阳性,尿胆原减少或消失,部分不完全梗阻者需结合其他临床表现而考虑。
5.粪色特点 粪中尿胆原减少或缺如,粪便呈浅灰色或陶土色。如梗阻为壶腹部周围癌引起,可因出血使粪便呈黑色或隐血阳性。
6.肝功能试验 碱性磷酸酶、γ-谷胺酰转肽酶明显升高。血清总胆固醇可升高,脂蛋白-X可阳性,长时期梗阻可使血清转氨酶升高及白蛋白下降,如维生素K缺乏可使凝血酶原时间延长,此时如注射维生素K可使凝血酶原时间纠正。
7.其他检查 B超、CT、ERCP、PTC、胆道造影均有助于梗阻性黄疸的诊断。CEA、CA19-9、α 1 -抗胰蛋白酶也有所帮助。
六、先天性非溶血性黄疸
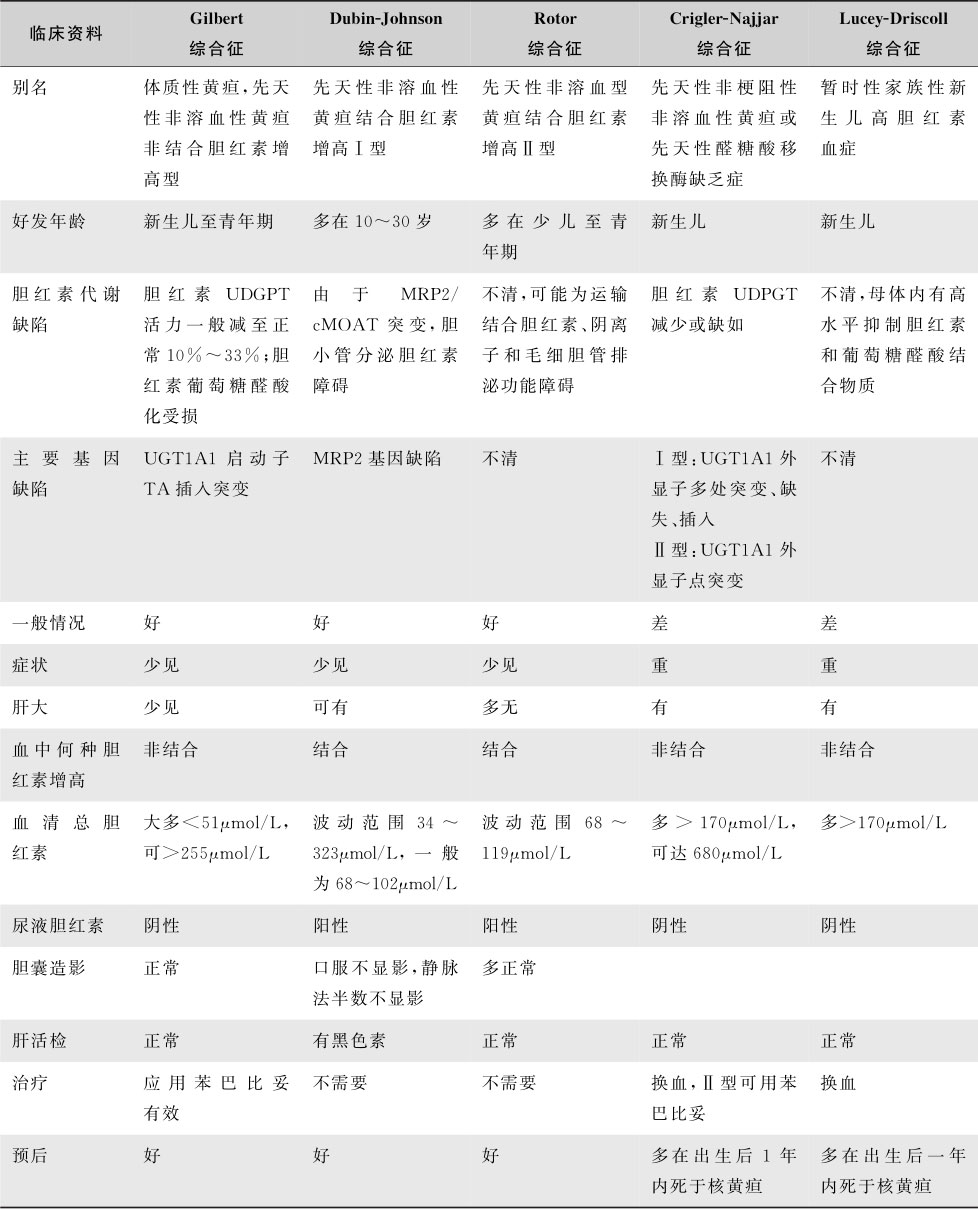
系指由于先天性酶缺陷所致肝细胞对胆红素的摄取、结合及排泄障碍,临床上少见,大多发病于小儿和青年期,有家族史,除极少数外,多数健康情况良好(表15-3-4)。
表15-3-4 常见遗传性胆红素代谢缺陷疾病临床特征
1.以非结合胆红素升高为主
(1)Gilbert综合征(Gilbert syndrome):
胆红素结合缺陷。是最常见的遗传性高胆红素血症,由于葡萄糖醛酸转移酶(UGT)1A1基因外显子1上游启动子TATAA序列出现重复片段,致使UGT活性下降而导致非结合胆红素在肝细胞内酯化过程障碍。可因饥饿、感染、发热、妊娠、手术而诱发或加重,血清非结合胆红素升高,应用苯巴比妥有效,或无须特别处理,预后良好。
(2)Crigler-Najjar综合征(Crigler-Najjar syndrome):
葡萄糖醛酸转移酶减少或缺失。分Ⅰ和Ⅱ型,Ⅰ型系UGT1A1基因1~5外显子发生多处替换、缺失或插入突变;而Ⅱ型仅是在任一外显子的点突变,UGT的结构变异相对较轻,故Ⅱ型病情明显好于Ⅰ型。Ⅰ型常在出生后不久(6~18个月)即死于核黄疸,肝移植是Ⅰ型患者首选的治疗方法,但移植之前,患儿需先维持一个循序渐进的光疗方案,使肝移植能在出现严重的神经损伤之前进行;Ⅱ型可在出生后即出现黄疸,也可在随后20~30年中反复发生。禁食、感染、酸血症、代谢紊乱等可诱发或加重,胆红素升高明显时可有核黄疸发生。Ⅱ型患者对苯巴比妥治疗有反应,预后较佳。
2.以结合胆红素升高为主
(1)Dubin-Johnson综合 征(Dubin-Johnson syndrome):
胆红素转运缺陷。有明显家族背景,可能为常染色体隐性遗传,是由于毛细胆管面肝细胞膜上MRP2蛋白基因变异所致。非结合胆红素仍可经OATP介导进入肝细胞,在酯化过程中与葡萄糖醛酸结合而被运输,但由于其在毛细胆管面肝细胞膜上的排泄障碍而诱发黄疸。临床以结合胆红素升高为主;肝外观呈绿黑色(黑色肝),肝活检组织检查见肝细胞内有弥漫性的棕褐色色素颗粒,多在肝小叶中央区的溶酶体内,性质和来源不明,不是铁质、胆汁及脂褐素。可能是黑色素或肾上腺代谢物多聚体。有些患者除肝细胞内有色素外,尿液及脾内也曾出现有类似色素的存在。本病无须特别治疗,预后良好。
(2)Rotor综合征(Rotor syndrome):
为慢性家族性高结合胆红素血症,也是常染色体隐性遗传。主要缺陷发生在肝脏对胆红素及相关有机阴离子的摄取或储存方面,检测尿中排出的粪卟啉有助于与Dubin-Johnson鉴别。肝活检正常,无色素沉积。
(3)良性复发性肝内胆汁淤积(Benign recurrent intrahepatic cholestasis,BRIC):
本病为家族性常染色体隐性遗传病。其特点为反复发作的瘙痒和黄疸。首次起病可发生在任何年龄,但多在20岁前发病。感染、抗生素及非甾体类药物的应用等均可诱发此病。病程可持续数周至数月。该病的肝脏病理主要表现为胆汁淤积,肝脏组织结构一般正常,一般不会进展为肝硬化。此病系家族性肝内胆汁淤积基因1(FIC1)突变所致。
(4)进行性家族性肝内胆汁淤积(progressive familial intrahepatic cholestasis,PFIC):
指引起婴儿胆汁淤积和儿童终末期肝病的三种表型相关的综合征。与Dubin-Johnson时的选择性胆红素转运缺陷不同,这些综合征的高胆红素血症是因广泛的胆汁分泌障碍引起。三种综合征均以常染色体显性遗传,1型和2型中尽管AKP水平升高,γ-GT水平低;3型患者γ-GT及AKP水平均增高。Ⅰ型也因FIC1变异引起,但比BRIC时的变异更严重。FIC1编码移位酶蛋白ATP8B1,功能为从外部转运氨基磷脂到不同细胞的膜内叶;2型因ABCB11基因变异引起,该基因编码胆盐输出泵;3型因ABCB4基因变异引起,该基因编码多药耐药基因3(MRP3)蛋白,具有转移磷脂酰胆碱的重要功能。
七、黄疸的鉴别诊断
(一)首先应与假性黄疸鉴别
假性黄疸见于过量进食含胡萝卜素食物或服用某些药物如阿的平、新霉素等,可引起皮肤发黄而巩膜正常。老年人球结膜有微黄色脂肪蓄积,巩膜黄染不均匀,此时皮肤不黄染。所有假性黄疸者,血清胆红素浓度均正常。
(二)黄疸病因诊断
1.最常见病因
慢性肝病失代偿、酒精性肝炎、胆囊疾病(胆囊炎,胆总管结石)、脓毒病/血流动力学异常、恶性肿瘤(胰腺癌、肝转移)。
2.常见病因
病毒性肝炎、药物或毒素导致肝脏疾病、溶血(尤其镰状细胞性贫血)、手术后(多种原因)、原发性胆汁性肝硬化、原发性硬化性胆管炎。
3.比较不常见病因
霍奇金病及非霍奇金淋巴瘤、全胃肠外营养、Gilbert综合征。
(三)黄疸鉴别诊断方法
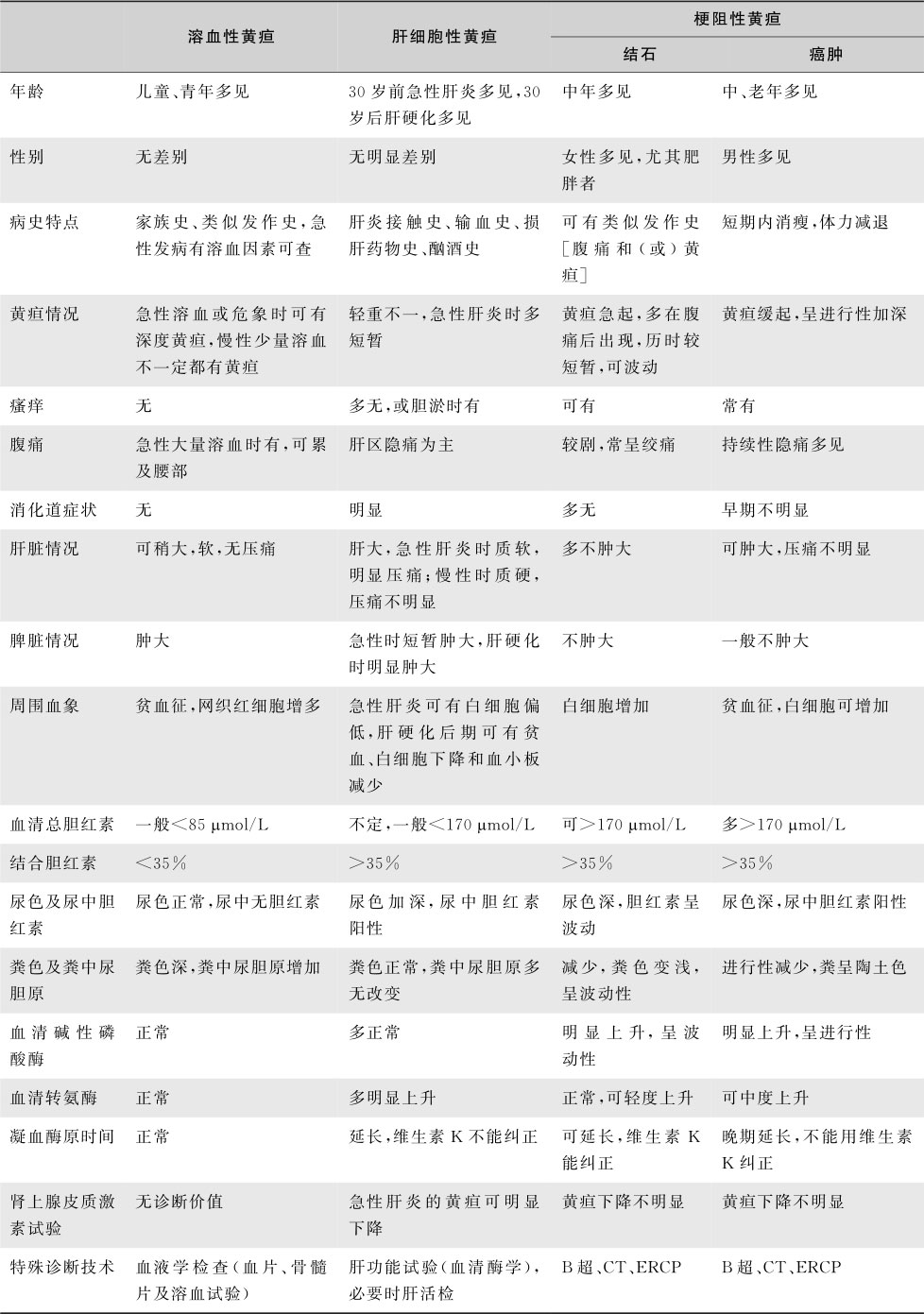
黄疸的鉴别诊断应结合病史、症状、体征、实验室及其他辅助检查结果,进行综合分析和判断(表15-3-5、图15-3-3),才能得到正确的诊断。
1.病史
对于黄疸患者首先要确定高胆红素血症是非结合型还是结合型,是急性还是慢性过程。如果是非结合型胆红素升高要确定是胆红素产生增多、摄取减少还是结合障碍。对于结合型胆红素升高为主者要确定是肝内胆汁淤积还是肝外胆道梗阻。发热、很快出现黄疸、右上腹痛、肝大并有触痛提示为急性病。寒战和高热可能是胆管炎或细菌感染,而低热和类似流感的症状通常提示为病毒性肝炎。疼痛放射到背部提示胆道或胰腺疾病;瘙痒,黄疸持续3~4周可能来自各种原因所致的梗阻性黄疸。
表15-3-5 黄疸的鉴别诊断
病史特点能够提供病因学线索。不洁饮食、近期输血、静脉内滥用药物和不健康性行为提示可能为病毒性肝炎。药物、溶剂、乙醇或口服避孕药通过引起胆汁淤积和肝细胞损害而产生黄疸。胆结石病史、既往胆道手术和曾经有过黄疸提示胆道疾病。黄疸家族史则提示可能有胆红素转运或合成缺陷或有遗传性疾病(例如 Wilson病、血色病、α 1 -抗胰蛋白酶缺乏)。30岁以下的年轻患者可能为急性器质性疾病,而65岁以上的老年患者多为结石和恶性肿瘤。男性多有酒精性肝病、胰腺癌或肝细胞性肝癌、血色病,而女性多有原发性胆汁性肝硬化、胆结石或慢性活动性肝炎。
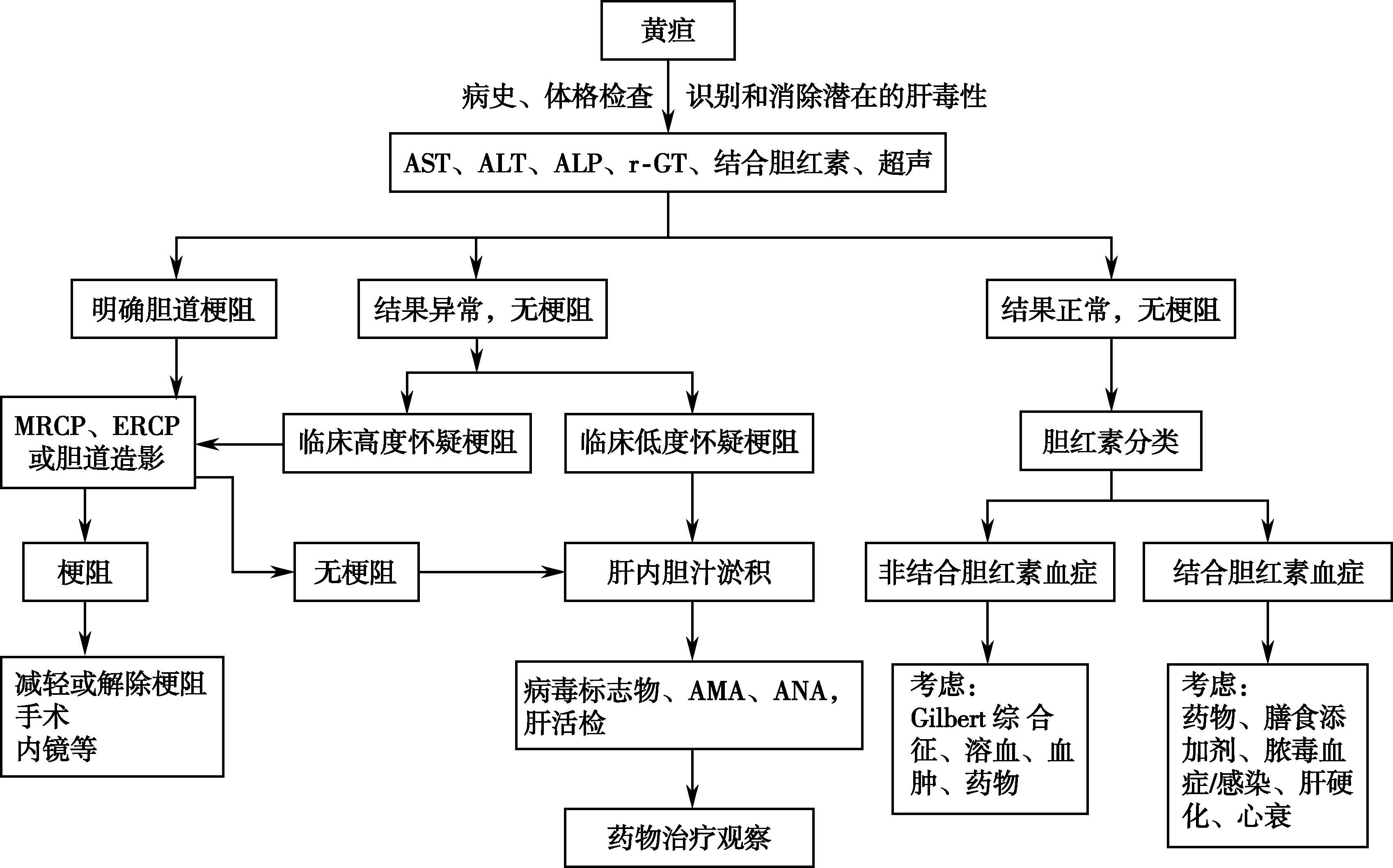
图15-3-3 黄疸患者诊治流程
2.症状与体征
高热常提示有细菌感染,在急慢性病中都能出现。恶病质、消瘦、肝掌、黄疣、男乳女性化及蜘蛛痣提示为慢性肝病。肝缩小、触及结节并伴有脾大则为肝硬化,而肿块或淋巴结肿大可能为恶性肿瘤。肝上下径超过15cm提示为脂肪肝、淤血、恶性肿瘤、其他浸润性疾病。腹水可出现于肝硬化、恶性肿瘤和较重的急性肝炎时。触诊胆囊肿大常为恶性胆道梗阻。扑翼样震颤和精神症状则为肝病晚期。
3.实验室检查
实验室检查可确定病史及体检中存在的疑点。
(1)非结合型高胆红素血症:
网织细胞数、乳酸脱氢酶、结合珠蛋白量及外周血涂片检查能提供溶血依据。如果确定是溶血,要进行免疫功能检查、维生素B 12 缺乏、铅中毒、地中海贫血、铁粒幼红细胞贫血的实验检查。如果不是溶血,大多数单纯的非结合型高胆红素血症最后可能被诊断为Gilbert综合征。
(2)结合型高胆红素血症:
首先要将胆汁淤积原因与肝细胞原因区别开来。包括测定转氨酶、碱性磷酸酶、总蛋白及白蛋白。如果碱性磷酸酶正常,那么不大可能是胆汁淤积性。虽然天门冬氨酸氨基转移酶(AST)和丙氨酸氨基转移酶(ALT)不是肝病的特异酶,但是大于300IU/ml在非肝胆病中是不常见的。急性黄疸型肝炎时,ALT、AST明显增高,其他肝病时,ALT、AST也可升高。AST>ALT为乙醇损害。胆汁淤积性黄疸时,二酶多数正常,少数病例可有升高,但幅度较低。重症肝炎时,随着黄疸的加深,二酶活力反而下降,甚至正常,这就是所谓的“胆酶分离”现象,预后险恶。亮氨酸转氨肽酶、5-核苷酸酶或γ-谷胺酰转移酶(γ-GT)有助于区别碱性磷酸酶升高是由肝脏疾病引起还是骨源性的。血清学检查可确定特征性肝脏疾病,例如抗线粒体抗体阳性多为原发性胆汁性肝硬化,肝炎血清标志物阳性多为病毒性肝炎,α 1 -抗胰蛋白酶、铁及血浆铜蓝蛋白的测定结果可以判定是否为遗传性肝病,甲胎蛋白过高多为恶性肿瘤,血沉、免疫球蛋白、抗核抗体和平滑肌抗体的测定结果可以判定是否为自身免疫病。低蛋白血症时球蛋白升高支持肝硬化诊断。胆汁淤积常伴有高胆固醇血症。
4.辅助检查
(1)超声检查:
是发现胆道梗阻的首选检查方法,它的准确率为77%~94%。急性梗阻时要经过4小时~4天时间才能发现胆道扩张。部分或间断梗阻可能不引起扩张。由于超声很难看到胆管末端,所以不能准确地确定梗阻部位,而且20%~40%的胆总管结石患者胆道直径正常。
(2)电子计算机断层扫描(CT):
超声检查不能明确诊断时,可以进行CT检查,CT能够较好地判断是肝内还是肝外团块性损害。在超声和CT引导下可对团块病变进行细针穿刺活检。CT也可了解胰腺及其周围情况。
(3)磁共振成像(MRI):
磁共振胆道成像(MRCP)对胆道疾病的诊断具有一定的价值,能清楚的显示胆道系统,是有用的非创伤性检查。
(4)经十二指肠镜逆行胰胆管造影(ERCP)和经皮肝穿胆道造影(PTC):
肝穿刺胆管造影适用于有胆管扩张和怀疑高位胆管梗阻者,ERCP适用于无胆管扩张和十二指肠壶腹、胰腺和低位胆管病变者。ERCP诊断胆管梗阻的敏感性为89%~98%,特异性为89%~100%。而PTC的敏感性和特异性分别为98%~100%。PTC除诊断外,还可作胆管引流。通过ERCP还可作括约肌切开取石术、气囊扩张狭窄胆管、放置鼻胆管引流、内支架等治疗措施。此两项措施已广泛用于黄疸的鉴别诊断。
(5)上消化道钡餐及内镜检查:
可发现曲张的食管胃底静脉,有利于门脉高压症的诊断。十二指肠低张造影有助于肝外梗阻的诊断,如胰头癌时,十二指肠乳头区及其附近可显示黏膜病变、压迹或充盈缺损,胆囊癌常在十二指肠球部或降部造成压迹。超声内镜有助于发现由十二指肠乳头癌、胆管癌或胰腺癌所致黄疸,经超声内镜细针穿刺进行胰腺活体组织学检查更有助于确定胰腺疾病性质。
(6)肝组织检查:
急性黄疸很少需作肝穿刺来协助诊断。肝穿刺常用于持续性黄疸怀疑肝内胆汁淤积或因其他弥漫性肝病如慢性肝炎、早期肝硬化病变所致,有时也用于肝内占位性病变的诊断,深度黄疸并非肝穿刺的禁忌证,但必须慎重以排除肝外梗阻所致的肝内胆管扩张情况,以免发生胆汁性腹膜炎。对先天性非溶血性黄疸的诊断一般均需作肝活检检查后才能确定。对凝血功能异常的患者,可作经静脉肝内活检,同时可了解肝静脉、门静脉的压力,无出血及胆汁性腹膜炎的并发症,但操作较复杂,需一定的技术和设备。
(7)腹腔镜检查:
对少部分诊断十分困难的病例仍可选用。通过腹腔镜可观察到肝脏大小、形态、是否有结节、色泽等,有利于某些疾病的诊断。另外腹腔镜直视下作肝活检也较安全正确。
主要参考文献
1.Ajiki T,Fukumoto T,Ueno K,et al.Three-dimensional computed tomographic cholangiography as a novel diagnostic tool for evaluation of bile duct invasion of perihilarcholangiocarcinoma.Hepatogastroenterology,2013,60(128):1833-1838.
2.Dai D,Mills PB,Footitt E,et al.Liver disease in infancy caused by oxysterol 7 alpha-hydroxylase deficiency:successful treatment with chenodexycholic acid.J Inherit Metab Dis,2014,37(5):851-861.
3.Fitz JG:Approach to the patient with abnormal liver chemistries or jaundice.In Podolsky DK,Camilleri M,Fitz JG,et al.YAMADA's Textbook of Gastroenterology 6th ed,Qxford:John Wiley&Sons Ltd,2016,819-833.
第三节
腹泻

刘红春
正常大便多为每日1次,亦可2~3日1次或1日2~3次。腹泻(diarrhea)是指每日排便3次及以上,或明显超过平日习惯的频率,粪质稀薄或水样便,常伴有排便急迫感及腹部不适或失禁等症状。常以每日大便重量超过200g作为腹泻的客观指标。腹泻按病程分急性和慢性两类,急性腹泻发病急,常呈自限性,多为病毒或细菌感染引起,病程在2周之内,少数可持续至2周以上;慢性腹泻的病程超过4周,或间歇期在2~4周内的复发性腹泻,常为非感染因素引起。人群中5%有慢性腹泻,其中40%患者在60岁以上。
【发病机制】
正常人每24小时约有9~10L液体进入空肠,饮食与消化液混合后形成等渗的食糜,在外源性肾上腺素能神经、神经多肽激素等调节下,小肠可吸收80%~90%的液体,仅有1.5 L左右排至结肠,结肠又吸收大部分水分,最终仅有100ml水分随粪便排出,如果小肠或结肠的分泌增加或吸收减少,则出现腹泻。腹泻主要由小肠液体和电解质转运改变引起,肠腔内的葡萄糖、半乳糖或氨基酸可通过与Na + 耦联增强小肠Na + 的吸收,任何减少Na + 、水吸收和(或)增加Cl - 、水分泌的过程,均可导致腹泻。腹泻按发病机制可分为渗透性、分泌性、渗出性和动力改变,但通常腹泻发生时可有几种机制共同参与,临床上分为吸收不良性腹泻(脂肪泻)、水样泻和炎性腹泻。
任何影响食物在肠腔内消化、肠黏膜吸收或营养运输至全身循环的疾病或药物都可造成吸收不良,其中饮食脂肪是最难消化的营养成分,脂肪泻是吸收不良最主要的表现。水样泻往往是摄入不吸收或难吸收物质引起渗透性腹泻,肠道快速通过,或神经内分泌肿瘤产生高浓度的促分泌素促进肠道分泌。渗出性腹泻时常有肠黏膜细胞损害、绒毛萎缩及隐窝细胞增生。损伤的小肠黏膜细胞双糖酶和多肽水解酶活性下降,Na + 耦联的糖和氨基酸转运机制及氯化钠吸收转运减弱或缺如;相反,增生的隐窝细胞仍能分泌Cl - ,结果水和电解质的吸收减少而分泌增加。此外,严重的炎症可发生免疫介导的血管损害或溃疡,脓血及蛋白从毛细血管和淋巴管中渗出;同时淋巴细胞和巨噬细胞释放多种炎症介质如前列腺素等刺激肠黏膜分泌,加重腹泻。
一、急性腹泻
【病因和临床表现】
急性腹泻(acute diarrhea)约80%为感染性,包括病毒、细菌及其毒素、寄生虫等。非感染性因素包括药物、化学品、缺血性结肠炎、过敏、放疗等。
1.食物中毒
如摄入污染了金黄色葡萄球菌毒素、砷、铅、汞等重金属的食物,或食用毒蘑菇以及鳍鱼等海鲜后出现呕吐腹泻等消化道症状。金黄色葡萄球菌毒素进入体内起病快,进食后4~6小时即可发病;蘑菇毒素中毒常伴肝肾衰竭。海鲜类中毒除了呕吐腹泻等消化道症状,常伴有口周发麻烧灼感,以及脸色潮红、头痛、心悸等。
2.肠道感染
包括病毒如诺如病毒和轮状病毒等,细菌如沙门氏菌、空肠弯曲菌和志贺氏菌等,或寄生虫如隐孢子虫等感染,常伴呕吐、腹部绞痛、水泻或血样便和发热;旅行者腹泻为旅途中或旅行后发生的腹泻,多为肠毒性大肠埃希菌感染所致;此外,一些全身感染如病毒性肝炎、流感等都可引起明显的腹泻。
3.药物
如泻药(包括硫酸镁、磷酸钠盐、聚乙二醇、乳果糖、大黄等)、细胞毒性药物(如奥沙利铂等)、非甾体类抗炎药、质子泵抑制剂、抗生素等,尤其是应用广谱抗生素后部分患者可继发艰难梭状芽胞杆菌感染引起假膜性肠炎。
4.其他
如粪块堵塞、盆腔炎症(如急性阑尾炎)、食物过敏、急性缺血性肠病、放疗等均可引起腹泻,偶有剧烈运动后出现腹部绞痛、便急伴恶心呕吐,可能与运动引起促分泌素释放或缺血有关。
【实验室检查和辅助检查】
新鲜粪便检查是诊断急性腹泻病因的重要步骤,发现红白细胞、吞噬细胞提示肠道感染,粪便白细胞和隐血试验有利于鉴别细菌性腹泻;粪乳铁蛋白有助于鉴别炎性和非炎性腹泻。粪培养阳性率低,但重度腹泻、免疫抑制状态者、血性腹泻以及有炎症性肠病基础的患者应及早行粪培养,可发现弯曲杆菌、沙门氏菌、志贺氏菌、艰难梭菌及真菌等致病菌。此外,耶尔森菌属、邻单胞菌属、肠出血性大肠埃希菌属O157∶H7、产气单胞菌属等因不做常规培养而易漏诊。大便找虫卵和寄生虫适用于时间较长的持续性腹泻、细胞或体液免疫缺陷、血性腹泻等患者,连续检查数日可提高阳性率。通常不需行结肠镜检查,当与炎症性肠病难以鉴别、疑似假膜性肠炎、应用免疫抑制的患者疑巨细胞病毒感染等需行肠镜检查,但需警惕肠穿孔。
【诊断】
急性腹泻多由自限性感染引起,病程在10天以内,根据病史体检,多不需深入检查。按腹泻严重程度需进一步检查的情况有:大量水泻导致低容量、每日便次超过6次、持续时间超过2天、血样便、腹部剧痛、发热(T>38.5℃)、高龄患者(>70岁)、或免疫抑制状态的患者。病史线索对急性腹泻的诊断很重要,如伴发热提示感染,进食后起病快提示食物中毒。
【治疗原则】
1.补液
急性腹泻所致死亡多由脱水引起,故首先需评价脱水程度,补充液体和电解质。严重脱水者应予林格氏液或生理盐水,并酌情补充钾和碳酸氢钠。对于清醒的轻中度脱水患者,口服补液盐与静脉补液同样有效。
2.止泻
次水杨酸铋对细菌性腹泻安全有效;阿片类和抗胆碱能药物不推荐;洛哌丁胺可使病原菌延迟排出,但对急性腹泻不伴高热脓血便的患者相对安全;加蒙脱石散及益生菌可缓解症状。化疗和放疗引起的轻-中度腹泻可予洛哌丁胺和非甾体类消炎药,严重腹泻可予奥曲肽。
3.抗生素
怀疑细菌感染时首选喹诺酮类抗生素或利福昔明。
【预防】
避免不洁饮食。轮状病毒疫苗可预防或减轻症状。前往疫区前可予霍乱疫苗注射。
二、慢性腹泻
【病因和发病机制分类】
(一)吸收不良
1.由于解剖结构改变、消化酶的缺乏、微胶粒形成障碍造成的腔内消化障碍,如Roux-Y手术、慢性胰腺炎、小肠细菌生长过度等。
2.黏膜吸收障碍 可由刷状缘营养转运酶缺乏,或广泛疾病破坏小肠黏膜、手术切除或小肠旁路使黏膜有效吸收面积减少。病因有无载脂蛋白B血症、麦胶性肠病、热带口炎、贾第蓝氏鞭毛虫、HIV感染、Whipple病、移植物抗宿主病(GVHD)、短肠综合征等。
3.营养运输至血液循环障碍,其中肠淋巴引流阻塞分为先天性淋巴管扩张和继发性淋巴管扩张如淋巴瘤、结核、缩窄性心包炎、腹膜后纤维化等。常有低蛋白血症,诊断需行小肠黏膜活检。(详见本篇第六章第十一节“吸收不良综合征”)
(二)水样泻
可为渗透性、分泌性、炎症性或混合性。
1.各种泻药
如镁离子磷酸根离子等;乳果糖等不吸收的糖;原发或继发性乳糖酶缺乏者摄入含乳糖食物;非渗透性通便药如酚酞、番泻叶等。
2.肠道快速通过
如高碳水化合物低脂饮食使胃排空增加,肠内容物过快通过肠腔,甲状腺功能亢进者。
3.神经内分泌肿瘤如
(1)类癌综合征:
可致水泻、皮肤潮红、哮喘和腹部绞痛。约1/3类癌患者以腹泻为首发症状。
(2)胃泌素瘤:
常伴难治性或少见部位的消化性溃疡,因分泌大量胃酸引起小肠黏膜损伤而致腹泻;此外,过低的pH可使胰脂肪酶失活和胆汁酸沉淀,引起脂肪消化不良。
(3)血管活性肠肽瘤(VIP瘤):
罕见,系胰腺非β细胞腺瘤分泌血管活性肠肽等引起,表现为大量水泻,钾、HCO 3 - 大量丢失引起严重脱水、低钾和代谢性酸中毒,可伴有血钙、血糖升高和颜面潮红。肿瘤分泌多种多肽类介质如VIP、前列腺素等,刺激小肠分泌大量液体和电解质。
(4)甲状腺髓样瘤:
可分泌降钙素、前列腺素、VIP、5-羟色胺等引起水泻,出现腹泻时往往肿瘤已有转移。真性分泌性腹泻的特点:①肠黏膜组织学基本正常;②肠液与血浆的渗透压相同;③粪质呈水样,量大,无脓血;④禁食不减轻腹泻。
4.绒毛状腺瘤
结直肠绒毛状腺瘤可引起腹泻,可能与肿瘤分泌前列腺素有关。
5.糖尿病相关性腹泻
糖尿病自主神经病变者肠动力紊乱蠕动过缓,致使结肠型的细菌在小肠定植和过度生长,脂肪、胆盐和碳水化合物的吸收受到影响;同时胰腺外分泌功能不全亦是腹泻的原因。
6.酒精相关性腹泻
可能与饮酒后肠道快速通过、胰腺分泌减少及酒精相关性肠病有关,戒酒并适当补充营养后,腹泻可逐渐好转。
7.病因不明分泌性腹泻
经过各种检查仍有部分病因不明,考来烯胺或洛哌丁胺多有效。
(三)炎症性腹泻
又称渗出性腹泻(exudative diarrhea),可水样或血性腹泻。病因包括:
1.炎症性肠病(详见本篇第六章第十节“炎症性肠病”)。
2.特殊细菌或原虫感染 如肠结核、肠阿米巴感染等。
3.脓肿形成 如憩室炎等。
4.嗜酸性胃肠炎。
5.食物过敏 常在食用海鲜、鸡蛋、坚果或牛奶后出现腹部痉挛、腹泻、呕吐。予泼尼松20~40mg,每日1次,共7~10日有效,依次减去法筛选致敏食物并避免食用可预防。
6.胶原性结肠炎和淋巴细胞性结肠炎 统称显微镜下结肠炎,其中胶原性结肠炎九成以上为中老年女性,可能与自身免疫或NASIDs有关。
7.蛋白丢失性肠病 包括淋巴管扩张、肠结核、淋巴瘤、系统性红斑狼疮等。
8.放射性肠炎 放射治疗后可发生临近部位的放射性肠炎,放射量在40~60Gy以上,少数甚至可在治疗后20年才出现症状。早期炎症介质增加,血管内皮细胞、上皮细胞凋亡。治疗往往不满意,柳氮磺胺吡啶和激素等抗炎药及抗生素疗效不佳,考来烯胺、NSAIDs及洛哌丁胺等可能有效。
9.其他疾病 急性肠系膜动静脉血栓可表现为急性血性腹泻伴腹痛,慢性肠系膜血管缺血可表现为水泻,此外白塞病、嗜酸性肉芽肿性血管炎等均可引起腹泻。
渗出性腹泻的特点是粪便含有渗出液和血液,结肠尤其是左半结肠炎症多有肉眼黏液脓便,如有溃疡或糜烂,往往出现脓血便。小肠炎症时往往无肉眼可见的脓血便。
【临床表现】
(一)年龄和性别
功能性腹泻、肠结核和炎症性肠病多见于青壮年,而结肠癌多见于老年男性,但近年来发病有年轻化趋势,显微镜下结肠炎多见于老年人。
(二)起病与病程
炎症性肠病、肠易激综合征、吸收不良综合征和结肠憩室炎等病引起的腹泻,可长达数年至数十年之久,常呈间歇性发作。结肠癌引起的腹泻很少超过两年。
(三)排便情况与粪便外观
病变位于直肠和(或)乙状结肠的患者多有里急后重,每次排便量少,有时只排出少量气体和黏液,粪色较深,多呈黏冻状,可混有血液,腹痛多为持续性,位于下腹或左下腹,便后可稍减轻;显微镜下结肠炎则表现为慢性反复发作的水泻;小肠病变的腹泻无里急后重,粪便稀烂成液状,色较淡,量较多。慢性胰腺炎等吸收不良性腹泻患者的粪便中可见油层漂于水面,多泡沫,含食物残渣,大便有恶臭,质黏不易冲洗;慢性痢疾、血吸虫病、溃疡性结肠炎、直肠癌等病引起的腹泻,粪便常带脓血;肠结核和肠易激综合征常有腹泻与便秘交替现象;影响睡眠的夜间腹泻多系器质性疾病所致。
(四)伴随症状
慢性腹泻伴发热腹痛时,要考虑克罗恩病、溃疡性结肠炎、阿米巴病、淋巴瘤和肠结核。显著消瘦和(或)营养不良要考虑引起小肠吸收不良的各种疾病、胃肠道肿瘤和甲状腺功能亢进症。伴随关节炎症状的要考虑溃疡性结肠炎、克罗恩病、Whipple病等。腹泻伴少见部位或难治性消化性溃疡要排除胃泌素瘤。吸收不良可伴维生素和矿物质缺少的表现,如铁、叶酸、维生素B 12 缺乏可引起厌食,感觉异常和共济失调;钙、镁、维生素D缺乏引起搐搦、骨质疏松、骨痛等。
(五)体格检查
长期腹泻营养不良可见双下肢水肿,甲状腺髓样癌可扪及甲状腺肿大,神经内分泌肿瘤有时可发现皮肤潮红,游走性坏死性红斑是胰高血糖素瘤的表现,糖尿病有时可发现自主神经功能失调。
【实验室及辅助检查】
常规粪检白细胞增多,粪隐血阳性,血白细胞、嗜酸性粒细胞或血沉增加,白蛋白下降提示炎症性腹泻。检测血清铁、叶酸、维生素B 12 、维生素D及凝血酶原时间(维生素K)来评价吸收不良患者的营养状况。
影像学检查:腹平片胰腺钙化提示吸收不良性腹泻。腹部CT、MRI或消化道钡餐可发现胃手术史、胃结肠瘘、盲袢、小肠狭窄、空肠多发憩室、肠动力异常等,这些解剖结构改变易引起小肠细菌过度生长。小肠皱襞增厚则提示淀粉样变、淋巴瘤、Whipple病、淋巴管扩张等。回肠为主的节段性肠壁增厚提示进展性克罗恩病,可伴浆膜渗出和系膜侧梳状征;空肠为主的肠壁均匀分层样增厚符合嗜酸细胞性胃肠炎;放射区域的肠壁水肿提示放射性肠炎。生长抑素受体 131 碘可定位胃泌素瘤、胰腺内分泌肿瘤及类癌等。
内镜和活组织检查:若麦胶性肠病血清试验(如抗麦胶蛋白抗体,AGAs)阳性,或临床提示小肠黏膜吸收不良,可胃镜行十二指肠远端活检或小肠镜下空肠活检。若抗组织转谷氨酰胺酶(t TG)IgA升高大于5倍且抗肌内膜抗体(EMA)阳性可确诊麦胶性肠病。
【诊断】
慢性腹泻(chronic diarrhea)多数可通过病史、体检、大便常规培养及找虫卵和寄生虫、大便艰难梭状芽孢杆菌毒素测定、大便脂肪测定,以及结肠镜检查和活检等来明确诊断。详细询问大便习惯、大便性状、体重下降情况、近期外出旅游史、食物/牛奶耐受情况,基础胃肠
若腹泻仍原因不明,可检测大便的重量、体积、脂肪、电解质、渗透压、pH值、泻药筛查等。碳水化合物吸收不良常粪pH下降,因细菌分解碳水化合物形成短链脂肪酸,若pH<5.3常提示单纯碳水化合物吸收不良。正常血清 粪渗透压差[290-2×(粪 Na + +粪 K + )]约为50~125,若压差<50提示分泌性腹泻,若压差>125,提示渗透性腹泻。粪Mg 2+ >50mmol/L,提示含镁泻药所致腹泻。病或肝脏疾病、腹部手术、放疗或化疗、家族史、特殊药物应用史、饮酒史。若每日排便10~20次,禁食无效多考虑分泌性腹泻,若同时伴有难治性消化性溃疡提示胃泌素瘤。
吸收不良性腹泻:高脂饮食(70~100g/d)后粪脂检测是吸收不良的最佳筛查方法,若粪脂检测阴性,应考虑选择性碳水化合物吸收不良或其他原因的水泻;若粪脂检测阳性,则根据临床怀疑进一步检查胰腺外分泌功能,小肠钡剂通过时间,近端小肠黏膜活检,D-木糖呼气试验等;经验性地补充外源性胰酶腹泻改善可诊断胰腺外分泌功能不全。疑寄生虫感染可大便检测虫卵和寄生虫,以及蓝氏贾第鞭毛虫抗原。
水样泻:碳标记或氢标记的呼气试验可评价碳水化合物、胆盐吸收不良或小肠细菌过度生长。通常神经内分泌肿瘤引起的腹泻罕见,若CT发现肿瘤,并有神经内分泌肿瘤综合征表现,可测定相应血浆激素水平。类癌、胃泌素瘤、VIP瘤、甲状腺髓样癌、胰高糖素瘤、生长抑素瘤等血清素和尿5-羟吲哚乙酸升高,血清胃泌素、血管活性肠肽、降钙素、胰高糖素、生长抑素、组胺或前列腺素升高。生长抑素受体放射性核素扫描敏感性高,对诊断卓-艾综合征有价值。
炎性腹泻:粪隐血常阳性,粪白细胞、乳铁蛋白、钙卫蛋白升高提示肠道炎症,胶囊内镜和结肠镜可发现溃疡。蛋白丢失性肠病最敏感的检测是24小时粪白蛋白或α 1 抗胰蛋白酶定量。
【治疗】
病因治疗和对症治疗都很重要(具体方案详见相关章节)。慢性腹泻诊疗流程详见图15-3-4。在未明确病因之前,要慎重使用止泻药和止痛药,以免掩盖症状造成误诊耽误病情。
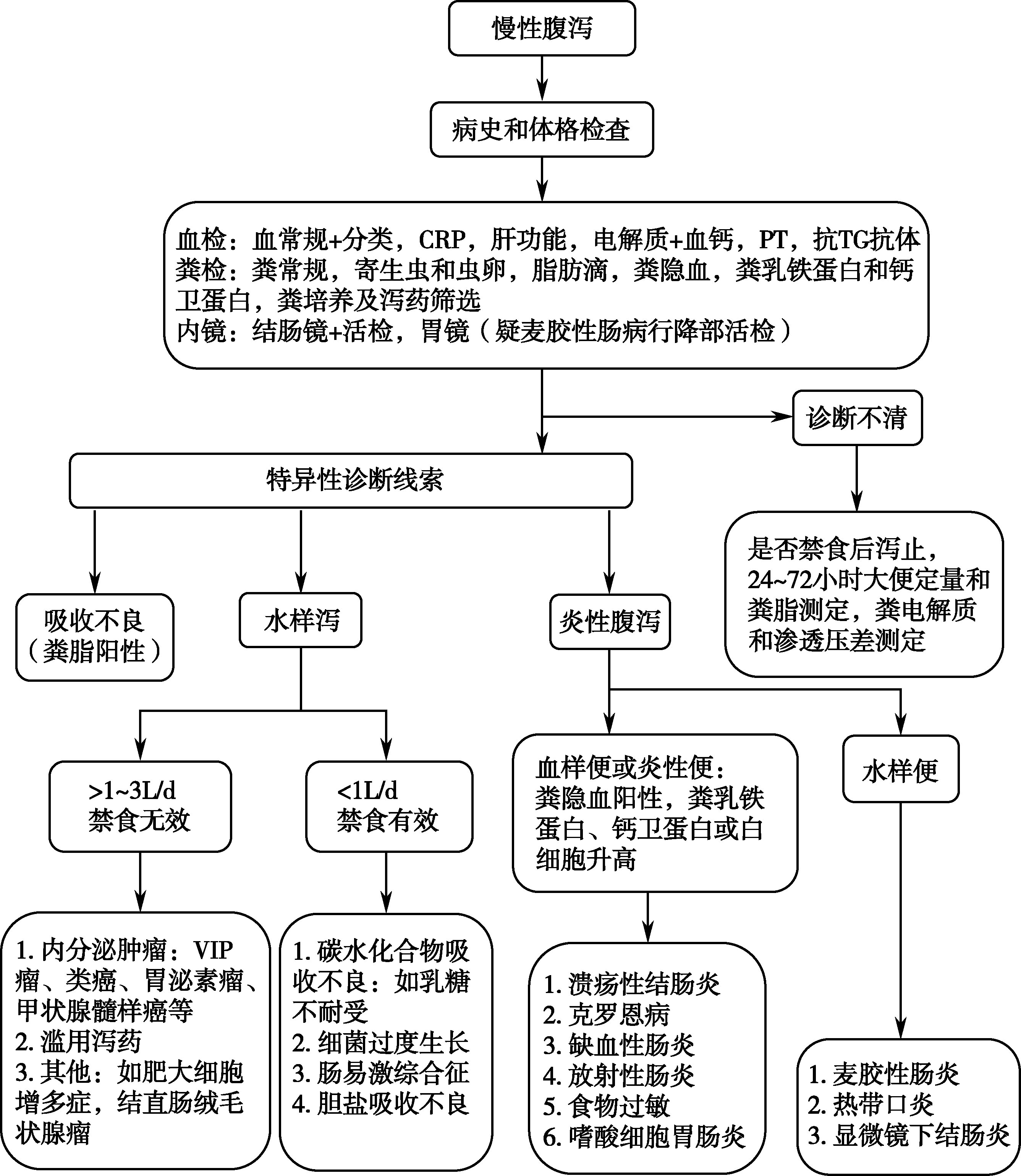
图15-3-4 慢性腹泻诊断流程
主要参考文献
1.Gail AH,Jonathan G,Miguel M.Chapter 41.Approach to the patient with diarrhea.Podolsky DK,Camilleri M,Fitz JG,et al.Yamada's Textbook of Gastroenterology,6th ed.Chichester:John Wiley&Sons,Ltd,2016,735-756.
2.DuPont HL.Acute infectious diarrhea in immunocompetent adults.N Engl J Med,2014,370(16):1532-1540.
3.Semrad CE.Chapter 140.Approach to the patients with diarrhea and malabsorption.Goldman L,Schafer AI.Goldman's Cecil Medicine.25th ed.Philadelphia,Pennsylvania:W.B.Saunders company,2016,918-935.
第四节
消化道出血

沈锡中 董玲
消化道出血(gastrointestinal bleeding)根据出血部位分为上消化道出血和下消化道出血。上消化道出血是指Treitz韧带以上的食管、胃、十二指肠和胰胆等病变引起的出血,包括胃空肠吻合术后的空肠上段病变。Treitz韧带以下的肠道出血称为下消化道出血。临床根据失血量与速度将消化道出血分为慢性隐性出血、慢性显性出血和急性出血。短时间内消化道大量出血称急性大出血常伴有急性周围循环障碍,死亡率约占10%。80%的上消化道出血具有自限性,下消化道出血死亡率一般不超过5%。小肠出血(small bowel bleeding)是相对少见的疾病,约占消化道出血的5%~10%,指经过常规上消化道内镜、下消化道内镜检查未发现病因的显性或者隐性消化道出血;通常出血部位在Vater壶腹部远端和回盲瓣近端之间。不明原因消化道出血(obscure gastrointestinal bleeding)是指经常规消化内镜检查(包括检查食管至十二指肠降段的上消化道内镜和肛门直肠至回盲瓣的结肠镜)和X线小肠钡剂检查(口服钡剂或钡剂灌肠造影)或小肠CT不能明确病因的持续或反复发作的出血。
【病因和分类】
消化道出血可因消化道本身的炎症、机械性损伤、血管病变、肿瘤等因素引起,也可因邻近器官的病变和全身性疾病累及消化道所致。现按消化道解剖位置分述如下。
(一)上消化道出血的病因
临床上最常见的出血病因是消化性溃疡、食管胃底静脉曲张破裂、急性糜烂出血性胃炎和胃癌,这些病因约占上消化道出血的80%~90%。
1.食管疾病
食管炎、食管溃疡、食管肿瘤、食管贲门黏膜撕裂、Cameron糜烂、物理/化学性损伤。
2.胃、十二指肠疾病
消化性溃疡、急性糜烂出血性胃炎、胃血管异常(动静脉畸形如Dieulafoy病等)、胃癌和胃其他肿瘤、急性胃扩张、十二指肠炎和憩室炎、膈疝、胃扭转、钩虫病、胃肠吻合术后的空肠溃疡和吻合口溃疡。
3.门静脉高压
食管胃底静脉曲张破裂出血、门脉高压性胃病。
4.上消化道邻近器官或组织的疾病
①胆道出血;②胰腺疾病累及十二指肠;③胸或腹主动脉瘤破入消化道;④纵隔肿瘤或脓肿破入食管。
5.全身性疾病在胃肠道表现出血
①血液病:白血病、再生障碍性贫血、血友病等;②血管性疾病;③结缔组织病:血管炎;④急性感染性疾病:流行性出血热、钩端螺旋体病;⑤尿毒症。
(二)下消化道出血病因
1.大肠癌和大肠息肉最常见。
2.肠道炎症性疾病 细菌性感染、寄生虫感染;非特异性肠炎,抗生素相关性肠炎,缺血性肠炎,放射性肠炎等。
3.血管病变 作为下消化道出血病因的比例在上升,如毛细血管扩张症、血管畸形、异位静脉曲张、肠血管瘤及血管畸形。
4.肠壁结构异常 如Meckel憩室,肠套叠等。
5.肛管疾病 痔疮、肛裂、肿瘤等。
(三)小肠出血病因
1.常见病因
(1)年龄<40岁:
炎症性肠病,Dieulafoy病,新生物,麦克尔(Meckel)憩室,息肉病。
(2)年龄>40岁:
血管扩张性病变,Dieulafoy病,新生物,非甾体抗炎药性溃疡。
2.罕见病因
过敏性紫癜(Henoch-Schoenlein purpura),小肠静脉曲张和(或)门脉高压性肠病,淀粉样变,蓝色橡皮泡痣综合征(blue rubber bleb nevus syndrome),弹性假黄瘤病(pseudoxanthoma elasticum),遗传性毛细血管扩张症(Osler-Weber-Rendu syndrome),AIDS伴发的卡波西肉瘤,Plummer-Vinson综合征,先天性结缔组织发育不全综合征(Ehlers-Danlos syndrome),遗传性息肉病综合征(家族性腺瘤性息肉病,Peutz-Jeghers病),恶性萎缩性丘疹,胆道出血,主动脉肠瘘(aortoenteric fistula)。
【临床表现】
消化道出血的临床表现取决于出血病变的性质、部位、失血量与速度,与患者的年龄、心肾功能等全身情况也有关。
(一)呕血、黑便和便血
是消化道出血特征性临床表现。上消化道急性大量出血多数表现为呕血,如出血速度快而出血量多,呕血的颜色呈鲜红色。少量出血则表现为黑便、柏油样便或粪便隐血试验阳性。出血速度过快,在肠道停留时间短,解暗红色血便。下消化道出血一般为血便或暗红色大便,不伴呕血。右半结肠出血时,粪便颜色为暗红色;左半结肠及直肠出血,粪便颜色为鲜红色。在空回肠及右半结肠病变引起少量渗血时,也可有黑便。
(二)失血性周围循环衰竭
消化道出血因循环血容量迅速减少可致急性周围循环衰竭,多见于短时期内出血量超过1000ml者。临床上可出现头昏、乏力、心悸、出冷汗、黑蒙或晕厥;皮肤湿冷;严重者呈休克状态。
(三)贫血
慢性消化道出血在常规体检中发现小细胞低色素性贫血。急性大出血后早期因有周围血管收缩与红细胞重新分布等生理调节,血红蛋白、红细胞和血细胞压积的数值可无变化。此后,大量组织液渗入血管内以补充失去的血浆容量,血红蛋白和红细胞因稀释而降低。平均出血后32小时,血红蛋白可稀释到最大程度。失血会刺激骨髓代偿性增生,外周血网织红细胞增多。
(四)氮质血症
在大量消化道出血后,血液蛋白的分解产物在肠道被吸收,以致血中氮质升高,称肠源性氮质血症。一般出血后1~2天达高峰,出血停止后3~4日恢复正常。
(五)发热
大量出血后,多数患者在24小时内常出现低热,持续数日至一周。发热的原因可能由于血容量减少、贫血、血分解蛋白的吸收等因素导致体温调节中枢的功能障碍。分析发热原因时要注意寻找其他因素,例如有无并发肺炎等。
【诊断】
(一)临床表现
1.消化道出血的识别
一般情况下呕血和黑便,呕吐物或粪便隐血强阳性,血红蛋白、红细胞计数下降常提示有消化道出血,但必须排除消化道以外的出血因素。首先应与口、鼻、咽部出血区别;也需与呼吸道和心脏疾病导致的咯血相区别。此外,口服动物血液、骨炭、铋剂和某些中药也可引起粪便发黑,应注意鉴别。
2.判别消化道出血的部位
呕血和黑便多提示上消化道出血,血便大多来自下消化道。上消化道大出血可表现为暗红色血便,如不伴呕血,常难以与下消化道出血鉴别。而慢性下消化道出血也可表现为黑便,常难以判别出血部位,应在病情稳定后急诊内镜检查。
3.出血严重程度的估计和周围循环状态的判断
每日出血量>5~10ml时,粪隐血试验可呈现阳性反应;每日出血量达50~100ml以上,可出现黑便。胃内积血量250ml时,可引起呕血。短时间出血量超过1000ml,可出现周围循环衰竭表现。对于上消化道出血的估计,主要动态观察周围循环状态,特别是血压、心率。如果患者由平卧位改为坐位血压下降(>15~20mmHg)、心率加快(>10次/分),提示血容量明显不足,是紧急输血的指征。患者血红细胞计数、血红蛋白及血细胞比容测定,也可作为估计失血程度的参考。
4.出血是否停止的判断
有下列临床表现,应认为有继续出血或再出血,须及时处理:①反复呕血,黑便次数增多,粪便稀薄,伴有肠鸣音亢进;②周围循环衰竭的表现经积极补液输血后未见明显改善,或虽有好转而又恶化;③红细胞计数、血红蛋白测定与血细胞比容持续下降,网织红细胞计数持续增高;④补液与尿量足够的情况下,血尿素氮再次增高。
5.出血病因和部位诊断
消化性溃疡患者多有慢性、周期性、节律性上腹疼痛或不适史。服用NSAIDs或肾上腺皮质激素类药物或处于严重应激状态者,其出血以急性胃黏膜病变为可能。有慢性肝炎、酗酒史、血吸虫等病史,伴有肝病、门脉高压表现者,以食管胃底静脉曲张破裂出血为最大可能。应当指出的是,肝硬化患者出现上消化道出血,有一部分患者出血可来自于消化性溃疡、急性糜烂出血性胃炎、门脉高压性胃病。45岁以上慢性持续性粪便隐血试验阳性,伴有缺铁性贫血、持续性上腹痛、厌食、消瘦,应警惕胃癌的可能性。50岁以上原因不明的肠梗阻及便血,应考虑结肠肿瘤。60岁以上有冠心病、心房颤动病史的腹痛及便血者,缺血性肠病可能大。突然腹痛、休克、便血者要立即想到动脉瘤破裂。黄疸、发热及腹痛伴消化道出血时,胆源性出血不能除外。儿童便血以Meckel憩室、感染性肠炎、血液病多见。
(二)辅助检查
1.内镜检查
内镜检查是消化道出血定位、定性诊断的首选方法,其诊断正确率达80%~94%,可解决90%消化道出血的病因诊断。内镜检查见到病灶后,应取活组织检查或细胞刷检,以提高病灶性质诊断的正确性,并根据病变特征判别是否继续出血或再出血的危险性,并行内镜下止血治疗。一般主张在出血24~48h内进行检查,称急诊内镜。急诊胃镜最好在生命体征平稳后进行,尽可能先纠正休克、补足血容量,改善贫血。胃镜检查可在直视下观察食管、胃、十二指肠球部直至降部,从而判断出血的病因、部位。结肠镜是诊断大肠及回肠末端病变的首选检查方法。重复内镜检查可能有助于发现最初内镜检查遗漏的出血病变。超声内镜、色素放大内镜等均有助于明确诊断,提高对肿瘤、癌前期病变等的诊断准确率。胶囊内镜具有安全、创伤小的优点,主要用于小肠疾病的诊断,对怀疑小肠出血的检出率约38%~83%。小肠镜具有可活检、可提供治疗(病灶标记、止血、息肉切除)等特点;目前有:①推进式小肠镜:为延长的上消化道内镜,可到达Treitz韧带远端70cm处;②深部小肠镜:有双气囊小肠镜、单气囊小肠镜、螺旋式小肠镜,还可以进行术中小肠镜检查。如操作人员技术熟练,理论上能检查整个肠道,可用于怀疑小肠出血的患者,检出率在48.9%~62.1%。对于胶囊内镜检查阳性的患者,再行小肠镜检查,将提高检出率至60%~90%。但若对胶囊内镜检查阴性的消化道出血患者,再次进行小肠镜检查,病变检出率仅为16.7%~37.8%。
2.X线钡剂检查
仅适用于出血已停止和病情稳定的患者,对急性消化道出血病因诊断的阳性率不高,多为内镜检查所代替。钡剂检查对于怀疑小肠出血的诊断率仅有3%~17%,目前并不推荐用于小肠出血的诊断。
3.放射性核素显像
急性显性消化道出血,其出血速度较慢(0.1~0.2ml/min),或者不确定有无活动性出血,未进行小肠镜或胶囊内镜检查者,可以使用 99m Tc标记的自体红细胞静脉注射后作腹部扫描成像,以探测标记物从血管外溢的证据;创伤小,可起到初步的定位作用,对Meckel憩室合并出血有较大诊断价值,并可指导进一步血管造影的时机。
4.血管造影
选择性血管造影对活动性大消化道出血(尤其是血流动力学不稳者)或者血管性病变的诊断及治疗具有重要作用,检出率40%~60%。根据脏器的不同可选择腹腔动脉、肠系膜动脉造影,出血速率>0.5ml/min时,可发现造影剂在出血部位外溢,定位价值较大。对确定下消化道出血的部位(特别是小肠出血)及病因更有帮助,也是发现血管畸形、血管瘤所致出血的可靠方法。但该检查是有创性操作;且有可能发生造影剂过敏、急性肾衰、血栓栓塞、感染和穿刺部位出血等并发症。
5.CT相关检查CT小肠成像(multiphasic CT enterography,CTE)
将肠腔充盈后使用多排CT扫描,可发现血管病变和肠道炎症改变;并提高小肠肿块尤其是黏膜来源的病变的检出率;可与胶囊内镜互补;常先行CTE,排除肠腔狭窄后再行胶囊内镜检查。CT血管造影(CT angiography,CTA)可准确检出并定位肠道血管性疾病,可检出0.3ml/min出血速度的病变。
6.剖腹探查
各种检查均不能明确原因时应剖腹探查。术中内镜是明确诊断不明原因消化道出血,尤其是小肠出血的可靠方法,成功率达83%~100%。另外,可在术中行选择性血管造影或注射亚甲蓝(美蓝),以帮助明确诊断(图15-3-5)。
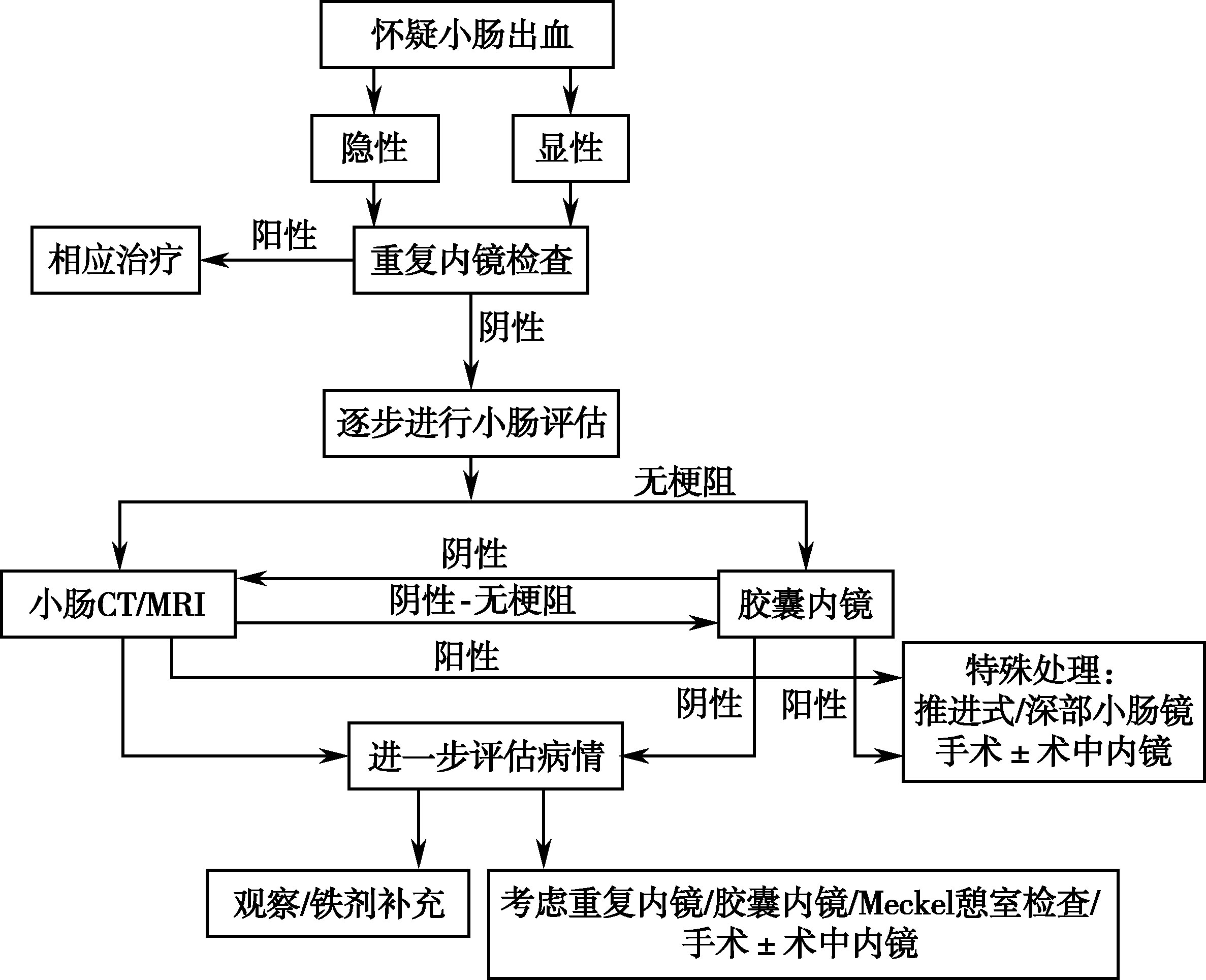
图15-3-5 小肠出血诊断流程
【治疗】
(一)一般治疗
卧床休息,严密监测患者生命体征,必要时行中心静脉压测定。观察呕血及黑便情况。定期复查血红蛋白浓度、红细胞计数、血细胞比容与血尿素氮。对老年患者视情况实施心电监护。
(二)补充血容量
及时补充和维持血容量,改善周围循环,防止微循环障碍引起脏器功能障碍,酌情输血,在配血同时可先用右旋糖酐或其他血浆代用品。紧急输血指征:改变体位出现血压下降、心率增快、晕厥;失血性休克;Hb<70g/L,血细胞比容<25%。但要避免输血输液量过多而引起急性肺水肿,以及对肝硬化门静脉高压的患者门静脉压力增加诱发再出血,肝硬化患者宜用新鲜血。
(三)上消化道大出血的止血处理
急性非静脉曲张上消化道大出血的处理,以消化性溃疡多见。
1.抑制胃酸分泌和保护胃黏膜
急性期静脉给予质子泵抑制剂,使胃内Ph>6.0,有助于消化性溃疡和急性胃黏膜病变的止血。无效时可加用生长抑素及其类似物,收缩内脏血管,控制急性出血。
2.内镜直视下止血治疗
经内镜直视下局部喷洒5%孟氏液(碱式硫酸铁溶液)、8%去甲肾上腺素液,凝血酶。也可在出血病灶注射1%乙氧硬化醇、1∶10000肾上腺素或立止血。内镜直视下高频点灼、激光、热探头、微波、止血夹等。
3.手术和介入治疗
内科积极治疗仍有大量出血危及患者生命时,需考虑外科手术治疗。少数患者严重消化道出血,无法进行内镜治疗,又不能耐受手术治疗时,可考虑选择性肠系膜动脉造影并血管栓塞治疗。
食管、胃底静脉曲张破裂出血的非外科治疗,参见本篇第八章第一节“肝硬化及其并发症”。
(四)下消化道大量出血的处理
基本措施是输血、输液、纠正血容量不足引起的休克。再针对下消化道出血的定位及病因诊断而做出相应治疗。如有条件内镜下止血治疗。对弥漫性血管扩张病变所致的出血,内镜下治疗或手术治疗有困难,或治疗后仍反复出血,可考虑雌激素/孕激素联合治疗。选择性动脉造影术后动脉内输注血管加压素可以控制90%的憩室和血管发育不良的出血,但有心血管方面的毒副作用。动脉内注入栓塞剂可能引起肠梗死,对拟进行肠段手术切除的病例,可作为暂时止血用。内科保守治疗无效,危及生命,有急诊手术指征。
(五)小肠出血的治疗
1.支持治疗,及早病因治疗。
2.药物治疗 病变部位不明或病变弥漫,不适用内镜治疗、手术治疗、血管造影栓塞治疗及治疗无效者,可考虑药物治疗。①性激素:如炔雌醇和炔诺酮等,但其预防消化道血管扩张出血复发的疗效仍存在争议,心血管不良反应较大;目前认为对于小肠出血的治疗没有作用;②生长抑素及其类似物(如奥曲肽):其减少出血的机制可能与抑制血管生成和内脏血流有关,对胃肠道毛细血管扩张和蓝色橡皮泡痣综合征引起的小肠出血有一定的治疗作用;③沙利度胺:为谷氨酸衍生物,对血管扩张引起的小肠出血有效,可能与其抗血管生成作用有关。但存在一定的不良反应,如周围神经病变、深静脉血栓等。
3.内镜下治疗 对双气囊小肠镜检查发现病变者,可同时治疗小肠血管损害病变且维持缓解时间较长。
4.血管造影下栓塞等治疗 主要用于急性大量小肠出血。方法主要包括选择性动脉内加压素治疗、超选择性微线圈栓塞或合用明胶海绵或聚乙烯醇栓塞等。
[附]食管贲门黏膜撕裂(Mallory-Weiss综合征)
食管贲门黏膜撕裂是食管下端和胃连接处的黏膜纵形裂伤,并发上消化道出血,一般出血有自限性,如累及小动脉可引起严重出血。1929年Mallory和Weiss首先从尸体解剖中认识本症。1956年Hardy首次应用内镜作出诊断。发病主要是腹内压力或胃内压骤然升高,促使黏膜撕裂。恶心或呕吐是胃内压升高的主要因素,包括妊娠呕吐、食管炎、急性胃炎、放置胃管、内镜检查、糖尿病酮症和尿毒症等都可引起剧烈呕吐。其他凡能引起胃内压升高的任何情况均可发生食管贲门黏膜撕裂,如剧烈咳嗽、酗酒、用力排便、举重、分娩、麻醉期间的严重呃逆、胸外按摩、喘息状态、癫痫发作、腹部钝性挫伤等。本症主要病理为食管远端黏膜和黏膜下层的纵形撕裂。裂伤多为单发,但也可有3~4处之多。裂伤长0.3~4cm。基底部为血凝块和黄色坏死组织所覆盖,边缘清楚,黏膜轻度水肿。本症诊断首先依靠病史,有引起胃内压骤升的因素,有食管裂孔疝者更要考虑本症。当前最有效的诊断手段是急诊内镜检查。钡餐X线检查价值较小。腹腔动脉造影也有助于诊断。如小量出血一般可自限止血,必要时可用去甲肾上腺素加入生理盐水中灌入食管胃腔,促使黏膜下血管收缩。也有主张在急诊内镜诊断的同时,对出血灶作电凝或光凝止血。少数出血量大而不止者,需外科做裂伤连续缝合术止血。如去除诱因,术后一般无复发可能。
主要参考文献
1.Gerson LB,Fidler JL,Cave DR,et al.ACG Clinical Guideline:Diagnosis and Management of Small Bowel Bleeding.Am J Gastroenterol,2015,110(9):1265-1287.
2.Loren L,Chatper 57.Gastrointestinal Bleeding.In Kasper DL,Fauci AS,Hauser SL,et al.Harrison's Principles of Internal Medicine.19th ed.New York:McGraw-Hill Education 2015:276-279.
第五节
腹水

郭津生
腹腔内液体积聚超过300ml就称为腹水(ascites)。
【病因】
腹水的病因多样(表15-3-6)。肝硬化门脉高压是腹水形成的最主要病因,约占所有腹水成因的85%,而肝硬化患者腹水的出现是其从代偿期进展到失代偿期的标志。引起腹水的病因还包括其他肝脏疾病如急性肝衰竭、窦前(门静脉血栓形成)和窦后性(Budd-Chiari综合征、缩窄性心包炎)门脉高压、肝脏广泛转移性癌,或非肝病病因如恶性肿瘤(腹膜转移癌)、腹膜结核、心功能不全、胰腺炎、肾病综合征,以及少见原因如淋巴管瘘、POEMS综合征等。5%患者具有混合性因素,如腹膜结核合并肝硬化、或肝硬化合并心功能不全。
【发病机制】
(一)局部因素
门静脉压力增高,导致肝窦和肠系膜毛细血管压力升高,体液从这两个部位漏出并超出淋巴管和胸导管的引流能力,过多的体液从肝包膜漏至腹腔。
(二)全身因素
1.水钠潴留
周围血管扩张和动脉有效血容量下降促发神经体液因素,通过反射性刺激交感神经系统和肾素-血管紧张素-醛固酮系统,刺激血管加压素的释放,导致持续性肾水、钠潴留和腹水形成。该机制可运用于肝硬化和非硬化性门脉高压,以及非肝性腹水中的充血性心衰、肾病综合征等。
2.低白蛋白血症
肝脏合成白蛋白功能减退或者由于大量白蛋白从肾脏或肠道丢失导致血清白蛋白降低,引起血浆胶体渗透压下降,水分趋于从血浆向第三间隙积聚。
3.腹腔内渗透压平衡改变
如腹腔内肿瘤转移灶、结核、结缔组织病(如系统性红斑狼疮所致浆膜炎)时富含蛋白的液体渗出到腹腔内。
4.腹膜化学性灼伤
胆胰系统损伤,胆汁或胰液漏入腹腔。
5.膜通透性增高和淋巴管阻塞
如尿毒素血症和血透患者的肾源性腹水。
【临床表现】
有不同程度的腹胀,少尿,严重者可有呼吸困难、活动受限等症状。体征包括直立下腹部、仰卧时侧腹部(呈蛙腹状)膨隆。叩诊患者仰卧位时腹部侧面鼓音-浊音交界面高于正常。移动性浊音阳性(对腹水诊断的敏感性83%,特异性56%)或有液波震颤提示腹水超过3000ml。大量腹水可并发各种疝(如脐疝、腹股沟疝),亦可并发胸腔积液(特别是右侧胸腔积液)和自发性腹膜炎。
【实验室检查】
(一)腹水分析
①常规和生化检查,包括腹水细胞计数和分类、腹水总蛋白和白蛋白。如只获取极少量腹水应先送检细胞计数和分类。②肿瘤标志物检查:AFP检查有助于肝癌诊断;CEA测定有助于胰腺和肠道肿瘤诊断。血清和腹水CA125对腹水的鉴别诊断没有价值。③腹水ADA:阳性提示结核性腹膜炎可能。④腹水细菌培养和药物敏感性测定:如腹水多形核计数≥250×10 6 /L时提示感染性腹水,在抗生素使用前使用需氧和厌氧菌血培养瓶床旁无菌采集20ml腹水进行细菌培养,部分标本可培养出细菌。多种菌阳性提示消化道穿孔可能。⑤腹水病理细胞:有助于肿瘤诊断,如大量腹水离心后送检敏感性增高。⑥其他:淀粉酶、LDH、胆红素、甘油三酯等。
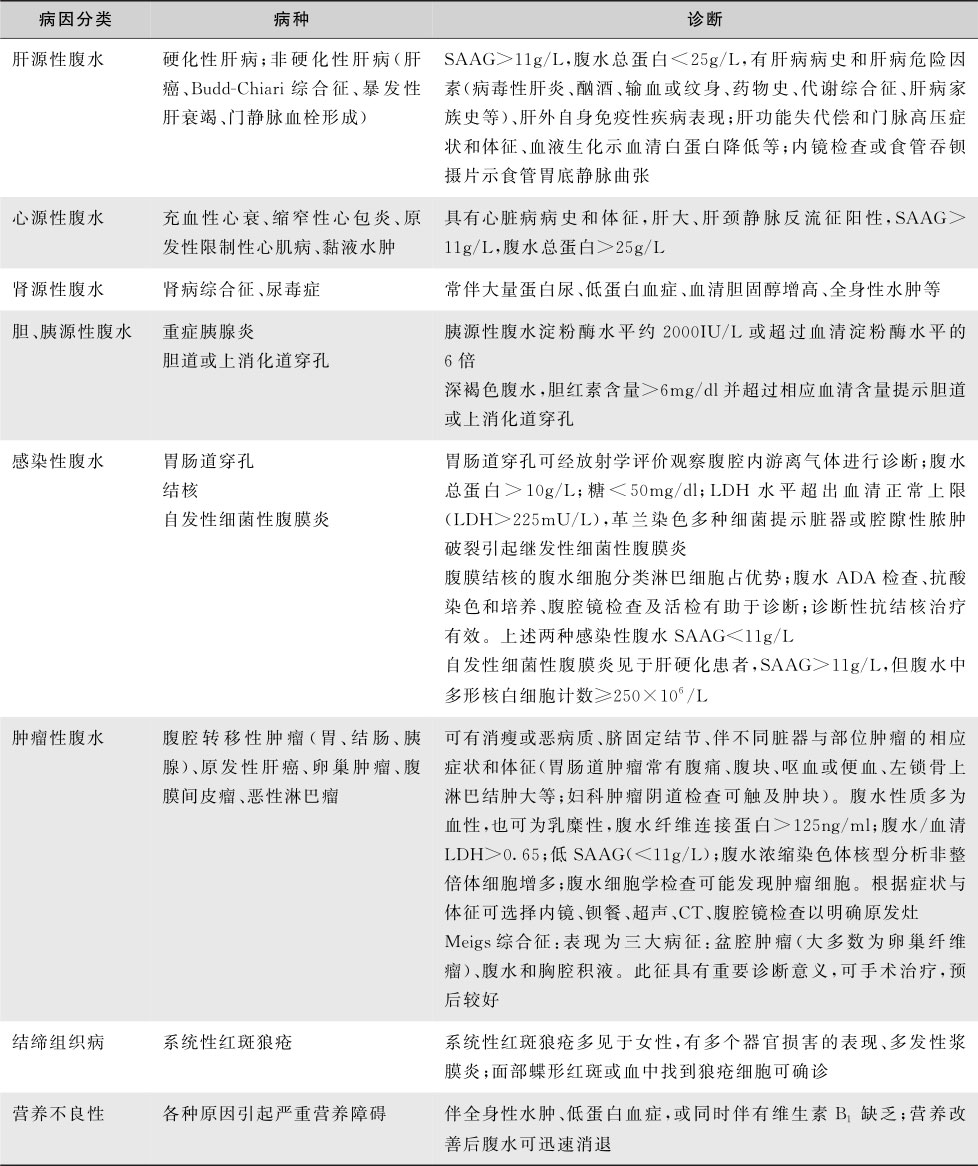
表15-3-6 腹水的病因分类及诊断
乳糜性和血性腹水是两种具有特殊外观和成分的腹水。①乳糜性腹水:呈乳白色,不透明,高甘油三酯含量(>200~1000mg/dl,乙醚试验和苏丹Ⅲ染色阳性)。见于腹腔内肿瘤、腹腔内炎症(包括结核、肠系膜淋巴结炎等)、腹膜后肿瘤、胸导管阻塞(炎症、丝虫病、梅毒)、外伤或手术。乳糜性腹水需与假性乳糜性腹水鉴别。假性乳糜性腹水也呈乳糜样外观,见于慢性腹腔化脓性感染,脓细胞脂肪变性破坏。化学成分为卵磷脂、胆固醇与小量蛋白质和脂肪颗粒。乙醚试验阴性。②血性腹水:呈粉红色或血水样,含大量红细胞[(>(10~20)×10 9 /L);蛋白>30g/L,见于肝癌结节破裂、肝外伤性破裂、急性门静脉血栓形成以及肝外疾病如异位妊娠、黄体破裂、自发性或创伤性脾破裂、急性出血坏死性胰腺炎、腹腔内肿瘤、结核性腹膜炎、Meigs综合征。
(二)血清腹水白蛋白梯度(serum-ascites albumin gradient,SAAG)
腹水分析获得腹水白蛋白定量,同时检查血清白蛋白以计算血清-腹水白蛋白梯度,有助于识别病因和指导治疗。SAAG≥11g/L,腹水蛋白<25g/L,考虑肝硬化门脉高压性腹水。SAAG≥11g/L,腹水蛋白≥25g/L,考虑心源性门脉高压性腹水。SAAG<11g/L,基本上可以排除门脉高压性腹水,应该考虑肿瘤性和结核等引起的腹水(表15-3-6)。
【诊断与鉴别诊断】
(一)诊断
1.腹水的诊断
可通过病史和局部体检发现。影像学检查和诊断性腹穿可证实腹水的存在,超声检查是最经济、常用和首选的无创诊断方法,可检出最少100ml的腹水。
腹腔穿刺是明确腹水病因的最快速有效的方法,应在所有新发生和在短期内腹水明显增加的患者中进行。通过腹穿可早期诊断和治疗亚临床型腹水感染,降低死亡率和致残率。腹穿少见并发症为腹壁血肿、血腹(见于血小板缺乏症及凝血异常的患者)和腹穿针引起的肠穿孔。
2.腹水的病因诊断
简要诊断流程见图15-3-6。辅助检查如钡餐造影、CT与MRI、血管造影以及内镜检查等可助病因诊断。腹腔镜可对腹膜和腹内肿瘤进行活检,适应证为原因不明的腹水、腹痛和急腹症、原因不明的腹痛和腹块等。
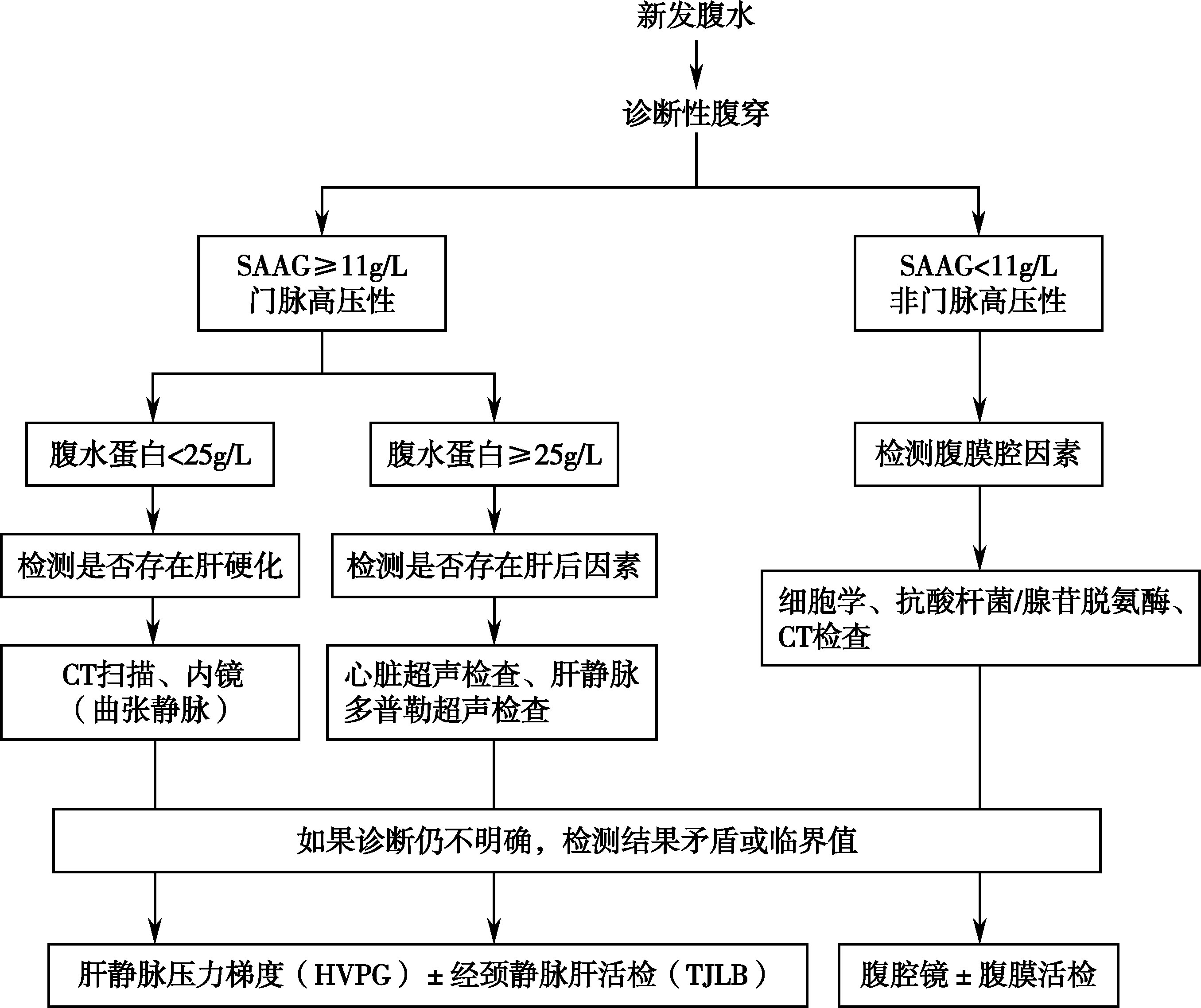
图15-3-6 腹水的病因诊断流程
(二)鉴别诊断
1.腹型肥胖
腹壁及身体其他部位脂肪堆积,腹部呈球形,脐下陷,移动性浊音阴性。影像学检查腹水阴性。
2.腹腔内占位性病变
(1)黏液瘤:
腹部膨胀,移动性浊音阴性,影像学检查结合穿刺活检有助于鉴别。
(2)巨大卵巢囊肿:
可引起高度腹部膨胀,可触知囊肿轮廓;前腹叩诊浊音,腹侧部呈鼓音;波动感;尺压试验阳性;脐孔有上移现象;阴道检查提示囊肿起源于卵巢;B超、CT等检查可帮助鉴别。
(3)巨大腹腔囊肿或假囊肿:
来源于肝脏、肾脏、胰腺、大网膜或腹膜后,可达到一定的程度甚至在腹穿时获得异常液体而与腹水相混淆。病变特点:①起病缓慢,无明显全身症状;②腹部膨大两侧不对称;③腰腹部(一侧或两侧)叩诊呈鼓音,可听到肠鸣音;④X线钡餐透视发现胃肠道受压现象,影像学等检查可证明囊肿起源于腹腔内或腹膜后器官。
3.其他
如腹内胃肠道积气、妊娠等。
【治疗】
主要根据病因选择不同的治疗方法。对高SAAG、有门脉高压的腹水患者主要使用利尿剂和限盐治疗,一般不必限水,除非尿钠浓度小于125mmol/L;还有一些二线治疗方案针对难治性腹水(见本篇第八章第一节“肝硬化及其并发症”)。肿瘤性腹水的治疗主要是采用腹穿、置管引流等方法缓解症状,此外可考虑全身和(或)腹腔内化疗,一般的利尿剂和水钠限制治疗往往无效。乳腺及卵巢肿瘤尽可能手术切除原发灶。对脏器穿孔引起的腹膜炎和腹水需手术治疗和抗生素治疗。
腹壁疝患者可使用适当大小的腹带和疝托,咳嗽或用力时用手托持疝袋以减少疼痛和疝增长;如疝不能减小或关闭应及时就医。脐疝绞窄或破裂的紧急修复需由对原发病(如肝硬化)有经验的外科医生进行;肝硬化腹水引起的脐疝修复需权衡风险和益处,应在经药物、TIPS、肝移植等治疗控制腹水和改善总的状况后进行。
肝性胸腔积液的处理一线治疗也为饮食限钠和使用利尿剂,如进展为难治性则考虑二线治疗如TIPS;胸腔插管引流在肝性胸腔积液禁忌。
[附]腹腔隔室综合征
健康状况下腹腔内压力0~5mmHg。腹腔隔室综合征(Abdominal compartment syndrome,ACS)是一系列引起腹腔内压力急剧上升(可达20mmHg以上)伴新发生的器官衰竭等严重病理生理的复杂病况:当腹壁顺应性下降(如腹膜炎,烧伤)、腹腔内容量急剧上升(如外伤后出血)、出现大量胸腔积液、腹水,使腹内压力升高到一定限度时,继发低血容量、血液浓缩、循环呼吸功能障碍、电解质紊乱、肝肾功能障碍和血栓形成等多器官受累表现,致死率和致残率极高。见于腹部外伤和手术、烧伤、重症胰腺炎、急性门静脉血栓形成、卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)等。
早期识别对防止和逆转全身性反应有至关重要的作用。ACS治疗原则是治疗基础病、降低腹压、防止和治疗因腹压增高引起的器官失功能和衰竭。降低腹压的方法包括:①改善腹壁依从性:镇静/止痛;使用神经肌肉阻滞剂;体位(平卧位)。②去除腔内容物:鼻胃减压;直肠减压/灌肠;胃/结肠动力药物。③去除腹腔内积聚液体:经皮减压(腹穿)。④纠正液体渗出正平衡:限制液体;利尿剂;胶体;血液透析/超滤等。
主要参考文献
1.Runyon BA.Introduction to the revised American Association for the Study of Liver Disease.Practice Guideline management of adult patients with ascites due to cirrhosis 2012.Hepatology,2013,57(4):1651-1653.
2.Garcia-Tsao G.Chapter 106,Ascites and its complications//Podlsky DK,Camillenivn M,Fitz JG,et al.YAMADA's Textbook of Gastroenterology.6th ed.West Sussex:John Wiley&Sons Ltd,2015:2087-2106.
3.Malbrain ML,De Keulenaer BL,Oda J,et al.Intra-abdominal hypertension and abdominal compartment syndrome in burns,obesity,pregnancy,and general medicine.Anaesthesiol Intensive Ther,2015,47(3):228-240.

