第八节
EGFR信号通路

一、表皮生长因子受体信号通路简介
表皮生长因子受体(epidermal growth factor receptor,EGFR),也称为erbB1或HER1,是HER家族成员之一,该家族还包括 HER2(erb B2,NEU)、HER3(erbB3)及 HER4(erb B4)。EGFR广泛分布于哺乳动物上皮细胞、成纤维细胞、胶质细胞、角质细胞等细胞表面,EGFR信号通路调控细胞的生长、增殖和分化等生理过程发挥重要的作用。EGFR是一种糖蛋白,属于酪氨酸激酶型受体,这种跨膜受体EGFR有三个结构域:胞外配体结合区,跨膜区和胞内激酶区。
二、EGFR信号通路的功能
EGFR被EGF和TGF-α(transforming growth factor α)或其他配体激活后,由单体转化为二聚体[同源二聚体或EGF相关性受体(酪氨酸激酶家族不同成员)结合成异源二聚体],激活胞内的激酶通路,使EGFR酪氨酸残基(Y992、Y1045、Y1068、Y1148、Y1173)发生自磷酸化作用,进而激活下游信号磷酸化。EGFR活化驱动一系列信号途径。主要有两条通路参与调节细胞增殖和存活:PI3K/AKT/mTOR信号途径和RAS/RAF/MEK/MAPK信号途径(图2-4-9)。这两条信号途径参与调节细胞周期,引起细胞增殖、凋亡、迁移、存活以及血管生成等。
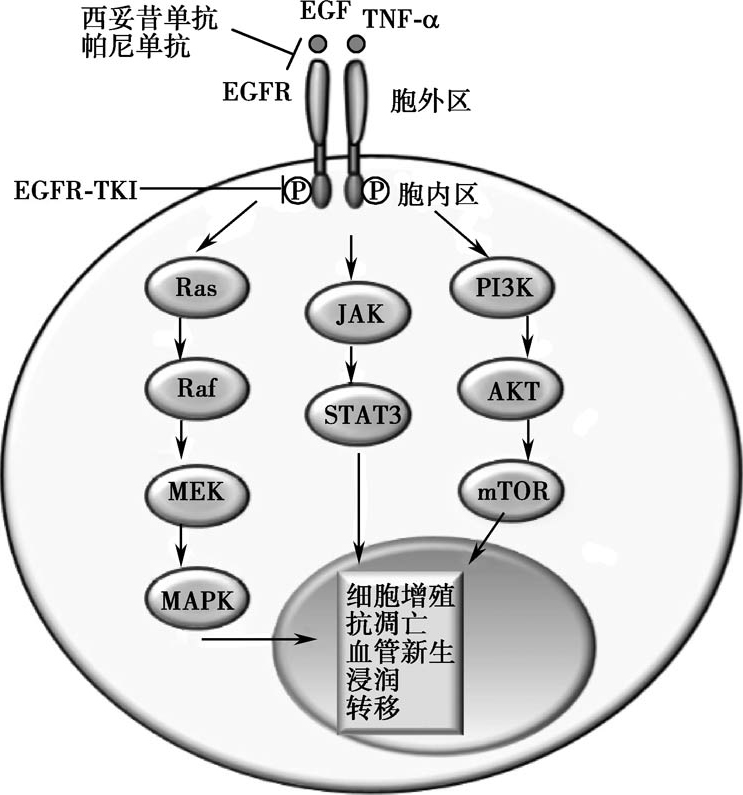
图2-4-9 EGFR信号通路
三、EGFR与疾病
EGFR以过量和(或)突变形式存在于各种肿瘤中,导致肿瘤细胞生长和增殖。EGFR在肾癌、肺癌、前列腺癌、胰腺癌、乳腺癌等实体肿瘤中高表达。许多肿瘤中EGFR发生缺失、突变和重排等异常,导致EGFR的持续活化以及受体下调机制的破坏。如EGFR信号转导通路中与配体结合的EGFR被内吞入细胞,信号通路即终止,受体将被降解或再循环到细胞膜表面。以EGFR作为新药设计的靶点已有数十种进入市场和临床试用中。
四、针对EGFR的靶向治疗
近年来EGFR在肿瘤中的作用以及针对EGFR的靶向治疗备受关注。基于EGFR基因激酶域基因突变理论研制的针对EGFR酪氨酸激酶的靶向药物为非小细胞肺癌(NSCLC)患者带来了新的治疗契机。抗EGFR的靶向治疗主要有两种方式:EGFR单克隆抗体以及小分子EGFR酪氨酸激酶拮抗剂(EGFR-TKI),后者首先应用于临床。西妥昔单抗(cetuximab)和帕尼单抗(panitumumab)是人/鼠嵌合或完全人源性抗EGFR胞外域单克隆抗体,它们通过抑制活化的配体与EGFR的结合,阻止激活下游信号通路的激活、抑制细胞的增殖、侵袭、转移。两种抗体分别在2004年和2007年获得美国食品与药品管理局的批准用于治疗结直肠癌。TKIs是人工合成的小分子,通过与ATP竞争性结合EGFR-TK域。TKIs通过结合酪氨酸激酶,阻断EGFR分子内自身磷酸化及酪氨酸激酶活化,阻止胞内下游信号途径的活化。应用最广的EGFR-TKIs是吉非替尼(gefitinib)和厄洛替尼(erlotinib)。EGFR突变可使TK受体组成性活化,并与EGFRTKIs敏感性相关。

(资源10) EGFR信号通路(彩图)


