实验2.2
燃烧热的测定
一、目的
1.通过物质的燃烧热的测定,掌握有关热化学实验的一般知识和测量技术,了解氧弹式量热计的原理、构造和使用方法。
2.掌握燃烧热的定义,理解恒压热与恒容热的差别及相互关系。
3.学会应用图解法校正温度改变值。
二、基本原理
燃烧热是指1摩尔物质完全燃烧时所放出的热量,在恒容条件下测得的燃烧热为恒容热( Q V ),恒容热等于这个过程的热力学能变化(Δ U )。在恒压条件下测得的燃烧热称为恒压热( Q p ),恒压热等于这个过程的焓变化(Δ H ),若把参加反应的气体和反应生成的气体作为理想气体处理,则存在下列关系式:

式中:Δ n 为生成物和反应物气体的物质的量之差; R 为摩尔气体常数; T 为反应时的热力学温度。
若测得某物质恒容热或恒压热中的任何一个,就可根据(2.2-1)式计算另一个数据。须指出,化学反应的热效应(包括燃烧热)通常是用恒压热效应(Δ H )来表示的。
三、仪器与试剂
量热仪、氧气钢瓶、充氧仪、压片机、万用表、分析天平、电子台秤各1台(套)。
苯甲酸(A.R.)、蔗糖(A.R.)、棉线和金属丝若干。
四、实验步骤
1.水当量的测定
(1)压片前先检查压片用钢模,若发现钢模有铁锈油污或尘土等,必须擦净后,才能进行压片,用天平称取约0.8 g苯甲酸,从模具的上面倒入已称好的苯甲酸样品,徐徐旋紧压片机的螺杆,直到将样品压成片状为止。抽出模底的托板,再继续向下压,使模底和样品一起脱落,将此样品表面的碎屑除去;另取一段棉线和金属丝(10 cm),在分析天平上分别准确称量记录好数据,用棉线将金属丝系在苯甲酸样品上,金属丝在样品上不可短路,在分析天平上准确称量记录好数据,此样品供测定燃烧热用。
(2)拧开氧弹盖,将氧弹内壁擦净,特别是电极下端的不锈钢接线柱更应擦干净,用万用表欧姆挡检查两电极是否通路,若通路,将样品的金属丝两端分别接在两个电极上,注意金属丝不能与坩埚相接触,旋紧弹盖再用万用表检查两电极之间是否通路,若通路则可充氧气。
使用高压钢瓶时必须严格遵守操作规则。将氧弹放在充氧仪台架上,拉动扳手充入氧气至1.2~1.5 MPa。氧弹结构见图2.2-1。充好氧气后,再用万用表检查两电极间是否通路,若通路可进行下步操作,否则将氧弹放气,检查断路原因,重新进行此步操作。
(3)用容量瓶加3 000 mL水于盛水桶内,将氧弹放入水桶内,把点火导线插在氧弹的两个电极上,装上搅拌桨,盖上盖子,先将数字贝克曼温度计测量探头插入量热计的恒温水夹套内,测量环境的温度,然后将数字贝克曼温度计测量探头插入盛水桶内。
(4)将仪器安装好后,首先检查控制箱的点火按钮不在点火的位置上,然后接通控制箱的电源,开始搅拌,温度稳定后开始读点火前最初阶段的温度,每隔一分钟读一次,读10个间隔,读数完毕,立即按下点火按钮约3~5 s,点火指示灯熄灭表示点火成功(如不着火可适当增大电流,重新点火,如点火失败,关闭电源,取出氧弹,放气后检查失败原因,再重新进行以上操作步骤),将点火按钮搬回原位置,然后每半分钟读一次温度读数,至两次读数之差小于0.005℃后,每隔一分钟再读取最后阶段的10次读数,便可停止实验。温度上升很快阶段的温度读数可较粗略,最初阶段和最后阶段则需精密到0.002℃。
(5)停止实验后关闭搅拌器,先取下数字贝克曼温度计测量探头,再打开量热计盖,取出氧弹将其拭干,打开放气阀门缓缓放气。放完气后,拧开弹盖,检查燃烧是否完全。若弹内有炭黑或未燃烧的试样时,则应认为实验失败。若燃烧完全,量取燃烧后剩下的引火丝并在天平上称量,并用少量蒸馏水洗涤氧弹内壁,最后倒去桶中的水,用毛巾擦干全部设备,留待进行下一次实验。量热计参见图2.2-2。微机操作程序见表2.2-1。
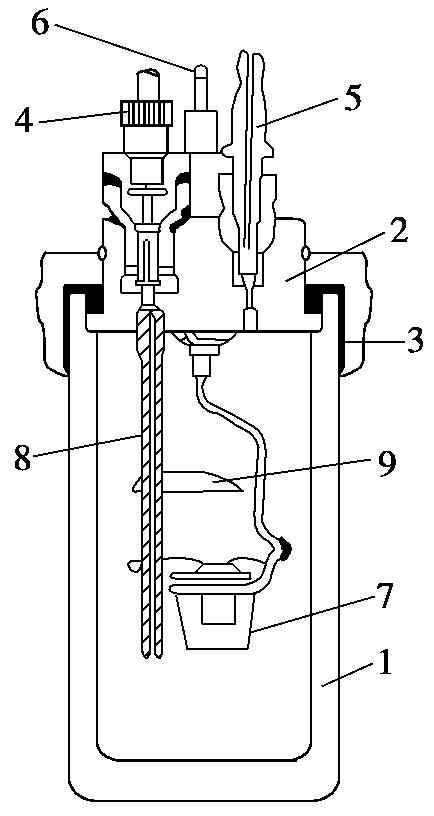
图2.2-1 氧弹的构造
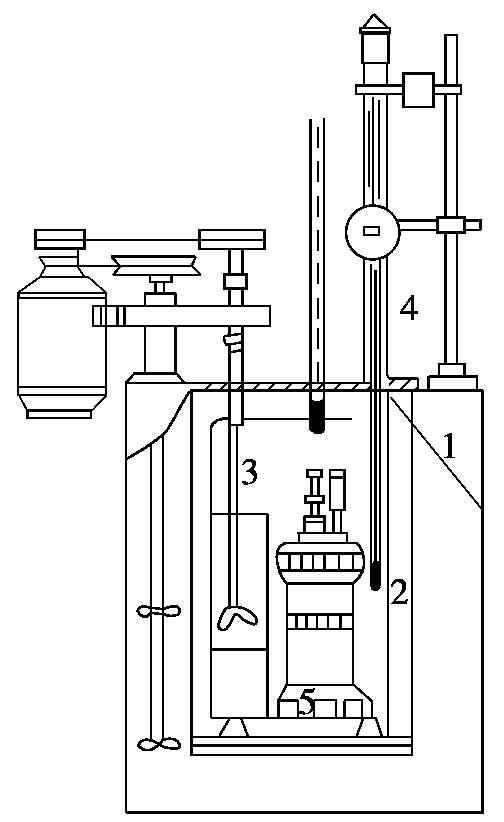
图2.2-2 量热计示意图
1.厚壁圆筒;2.弹盖;3.螺帽;4.进气孔;5.排气孔;6.电极;
7.燃烧皿;8.电极(同时也是进气管);9.火焰遮板
1.温度夹套;2.挡板;3.盛水桶;
4.温度传感器;5.氧弹
2.蔗糖的燃烧热 Q V 的测定
称取约1.2 g蔗糖代替苯甲酸重复上述实验。微机操作规程见表2.2-1和表2.2-2。
表2.2-1 热容量测定微机操作说明
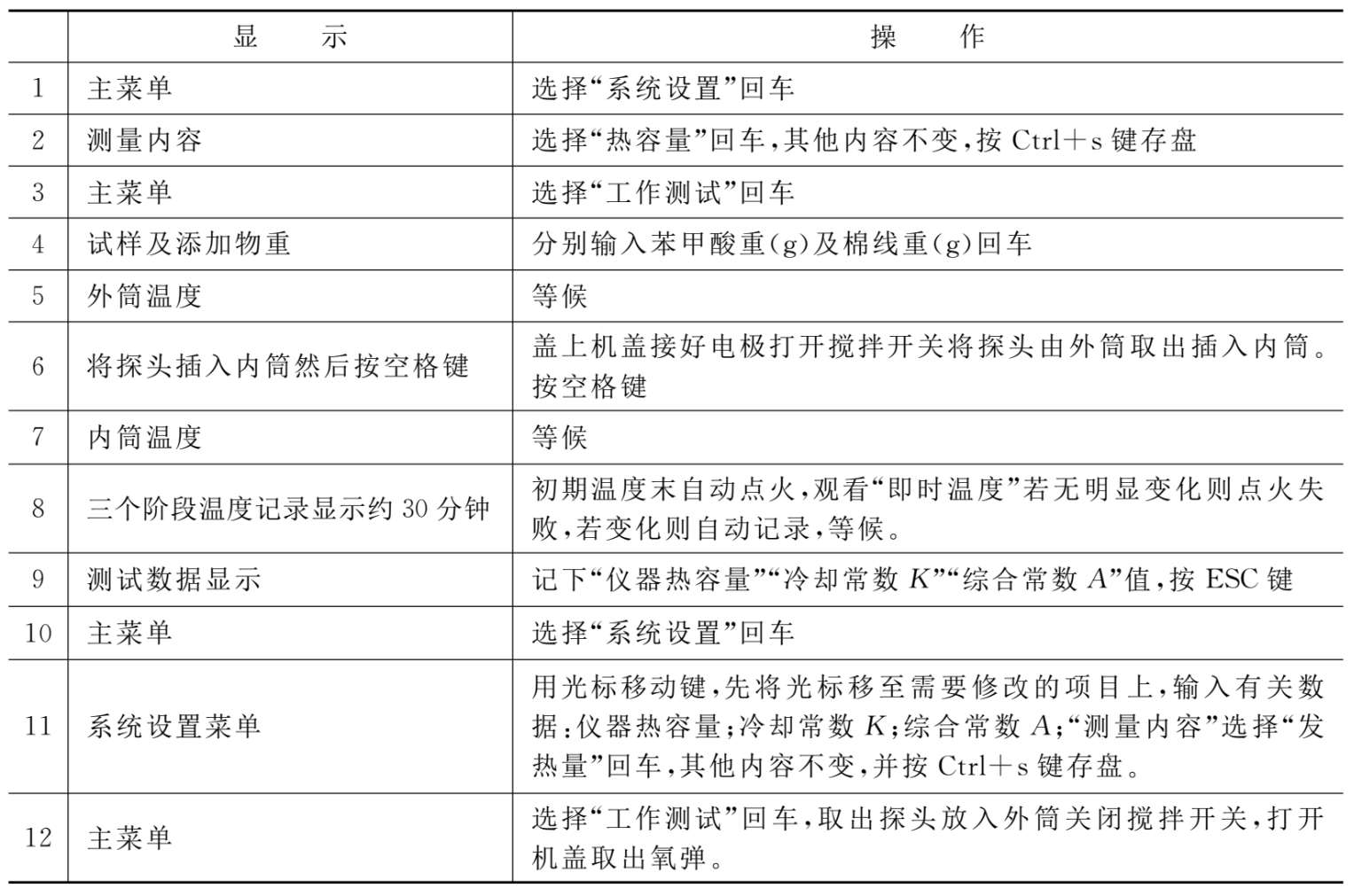
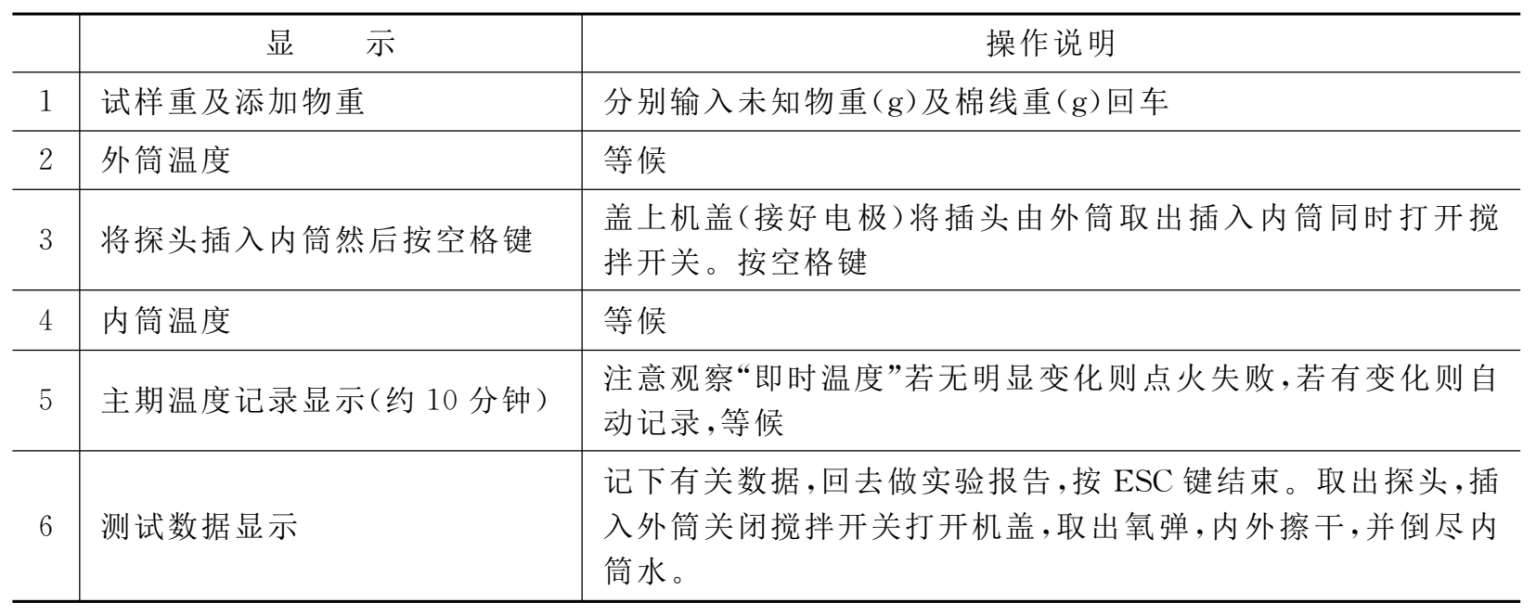
表2.2-2 未知物热值测定微机操作说明
3.WZR-1B型微电脑量热计实验操作步骤
(1)试样准备
①称取样品(苯甲酸为0.8 g,冰糖为1.2 g),压片,将精确称量好的棉线和金属丝中间部分相互缠绕5圈,将棉线系在压好的苯甲酸片上,再称重。注意金属丝在样品上不能短路,将金属丝两头分别放入氧弹头的点火电极的卡口内,推下卡环,样品上的金属丝不可与坩埚相接触,氧弹头放入弹筒内,旋紧氧弹盖。
②使用高压钢瓶时必须严格遵守操作规则。在实验指导教师的指导下,打开钢瓶总阀,调节减压阀,使得减压表指示为1.2 MPa~1.5 MPa范围内即可。
③用充氧器充氧,轻压充氧悬臂,保持5秒钟,松开充氧悬臂,氧弹用放气针放气。再次用充氧器充氧,当充氧器上的表压与钢瓶的减压表表压基本相同后,松开充氧悬臂。将氧弹放入仪器的内筒。
(2)系统设置
①打开仪器电源,进入初始界面。
②按系统设置键,检查系统设置参数(参数具体数据请看黑板)。返回初始化界面。
注意:以上数据已经填好,不要改动。
(3)初始化仪器参数
试样编号:学号-1,学号-2,类推。
试样质量:输入试样质量,单位为g。
点火丝质量:输入点火丝质量,单位为g。
添加物质量:如没有助燃的物质添加不用输入,单位为g。
全硫含量、含氢量、收到水分和分析水分根据样品情况添加。
(4)试验开始
记录取初始温度,按实验开始键,实验开始。开始注水,注水后进入曲线检测界面,注意观察曲线走势,点火成功或失败仪器会自动运行和停止,实验结束,显示实验结果,打印实验数据,取出氧弹,放气,观察燃烧是否完全,将剩余的金属丝称重。返回初始化界面,准备下个实验。
五、数据处理
1.用雷诺图解法求出苯甲酸、蔗糖燃烧前后的温度差Δ T 。
2.求出蔗糖的恒压燃烧热(计算热量时需减去引火丝和棉线燃烧放出的热量)。
3.结合实验仪器和计算公式,讨论哪些因素容易造成误差?如果要提高实验的准确度应从哪几方面考虑?
六、思考题
1.说明恒容热效应( Q V )和恒压热效应( Q p )的相互关系。
2.在这个实验中,哪些是体系,哪些是环境?实验过程中有无热损耗?这些热损耗对实验结果有何影响?
3.加入内筒中水的温度为什么要选择比外筒水温低?低多少为合适?为什么?
七、讨论
1.在精确测量中,点火丝的燃烧热和氧气中含氮杂质的氧化所产生的热效应等都应从总热量中扣除。前者可将点火丝在实验前称重,燃烧后小心取下,用稀盐酸浸洗,再用水洗净、吹干后称重,求出燃烧过程中失重的量(燃烧丝的热值为 6 695
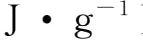 。后者可用0.1
。后者可用0.1
 NaOH溶液滴定洗涤氧弹内壁的蒸馏水(在燃烧前先在氧弹中加入0.5 mL水),每毫升0.1
NaOH溶液滴定洗涤氧弹内壁的蒸馏水(在燃烧前先在氧弹中加入0.5 mL水),每毫升0.1
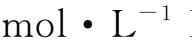 NaOH溶液相当于5.983 J(放热),从而可计算出氧气中含氮杂质氧化所产生的热效应。
NaOH溶液相当于5.983 J(放热),从而可计算出氧气中含氮杂质氧化所产生的热效应。
2.用雷诺图(温度-时间曲线),确定实验中的Δ T ,如图2.2-3(a)所示。
图中 b 点相当于开始燃烧的点, c 为观察到的最高点的温度读数,作相当于环境温度的平行线 TO ,与 T - t 线相交于 O 点,过 O 点作垂直线 AB ,此线与 ab 线和 cd 线的延长线交于 E , F 两点,则 E 点和 F 点所表示的温度差即为欲求温度的升高值Δ T 。图中 EE′ 为开始燃烧到温度升至环境温度这一段时间Δ t 1 内,因环境辐射和搅拌产生能量所造成量热计温度的升高,必须扣除。 FF′ 为温度由环境温度升到最高温度 c 这一段时间Δ t 2 内,量热计向环境辐射出能量而造成的温度降低,故需添上,由此可见 E , F 两点的温度差较客观地表示了样品燃烧后,使量热计温度升高的值。
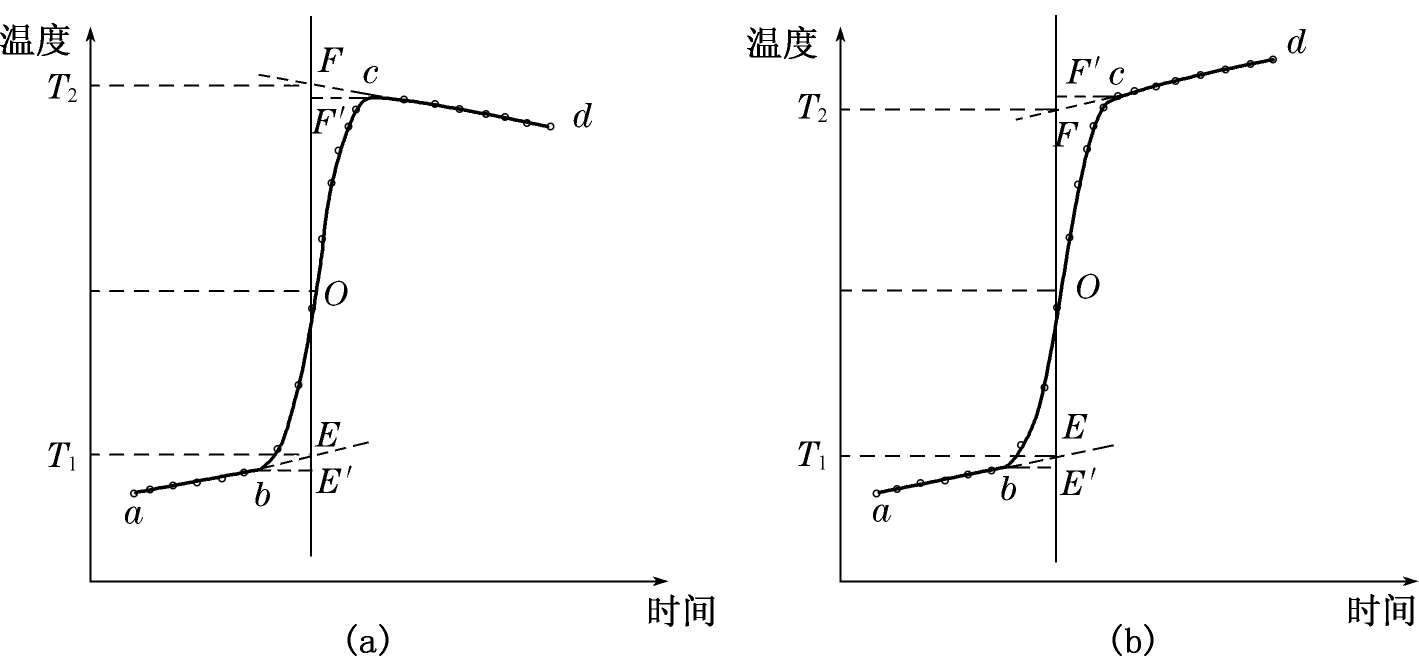
图2.2-3 雷诺校正图
有时量热计绝热情况良好,热漏小,但由于搅拌不断产生少量能量,使燃烧后最高点不出现,如图2.2-3(b)所示,这时Δ T 仍可按相同原理校正。
3.对其他热效应的测量(如溶解热、中和热、化学反应热等)可用普通杜瓦瓶作为量热计。也是用已知热效应的反应物先求出量热计的水当量,然后对未知热效应的反应进行测定。对于吸热反应可用电热补偿法直接求出反应热效应。
参考文献
1.傅献彩,沈文霞,姚天杨.物理化学(第四版).北京:高等教育出版社,1990
2.孙尔康,徐维清,邱金恒.物理化学实验.南京:南京大学出版社,1997
3.北京大学化学系物理化学教研室.物理化学实验(修订本).北京:北京大学出版社,1985
4.罗澄源等.物理化学实验(第二版).北京:高等教育出版社,1984

