实验2.4
中和热的测定
一、目的
1.掌握中和热的概念及测定方法,了解测定量热计热容的几种方法。
2.掌握“量热法”测定中和热,理解“量热法”原理。
3.学习用图解法进行数据处理以求得正确Δ T 的方法。
4.测定盐酸、醋酸与氢氧化钠反应的中和热,并计算醋酸的解离热。
二、基本原理
在一定的温度、压力和浓度下,1 mol酸和1 mol碱中和所放出的热量叫做中和热。对于强酸和强碱在水溶液中几乎完全电离,中和反应的实质是溶液中的氢离子和氢氧根离子反应生成水,这类中和反应的中和热与酸的阴离子和碱的阳离子无关。热化学方程式可用离子方程式表示为:

当在足够稀释的情况下中和热是不随酸和碱的种类而改变的,中和热几乎是相同的。(2.4-1)式可作为强酸和强碱中和反应的通式。在20℃时:Δ H 中和 =-57.11 kJ·mol -1 ,25℃时:Δ H 中和 =-57.3 kJ·mol -1 。若所用溶液相当浓,则所测得的中和热数值常较高。这是由于溶液相当浓时,离子间相互作用力及其他因素影响的结果。若所用的酸(或碱)只是部分电离的弱酸(或弱碱),当其与强碱(或强酸)发生中和反应时,其热效应是中和热和解离热的代数和,因为在中和反应之前,首先弱酸要进行解离。例如,醋酸和氢氧化钠的反应如下:
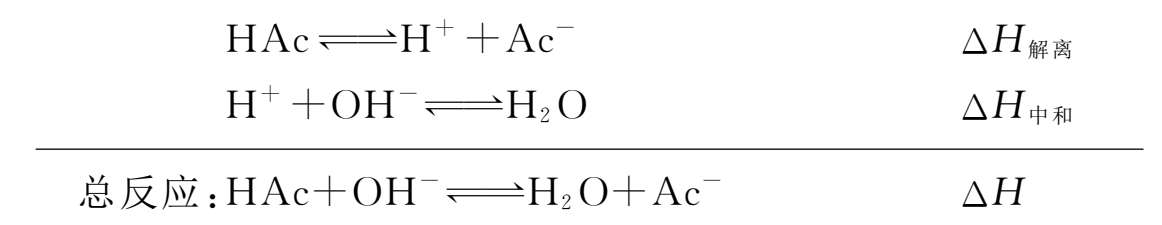
根据盖斯定律,有
Δ H =Δ H 解离 +Δ H 中和 ,
所以

实验需标定量热计的热容,常用确定量热计热容的方法有三种:
①电热标定法。对量热计及一定量的水在一定的电流、电压下通电一定时间,使量热计升高一定温度,根据供给的电能及量热计温度升高值,计算量热计的热容 C 。
②化学标定法。使已知热效应的反应过程在量热计中发生,根据量热计的温度升高值,来计算量热计的热容 C 。
③混合平衡法。向一定量的水中加入一定量的冰水混合物达到温度平衡,由热量平衡关系计算量热计的热容 C 。
本实验是采用电热法标定量热计的热容。
在杜瓦瓶中盛以一定量的水,搅拌,用贝克曼温度计相隔一定时间测温,在温度变化稳定后,在一定的电流、电压下通电一定时间,使量热计升高一定温度,根据供给的电能(
 )及量热计温度升高值(Δ
T
),由下式计算量热计的热容
C
:
)及量热计温度升高值(Δ
T
),由下式计算量热计的热容
C
:

三、仪器与试剂
杜瓦瓶量热计(1 000 mL)1套(含贝克曼温度计、电加热器、电动(或手动)搅拌器、盛液管),直流稳压电源(或蓄电池)1套,可变电阻2个,电流表(0~3 A)1台,电压表(0~3 V) 1台,单刀双掷开关1个,计时器(或秒表)1块,放大镜1个,移液管(50 mL)2支,容量瓶(500 mL,250 mL,100 mL,50 mL)各1个。
1.000
 NaOH溶液(新配制并已准确标定),1.000
NaOH溶液(新配制并已准确标定),1.000
 HCl标准溶液,1.000
HCl标准溶液,1.000
 HAc标准溶液。
HAc标准溶液。
四、实验步骤
1.量热计的组装
按图2.4-1所示装好量热系统,调节贝克曼温度计(调节方法见5.1)使水银面位于1~2之间。
2.电加热器的连接
按图2.4-2接好加热器线路,稳压电源P输出的电流经滑线电阻 R 1 加在电加热器L上,滑线电阻 R 1 用来调节电流强度。
可以从电流表A和电压表V读出电流和电压值。 R 2 是与电加热器L的电阻相当的降压电阻(约5Ω)。开关K倒向接点2时,电流在滑线电阻 R 1 和电阻 R 2 上放电,使直流电源系统在电加热器上处于较稳定的工作状态。

图2.4-1 量热计装置图
1.搅拌器;2.贝克曼温度计;3.内管;4.杜瓦瓶;
5.碱液;6.酸液;7.电加热器
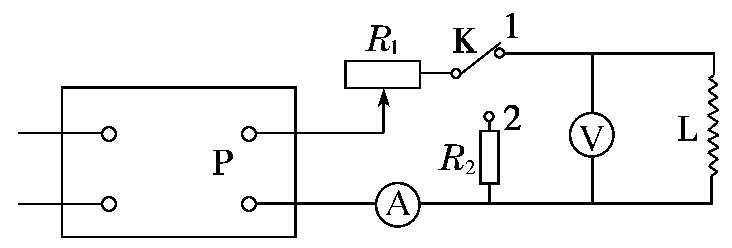
图2.4-2 电加热器线路图
3.量热计热容的测定
在干净干燥的杜瓦瓶中准确加入500 mL蒸馏水,塞紧瓶塞。开动搅拌器,按动秒表每分钟记录一次水温,记录10分钟(注意:在每次读数前,都要用套有橡皮胶管的玻锤轻击贝克曼温度计水银面附近几下,以消除水银在毛细管中的粘滞现象)。读取第10个数的同时,将电加热器中的开关K倒向2,使电流保持在1.0 A左右的某一定值,每30秒记录一次温度(注意电流、电压必须保持原来指定值,否则,需随时调节)。待水温升高0.8~1.0℃时,停止加热,并记录电流、电压、通电时间,继续搅拌,每分钟记录一次水温,测量10分钟为止。由雷诺作图法确定温度的变化Δ T 1 。
按上述操作方法重复两次,取其平均值。
4.强酸强碱中和热的测定
在干净干燥的杜瓦瓶中,用容量瓶加入400 mL蒸馏水,再用移液管准确量取50 mL,1.000
 的NaOH标准溶液,注入杜瓦瓶中,然后用另一支移液管吸取 50 mL,1.100 mol·L
-1
的HCl溶液,小心地注入内管中,搅拌,并开始记录时间,每分钟记录一次温度,记录10 min,在内管上端用洗耳球迅速打入空气,使管内的HCl溶液迅速地压入杜瓦瓶内与NaOH溶液反应。记录开始反应的时间,此时温度升高很快,每隔30秒记录一次温度,待温度变化不大时,每分钟记录一次,记录10次为止。由雷诺作图法确定温度的变化Δ
T
2
。
的NaOH标准溶液,注入杜瓦瓶中,然后用另一支移液管吸取 50 mL,1.100 mol·L
-1
的HCl溶液,小心地注入内管中,搅拌,并开始记录时间,每分钟记录一次温度,记录10 min,在内管上端用洗耳球迅速打入空气,使管内的HCl溶液迅速地压入杜瓦瓶内与NaOH溶液反应。记录开始反应的时间,此时温度升高很快,每隔30秒记录一次温度,待温度变化不大时,每分钟记录一次,记录10次为止。由雷诺作图法确定温度的变化Δ
T
2
。
按上述操作方法重复两次,取其平均值。
5.用HAc代替HCl,重复上述操作,求得Δ T 3 。
五、数据处理
将数据记录于表2.4-1中。
表2.4-1 实验数据
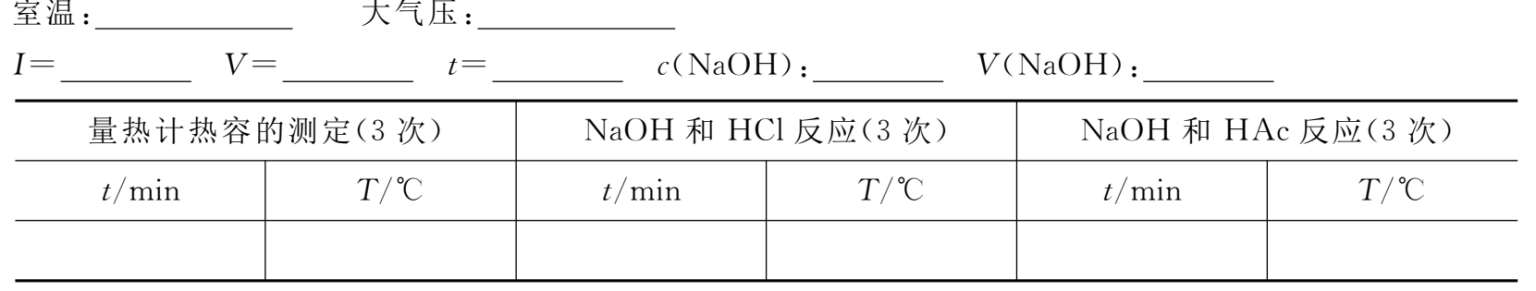
1.求温差Δ T 。由于温度计、量热计的热滞后性电加热后需要一,段时间才能升到最高温度。而量热计是非严格的绝热系统,在升温的时间里难免与环境间发生微小的热传递。为了消除热传递的影响,求得绝热条件下的准确温升,可采用图2.4-3所示的外推法,即雷诺图解法。根据实验记录的贝克曼温度计读数与时间的数据,作出温度-时间曲线。取图中迅速升温阶段时的中点(或电加热时间的中点)作垂线。此垂线与迅速升温前后温度缓慢变化阶段直线的延长线相交于 A , B 两点, A , B 两点相应纵坐标读数之差为绝热条件下准确的温升。
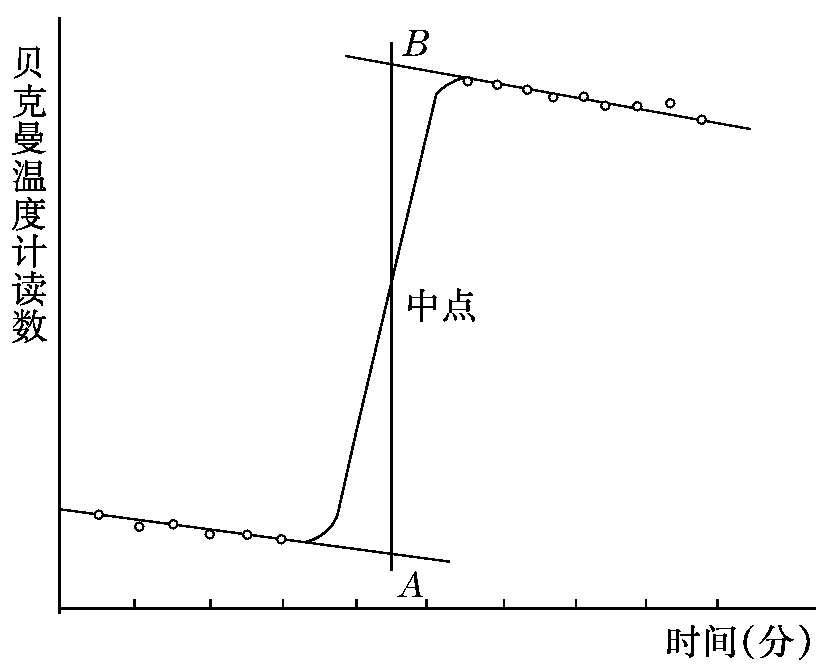
图2.4-3 雷诺校正图
用上述方法分别求电加热测热容及中和反应的准确温升。
2.量热计热容的计算。列表记录标定量热计热容时的时间-温度数据,用雷诺图解法求出Δ T 1 ,并根据(2.4-3)式计算量热计热容 C 。
3.列表记录强酸强碱中和反应的时间-温度数据,用雷诺图解法求出Δ T 2 ,并计算:
Δ H 中和 =- C ·Δ T 2 / c · V 。
4.列表记录弱酸强碱中和反应的时间-温度数据,计算Δ H 和醋酸的解离热:
Δ H 解离 =Δ H -Δ H 中和 。
5.将中和热的实验值与文献值比较求实验值的相对误差(此误差一般小于3~5%)。强酸强碱中和热文献值用下式表示:
Δ H 中和 =-57 110+209.2( t /℃-25)(J·mol -1 ),
式中 t 为中和反应的摄氏温度。本实验中应为中和反应前的温度,用此式求得本实验温度下的中和热文献值。
6.结合计算公式,进行误差分析。
六、讨论
1.用吹出管加样的方法,目的是使酸和碱液在反应前都处于同一个温度,消除温度不同而带来的误差。
2 .中和热和电离热都与浓度和温度有关,由基尔霍夫定律可知[
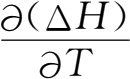 ]
p
=Δ
C
p
,强酸强碱中和热随温度升高而减少,因此在阐述中和过程和电离过程的热效应时,必须注意记录酸和碱的浓度以及测量的温度。
]
p
=Δ
C
p
,强酸强碱中和热随温度升高而减少,因此在阐述中和过程和电离过程的热效应时,必须注意记录酸和碱的浓度以及测量的温度。
3.实验中所用酸的浓度要略高于碱的浓度,或使酸的用量略多于碱的量,以使碱全部被中和。为此,应在实验后用酚酞指示剂检查溶液的酸碱性。
4.实验所用NaOH溶液必须用丁二酸或草酸进行标定,并且尽量不含CO 3 2- ,所以最好现用现配。
5.实验中通常采用机械搅拌的方式使体系温度均匀并使反应充分,这就引进了非体积功。所以严格说来,此时反应热与焓变不相等,二者相差一非体积功,即Δ H = Q - W′ 。同时由于搅拌而产生的热量也对实验结果有一定的影响。
6.实验中将酸碱的热容视为与水相同,并假设量热计完全绝热,这与实际情况都有出入,必然导致一定的误差。
7.如果所用酸、碱的浓度偏高,则由于离子间的相互作用力的变化及其影响,而使中和热测定值偏高。通常取0.1~0.5 mol·L -1 的浓度较为适宜。
8.实际上,所用的酸和碱均有一定的浓度,在中和反应发生的同时,还发生酸碱的稀释,也伴随有热量产生,故在测定中和焓时,应进行稀释焓的校正。
七、结果要求和文献值
1.雷诺图实验点分布规律性良好。用雷诺图解法,求出温度变化值Δ T 。
2.NaOH和HAc中和热的文献值见相关手册。
八、思考题
1.弱酸的电离是吸热还是放热?
2.中和热除与温度、压力有关外,还与浓度有关,如何测量在一定温度下,无限稀释时的中和热?
3.一般中和热文献值为无限稀释中和反应的热效应,而实验中所用酸的浓度不是无限稀,实测热效应与文献值可能有什么差别,应再测什么数据才能弥补它们间的差别?
参考文献
1.罗澄源等.物理化学实验.北京:人民教育出版社,1979
2.广西师范大学.物理化学实验.桂林:广西师范大学出版社,1991
3.东北师范大学等.物理化学实验(第二版).北京:高等教育出版社,1989
4.石油大学物理化学教研室.物理化学实验.东营:石油大学出版社,1990

