实验2.7
液相反应平衡常数的测定
一、目的
1.利用分光光度计测定低浓度下铁离子与硫氰酸根离子生成硫氰合铁配离子液相反应的平衡常数。学习一种液相反应平衡常数的测定方法。
2.通过实验进一步理解热力学平衡常数的数值不因反应物起始浓度不同而发生变化。
3.掌握分光光度计的使用。
二、基本原理
在水溶液中,铁离子(Fe 3+ )与硫氰酸根离子(SCN - )可生成一系列的配离子,并共存于同一平衡系统中,但当铁离子与硫氰酸根离子的浓度很低时,只有如下的反应

即反应被控制在仅仅生成最简单的FeSCN 2+ 配离子。其平衡常数表示为

通过实验和计算可以看出,在同一温度下,改变铁离子(或硫氰酸根离子)浓度时,溶液的颜色改变,平衡发生移动,但平衡常数 K c 保持不变。
当溶液的浓度很低时,根据朗伯-比尔定律可知,吸光度(又称光密度、消光度)与溶液浓度成正比。因此,可借助于分光光度计测定其吸光度,从而计算出平衡时硫氰合铁配离子的浓度及铁离子和硫氰酸根离子的浓度,再根据(2.7-2)式计算出该反应的平衡常数 K c 。
三、仪器与试剂
721型分光光度计1台,烧杯(50 mL)6个,移液管(5 mL,10 mL,15 mL)各3支。
4×10 -4 mol·L -1 NH 4 SCN溶液,1×10 -1 mol·L -1 和4×10 -2 mol·L -1 FeCl 3 溶液。
四、实验步骤
1.不同浓度试样的配制
取四个50 mL的烧杯,编成1,2,3,4号。用移液管向各编号的烧杯中各加入5 mL,4×10 -4 mol·L -1 的NH 4 SCN溶液。另取四种浓度各不相同的Fe 3+ 溶液各5 mL,分别注入各编号的烧杯中。使体系中SCN - 的初始浓度与Fe 3+ 的初始浓度达到表2.7-1中所示的数值。为此,可按以下步骤配制不同浓度的Fe 3+ 溶液:
在1号烧杯中直接注入5 mL,1×10 -1 mol·L -1 的Fe 3+ 溶液;
在2号烧杯中直接注入5 mL,4×10 -2 mol·L -1 的Fe 3+ 溶液;
取 50 mL烧杯一个,注入 10 mL ,4×10 -2 mol·L -1 的Fe 3+ 溶液,然后加纯水15 mL稀释,取此稀释液(Fe 3+ 离子浓度为1.6×10 -2 mol·L -1 )5 mL加到3号烧坏中;另取稀释液(即Fe 3+ 离子浓度为1.6×10 -2 mol·L -1 )10 mL加到另一个50 mL的烧杯中,再加纯水15 mL,配制成浓度为6.4×10 -3 mol·L -1 的Fe 3+ 溶液,取此溶液5 mL加到4号烧杯中。
2.分光光度计的调节与溶液吸光度测定
选择颜色较深的溶液放入光路中,测定不同波长下的吸光度,以吸光度作纵坐标,波长作横坐标绘制吸收光谱图,选其中最大收时的波长作为比色分析的入射光波长。
将721型分光光度计调整好,并把波长调到 λ 最大 处,然后分别测定上述四个编号烧杯中各溶液的吸光度。
五、数据处理
1.将测得的数据填于表2.7-1中,并计算出平衡常数 K c 值。
表2.7-1实验数据及数据处理结果

表2.7-1中数据按下列方法计算:
对1号烧杯[Fe 3+ ]与[SCN - ]反应达平衡时,可认为[SCN - ]全部消耗,此平衡时硫氰合铁离子的浓度为反应开始时硫氰酸根离子的浓度。即为:
[FeSCN 2+ ] 平(1) =[SCN - ] 始 。
以1号溶液的吸光度为基准,计算2,3,4号溶液的吸光度与1号溶液的吸光度之比,而2,3,4号各溶液中[FeSCN 2+ ] 平 ,[Fe 3+ ] 平 ,[SCN - ] 平 可分别按下式求得:

根据(2.7-2)式计算平衡常数。
2.结合计算公式,进行误差分析。
六、思考题
1.可能引起本实验误差的因素是什么?
2.你认为如何提高本实验的精度?
3.如Fe 3+ ,SCN - 浓度较大时,则不能按公式来计算 K c 值,为什么?
4.为什么由公式[FeSCN 2+ ] 平 =吸光度比×[SCN - ]可计算出[FeSCN 2+ ] 平 ?
七、附录:721,722型分光光度计的工作原理、光学系统和维护使用
1.分光光度计的工作原理
分光光度计的基本原理是溶液中的物质在光的照射激发下,产生了对光吸收的效应,物质对光的吸收是具有选择性的。各种不同的物质都具有其各自的吸收光谱,因此当某单色光通过溶液时,其能量就会被吸收而减弱,光能量减弱的程度和物质的浓度有一定的比例关系,也即符合于比色原理——比耳定律,即
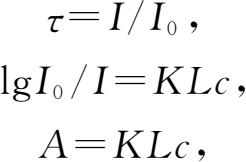
式中: τ 为透射比; I 0 为入射光强度; I 为透射光强度; A 为吸光度; K 为吸收系数; L 为溶液的光径长度; c 为溶液的浓度。
从以上公式可以看出,当入射光、吸收系数和溶液的光径长度不变时,透过光是根据溶液的浓度而变化的。
2.721型分光光度计
721型分光光度计的仪器外形见图2.7-1。

图 2.7-1 721型分光光度计的外形
1.波长导轮;2.0% T 旋钮;3.100% T 旋钮;4.灵敏度旋钮;
5.比色池盖;6.试样架拉手;7.光波长读数看窗;8.微安表
721型分光光度计采用自准式光路,单光束方法,其波长范围为360~800 nm,用钨丝白炽灯泡作光源,其光学系统如图2.7-2所示。
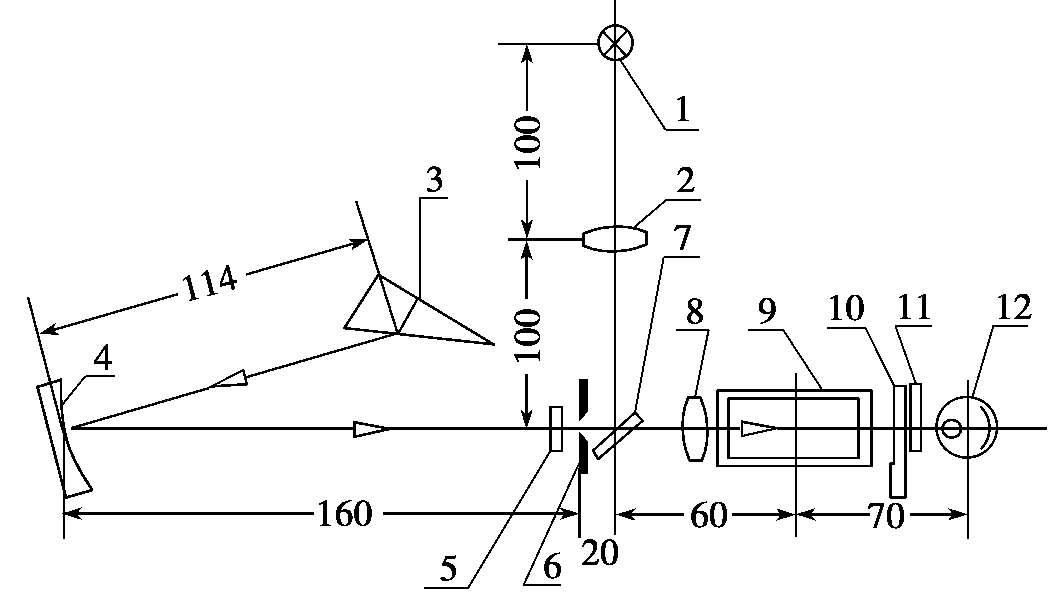
图2.7-2 721型分光光度计的光学系统
1.光源灯12 V,25 W;2.聚光透镜;3.色散棱镜;4.准直镜;5.保护透镜;6.狭缝;
7.反射镜;8.聚光透镜;9.比色皿;10.光门;11.保护玻璃;12.光电管
由光源灯发出的连续辐射光线,射到聚光透镜上,会聚后再经过平面镜转角90°,反射至入射狭缝。由此入射到单色光器内,狭缝正好位于球面准直镜的焦面上,当入射光线经过准直镜反射后就以一束平行光射向棱镜(该棱镜的背面镀铝),光线进入棱镜后,就在其中色散,入射角在最小偏向角,入射光在铝面上反射后是依原路稍偏转一个角度反射回来,这样从棱镜散射后出来的光线再经过物镜反射后,就会聚在出光狭缝上,出光狭缝和入光狭缝是一体的,为了减少谱线通过棱镜后呈弯曲形状对于单色性的影响,因此把狭缝的两片刀口作成弧形的,以便近似地吻合谱线的弯曲度,保证了仪器及一定幅度的单色性。
3.722型光栅分光光度计
722型光栅分光光度计采用光栅自准式色散系统和单光束结构光路。仪器外形如图2.7-3 所示。

图2.7-3 722型光栅分光光度计的外形
1.数字显示器;2.吸光度调零旋钮;3.选择开关;4.吸光度调斜率电位器;5.浓度旋钮;6.光源室;7.电源开关;
8.波长手轮;9.波长刻度窗;10.试样架拉手;11.100% T 旋钮;12.0% T 旋钮;13.灵敏度调节旋钮;14.干燥器
钨灯发出的连续辐射光经滤色片聚光镜聚光后投向单色器进入狭缝,此狭缝正好处于聚光镜及单色器内准直镜的焦平面上,因此进入单色器的复合光通过平面反射镜反射及准直镜准直变成平行光射向色散元件光栅,光栅将入射的复合光通过衍射作用形成按照一定顺序均匀排列的连续单色光谱,此单色光谱重新回到准直镜上,由于仪器出射狭缝设置在准直镜的焦平面上,这样,从光栅色散出来的光谱经准直镜后利用聚光原理成像在出射狭缝上,出射狭缝选出指定带宽的单色光通过聚光镜落在试样室被测样品中心,样品吸收后透射的光经光门射向光电管阴极面。光学系统光路见图2.7-4,图中保护玻璃为防止灰尘进入单色器而设,与原理无关。
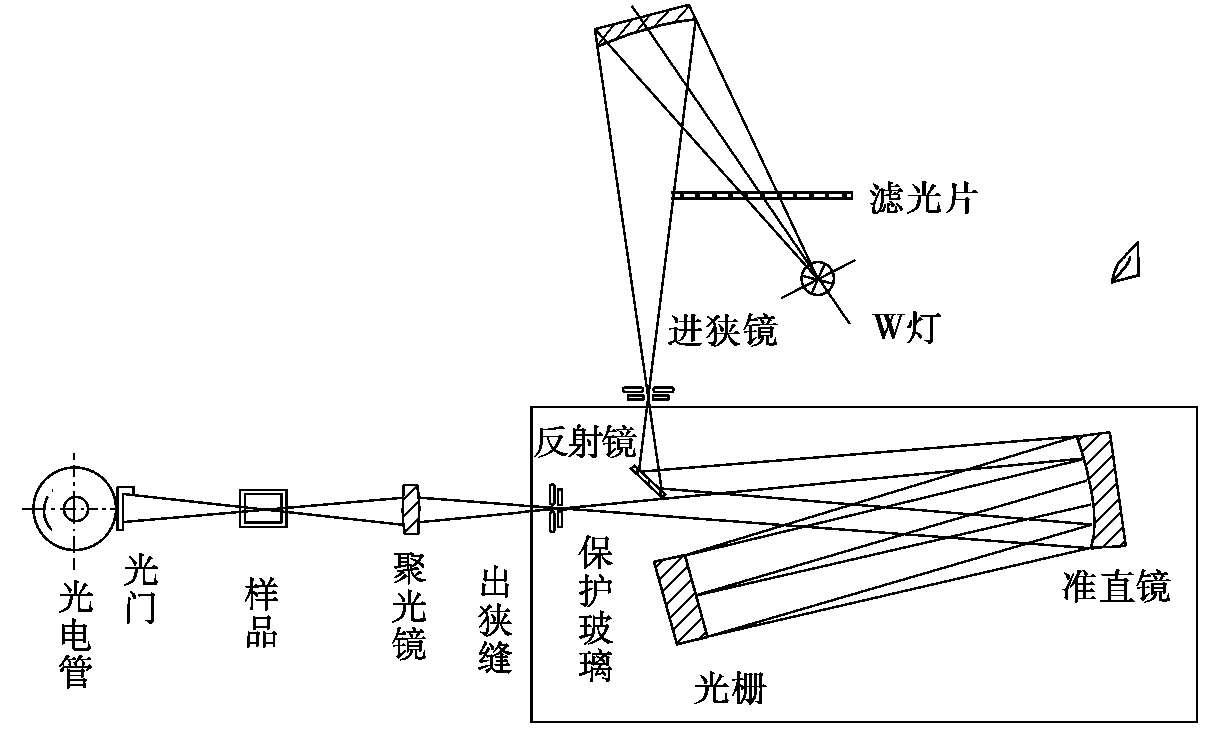
图2.7-4 722型光栅分光光度计的光学系统
4.分光光度计的维护使用
(1)为确保仪器稳定工作,在电源波动较大的地方,最好使用交流稳定电源。
(2)当仪器停止工作时,应关闭仪器电源开关,再切断电源。
(3)为了避免仪器积灰和玷污,在停止工作的时间里,用防灰罩罩住仪器,同时在罩子内放置数袋防潮剂,以免灯室受潮、反射镜镜面发霉或玷污,影响仪器日后的工作。仪器工作数月或搬动后,要检查波长准确度,以确保仪器的使用和测定精度。
参考文献
1.南开大学化学系物理化学教研室.物理化学实验.天津:南开大学出版社,1991
2.吴子生,严忠.物理化学实验指导书(第一版).长春:东北师范大学出版社,1995
3.东北师范大学等.物理化学实验(第二版).北京:高等教育出版社,1989

