实验2.8
合成氨反应平衡常数的测定
一、目的
1.掌握流动法测定气-固催化反应平衡常数的一般技术。
2.测定合成氨反应在不同温度下的平衡常数。
3.用化学反应的等压方程和等温方程计算合成氨的
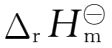 ,
,
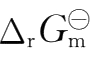 和
和
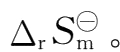
二、基本原理
将反应物连续地通过反应器,生成的产物不断地从反应器中分离出去,这类反应系统的实验方法称为流动法。流动法测定合成氨反应的平衡常数可以通过两种方法来实现:
①以氮、氢为原料气,经过精确控温的铁催化剂层,然后分析反应达到平衡状态的尾气,尾气的组成就是在催化剂温度下合成氨反应系统的平衡组成,由平衡组成可求算平衡常数。
②以氨分解法进行测定。以氨为原料气,经过精确控温的催化反应器,此反应器中装有足够量的铁催化剂,氨气流经过催化剂后发生分解反应并达到平衡状态,测定反应的尾气组成,即可以求算合成氨反应的平衡常数。
本实验采用第一种方法,合成氨反应的计量方程式为:

反应在常压下进行,假设反应混合物为理想气体,反应的标准平衡常数
 可用各组分的平衡分压表示
可用各组分的平衡分压表示

反应的时间为 t (s),标准状态下气体的流速为 v ,在 t 时间内进入反应器的N 2 ,H 2 的物质的量分别为 n 0 (N 2 ), n 0 (H 2 ), t 时间内离开反应器的N 2 ,H 2 ,NH 3 物质的量分别为 n (N 2 ), n (H 2 ), n (NH 3 ),则物料衡算有 n (N 2 )= n 0 (N 2 )-1/2 n (NH 3 ), n (N 2 )= n 0 (H 2 )-3/2 n (NH 3 ),由于在一定的温度和压力下,一定时间内流入与流出的气体的物质的量与流速成正比,所以
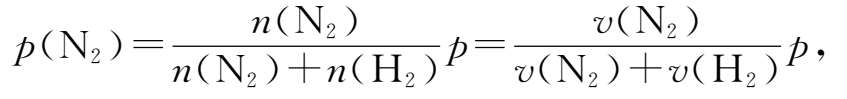
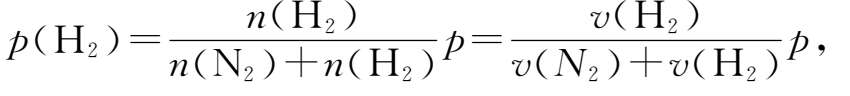
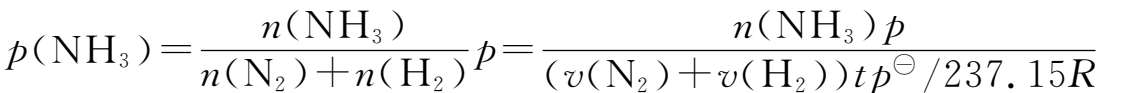
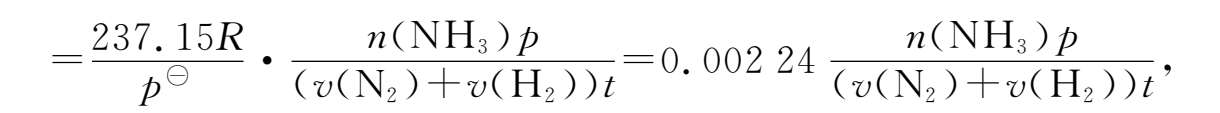
代入(2.8-1)式得
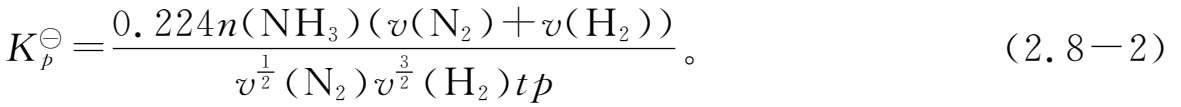
由实验测得在
T
及总压
p
下的N
2
,H
2
的流速,
t
时间内产生的NH
3
的物质的量,代入(2.8-2)式即可求得反应温度为
T
K时得
 值。
值。
化学反应的等压方程为:

上式近似认为
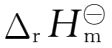 与温度无关,积分,得
与温度无关,积分,得

式中
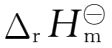 为反应的标准反应热,如测得不同温度下的
为反应的标准反应热,如测得不同温度下的
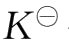 值,则可由
值,则可由
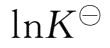 对1/
T
作图求得
对1/
T
作图求得
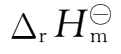 。
。
又由化学反应的等温方程式
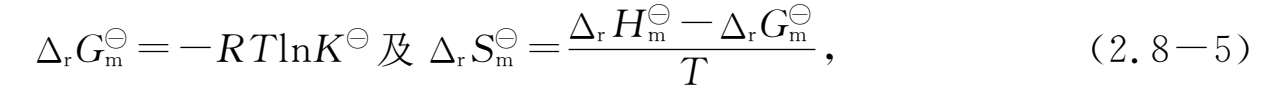
即可求得相应温度下的
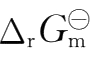 和
和
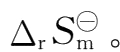
三、仪器与试剂
实验装置1套(如图2.8-1所示),5A型分子筛,AgX型分子筛,纯氮钢瓶,纯氢钢瓶,温度控制器,磁力搅拌器,秒表,热电偶。
18~36目的A6催化剂,1.0×10 -3 mol·L -1 的H 2 SO 4 溶液。
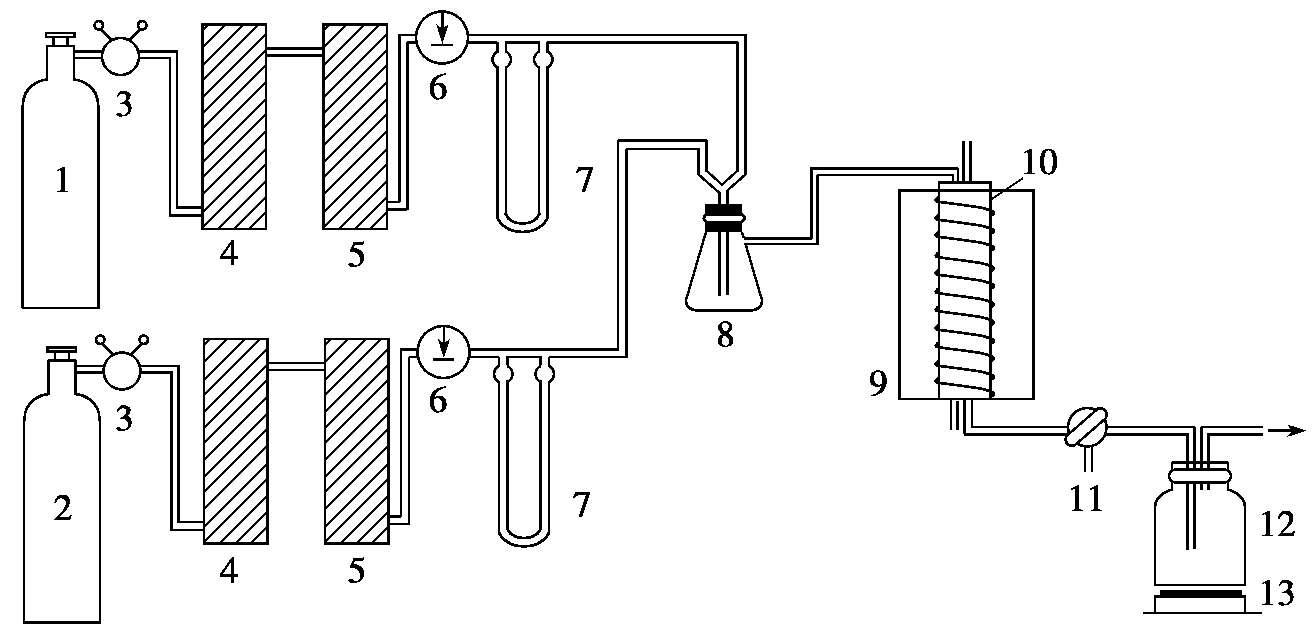
图2.8-1 合成氨反应平衡常数测定装置
1.氮气瓶;2.氢气瓶;3.减压阀;4.5A型分子筛干燥塔;5.AgX型分子筛干燥塔;6.针形阀;7.毛细管流量计;
8.气体混合瓶;9.管式电炉;10.石英反应器;11.三通阀;12.吸收瓶;13.磁力搅拌器;14.热电偶导管
四、实验步骤
1.按图2.8-1安装各种仪器,安装好热电偶,将催化剂置于管式电炉中,仔细检查整个线路是否严密不漏气。
2.将三通阀旋至放空位置,打开氢气钢瓶,调节针形阀,使氢气的流速为27 mL·min -1 左右,接通电炉电源,慢慢升温到450℃,恒温1 h,然后升温到550℃。
3.打开氮钢瓶,调节针形阀,使氮气的流速为9 mL·min -1 左右。应控制氮气和氢气的流速之比为1∶3。
4.在NH 3 吸收瓶中加入1 mL,1.0×10 -3 mol·L -1 H 2 SO 4 标准溶液,再加入20 mL蒸馏水和三滴甲基红指示剂。
5.待氮气和氢气流速和反应温度稳定后,记下氮气和氢气的流速和反应温度。打开磁力搅拌器,将三通阀旋到与出气口玻璃管相通的位置,稍待一会后,再将出口玻璃管插入吸收瓶溶液内,当第一个气泡鼓出时按下秒表,记录吸收液变色所用的时间 t 。
6.重复步骤4,5操作,测得重现性较好的有关数据。
7.升温到600℃,650℃,700℃,750℃,同法分别测得各个温度下的有关数据。
五、数据处理
1.列表记录实验测得各个温度下的有关数据,并计算出
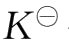 。
。
2.以lg
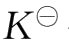 对1/
T
作图,求
对1/
T
作图,求
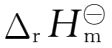 。
。
3.由等温方程式计算出
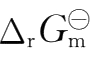 和
和
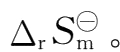
4.结合计算公式,进行误差分析。
六、思考题
1.为什么氮气和氢气的流速比要调节为1∶3?
2.实验应注意控制哪些条件?
3.实验的误差主要来源于温度的控制、反应终点的控制和流速的控制,试简要说明之。
参考文献
1.吴子生,严忠.物理化学实验指导书(第一版).长春:东北师范大学出版社,1995
2.北京大学化学系物理化学教研室.物理化学实验(第一版).北京:北京大学出版社,1985
3.广西师范大学等.基础物理化学实验(第一版).桂林:广西师范大学出版社,1991
4.陈龙武,邓希贤,朱长缨.物理化学实验技术(第一版).上海:华东师范大学出版社,1986

